Магний. Общая информация
Mg присутствует во всех тканях организма, более половины его находится в костной ткани. Общее содержание магния в организме человека составляет около 25 г, наибольшую концентрацию иона отмечают в тканях с интенсивным обменом веществ. Ионы магния преимущественно содержатся внутри клетки, где они связаны с белками; присутствуют в ядре, митохондриях, цитоплазматическом ретикуломе; в цитоплазме около 80% магния находится в комплексе с АТФ. Внеклеточный магний (в т. ч. магний плазмы крови) составляет лишь 1% от общего количества, содержащегося в организме.
Магний является облигатным кофактором многих ферментативных реакций: необходим для реакций гликолиза, для образования АТФ при окислительном фосфорилировании в митохондриях. Магний выступает в роли физиологического регулятора клеточного роста, поддерживая адекватный запас пуриновых и пиримидиновых нуклеотидов, необходимых для синтеза ДНК и РНК. Истощение запасов Mg2+ в клетке приводит к снижению синтеза белка; магний необходим на всех этапах синтеза белковой молекулы. Активация и ингибирование системы ц-АМФ, медиатора многих физиологически активных веществ, связаны с магнием: он повышает активность аденилатциклазы и формирование циклического АМФ.
Магний поступает в организм с пищей и водой. Сбалансированная диета содержит 300–350 мг/сут, недостаток магния в пище может быть причиной дефицита элемента в организме. Главным источником магния являются орехи, овес, зелень, мясо. Большая часть магния абсорбируется в тонком кишечнике. Витамин D и его метаболиты повышают абсорбцию Mg, но в меньшей степени, чем Ca. Избыток в пище органических кислот связывает Mg, нарушая его всасывание. При усиленном поступлении Mg с пищей, при парентеральном введении, избыток катиона быстро экскретируется почками, которые являются основным регулятором поддержания постоянной концентрации Mg в организме. При истощении запасов Mg его экскреция снижается или прекращается вообще.
Активное участие Mg в различных физиологических процессах является основой многообразия клинической симптоматики при гипо- и гипермагниемии. Расстройства, связанные с дефицитом магния, имеют сложный характер и обычно сопровождаются множественными нарушениями обмена веществ. Клинические симптомы недостаточности Mg носят преимущественно неврологический характер: сонливость, слабость, раздражительность, тетания, тремор и фасцикуляции (подергивания) мышц, также отмечают тошноту и рвоту. Неврологические симптомы, особенно тетания, коррелируют с развитием гипокальциемии и гипокалиемии.
Недостаток магния в организме человека выявляют при многих ССЗ. Магний оказывает влияние на функциональное состояние эндотелия, участвующего в регуляции сосудистого тонуса, гемостаза, иммунного ответа, миграции клеток крови в сосудистую стенку, синтеза факторов воспаления и их ингибиторов. Неблагоприятные эффекты дефицита магния отмечают в виде повышения тонуса коронарных сосудов, увеличения чувствительности к вазоконстрикторным агентам (серотонин, ангиотензин, норадреналин, ацетилхолин), развития гипертонии и аритмии. У пациентов с ИБС содержание Mg в сыворотке крови часто понижено; резкое падение концентрации Mg в крови может быть одной из причин внезапной смерти. При гипомагниемии отмечают изменения данных ЭКГ: удлинение интервала Q–T и PR(Q); депрессия сегмента ST; инверсия зубца T и др.
Гипомагниемия наблюдается при разнообразной эндокринологической патологии: тиреотоксикоз, первичный гипоальдостеронизм, около 30% больных СД имеют разную степень гипомагниемии. Концентрация магния оказывает влияние на уровень ПТГ: как повышенное, так и пониженное содержание иона в крови угнетает секрецию гормона. При значительном снижении содержания магния в крови часто наблюдают выраженную гипокальциемию, что, по мнению многих исследователей, является следствием развития острого гипопаратиреоза, вызванного торможением секреции ПТГ. Неэффективность лечения гипокальциемии витамином Д в ряде случаев обусловлена именно гипомагниемией; инъекции сульфата магния способствую нормализации уровня кальция.
Физиологически магний выступает как антагонист кальция; его дефицит сопровождается накоплением кальция в сыворотке крови. Гиперкальциемия, понижая реабсорбцию Mg в почечных канальцах, в свою очередь способствует гипомагниемии.
При гипермагниемии наряду с неврологической симптоматикой (параличи, атаксия, сонливость, нарушения сознания) отмечают расстройства функционирования ЖКТ (тошнота и рвота), гипотензию, брадикардию, изменения данных ЭКГ (удлинение интервалов P-R и QT, расширение комплексов QRS). Значительное увеличение концентрации магния может быть причиной комы, остановки сердца и дыхания.
Гипермагниемия может быть вызвана избытком поступления иона, нарушением работы почек, наблюдается также при гипотиреозе, лактацидозе, гепатите, злокачественных новообразованиях.
Магний в кардиологической практике
Магний, впервые выделенный английским химиком Гемфри Дэви в 1808 г., является двухвалентным металлом с массой 24,301; в ионизированной форме он представляет собой положительный ион – катион – с зарядом 2+ (Mg ++ ). Вместе с еще 11 основными структурными химическими элементами человеческого организма (углерод, водород, кислород, азот, натрий, калий, кальций, хлор, фосфор, сера и фтор) магний определяет 99% элементарного состава тела. По содержанию в организме он занимает четвертое место среди других катионов (после натрия, калия и кальция), а по содержанию в клетке – второе (после калия).
В качестве кофактора пируватдегидрогеназного комплекса Mg ++ регулирует поступление продуктов гликолиза в цикл Кребса и этим препятствует накоплению лактата. Он участвует в синтезе и распаде нуклеиновых кислот, синтезе белков, жирных кислот и липидов, в частности, фосфолипидов, а также контролирует синтез ц-АМФ – универсального регулятора клеточного метаболизма и множества физиологических функций.
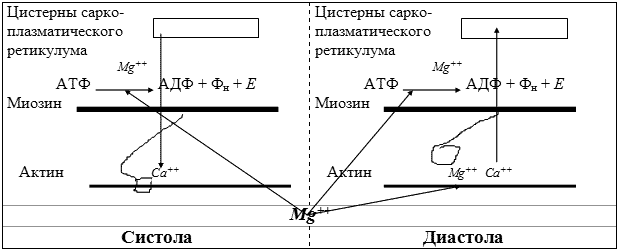
Принимая участие в высвобождении требующейся для функционирования мышечной клетки энергии и играя одну из главных ролей в расслаблении миоцита, Mg ++ контролирует цикл систола-диастола (рис. 1).
Рис. 1. Регуляция ионами Mg ++ цикла “систола-дистола” (гипотетическая схема)
Так же в эксперименте продемонстрировано, что Mg ++ ингибирует протромбин, тромбин, фактор Кристмаса, проконвертин и плазменный компонент тромбопластина, а также его антиагрегантное действие.
Среди метаболических функций проявляющихся на уровне целого организма, необходимо подчеркнуть его роль в поддержании нормального липидного спектра, участие в обеспечении ответа тканей на инсулин и торможение гормона паращитовидной железы.
Несмотря на то, что магний широко распространен в природе, его дефицит в человеческой популяции встречается чрезвычайно часто. Так, гипомагнезиемия определяется у 7-11% госпитализированных кардиологических больных, причем в 2 раза чаще у пациентов отделений интенсивной терапии (Weiss, 1995). Тому имеется множество причин. Однако достоверное выявление недостатка магния представляет определенные трудности, в связи с чем его диагностика на практике нередко проводится на основании клинических признаков. Так, если в одном из скрининговых исследований, проведенных в США, было показано, что гипомагнезиемия (уровень сывороточного Mg ++ ниже 0,74 ммоль/л) встречалась в 47,1% случаев (Wang, 1990), то клинические признаки магниевого дефицита выявляются более чем у 72% взрослых американцев.
По причинам магниевый дефицит можно подразделить на первичный и вторичный.
II. Вторичный дефицит магния – явление, присущее практически всем обществам современного мира. Причин тому множество, и они с известным допущением могут быть разделены на 2 большие группы: факторы, зависящие от условий жизни и связанные с различными заболеваниями.
Б. Причины магниевого дефицита, связанные с патологическими процессами – нарушение абсорбции в связи с возрастными изменениями или заболеваниями ЖКТ (от синдрома малой абсорбции при, например, болезни Крона, до относительно небольших нарушений функции кишечника при хроническом дуодените или субклиническом течении дисбактериоза); проявления сахарного диабета и его осложнения (гипергликемия, полиурия, применение сахароснижающих средств, диабетическая нефропатия с нарушением реабсорбции); гипергликемия любого происхождения (в том числе и ятрогенная); почечный ацидоз, нефротический синдром; гиперкортицизм; гипер-катехоламинемия; гиперальдостеронизм; гипертиреоз; гиперпаратиреоз; гиперкальциемия; артериальная гипертензия; инфаркт миокарда; застойная сердечная недостаточность; факторы риска ИБС, в частности ожирение; передозировка сердечных гликозидов; диуретическая, глюкокортикоидная, цитостатическая терапия.
Дефицит Mg ++ проявляется разнообразными клиническими симптомами и синдромами, которые можно сгруппировать следующим образом (табл. 1). Поскольку неоднородность распределения Mg ++ в тканях организма делает мало информативным определение его содержания в сыворотке или эритроцитах, заподозрить магниевый дефицит можно на основании сочетания отдельных клинических признаков магниевого дефицита, особенно, если они затрагивают различные системы и наблюдаются на фоне значимого провоцирующего фактора, например злоупотребления алкоголем.
Дефицит Mg ++ с преобладанием Са ++ и неконтролируемое вхождение последнего в кардиомиоцит лежит в основе реперфузионного синдрома, развивающегося после медикаментозной, инструментальной или спонтанной реваскуляризации миокарда при остром инфаркте и проявляющегося, прежде всего, нарушениями сердечного ритма.
Как при инфаркте миокарда, так и в других ситуациях внутриклеточный дефицит Mg ++ может служить причиной тахикардии и различных аритмий вплоть до фатальных. Выраженный магниевый дефицит сопровождается удлинением интервала QT (что, как известно, ассоциируется с развитием желудочковых нарушений ритма и внезапной смерти) и увеличением «дисперсии» QT (разницы между QTMAX и QTMIN), считающийся еще более надежным признаком высокой вероятности развития нарушений ритма, в том числе и фатальных. Наиболее характерным для дефицита Mg ++ вариантом аритмии является желудочковая тахикардия типа «пируэт» (torsade de pointes), а также индуцированные дигиталисом нарушения ритма, пароксизмальная суправентрикулярная аритмия, мономорфная желудочковая тахикардия. У пациентов с инфарктом миокарда выявлена корреляция между дефицитом магния и разнообразными желудочковыми нарушениями ритма.
Гипомагнезиемия ассоциируется с повышенной агрегацией тромбоцитов и возрастанием риска тромбозов и эмболий. При недостатке Mg ++ ослабляется антиоксидантная защита.
Магниевый дефицит (уменьшение его содержания в мышцах и эритроцитах) обнаружен у больных с пролапсом митрального клапана (Cohen et al., 1986, Durlach, 1994), для которых также характерны нарушения ритма.
Развивающийся при злоупотреблении алкоголем дефицит Mg ++ играет определенную роль в формировании многих осложнений хронической интоксикации этанолом (от поведенческих реакций до миопатии) и играет существенную роль в развитии абстинентного синдрома.
В обычных физиологических условиях кинетический цикл Mg ++ склаВ обычных физиологических условиях кинетический цикл Mg ++ складывается из абсорбции в ЖКТ, распределения в средах организма и элиминации, осуществляемой в основном путем экскреции с мочой.
Всасывание Mg ++ может осуществляться во всем кишечнике вплоть до сигмовидной кишки. Его усвояемость из пищевых продуктов составляет 30-35% (то есть из 300-350 мг суточной потребности усваивается около 100 мг). Она может увеличиваться под влиянием витамина В6 и ряда органических кислот (молочной, аспарагиновой, оротовой). Молоко и некоторые молочные продукты, содержащие казеин, также способствуют увеличению абсорбции Mg ++ (возможно, в связи с большим содержанием оротовой кислоты).
Общее количество магния в организме взрослого человека составляет 24-25 г или примерно 1000 ммоль. Наибольшая его часть – 60% – содержится в костях, формируя в содружестве с кальцием их структуру; в случае необходимости отсюда может быть мобилизовано не более 20-30%. Mg ++ является типичным интрацеллюлярным элементом – его внутриклеточная фракция составляет 39% всего его запаса (до 80-90% внутриклеточного магния находится в виде комплекса с АТФ, в связи с чем уровень АТФ является одним из основных факторов, лимитирующих накопление этого элемента в клетке). Оставшийся 1% распределяется во внеклеточном пространстве, включая и сыворотку крови, на которую приходится лишь 0,3%.
Наибольшие количества магния содержатся в тканях с наиболее интенсивными обменными процессами. Основная часть его внутриклеточной фракции практически поровну поделена между мозговой и мышечной тканями. При этом наивысшее относительное содержание Mg ++ отмечается в миокарде.
Концентрация магния в сыворотке крови составляет в норме 0,75-0,95 ммоль/л, а в клетках может достигать 5-10 ммоль/л. Однако в связи с неоднородностью его распределения в различных тканях внутриклеточная его концентрация варьирует в широких пределах, составляя, например, в эритроцитах лишь 2-2,6 ммоль/л. Содержание магния в сыворотке крови не отражает его запасы в организме, а зависит лишь от интенсивности его движения из депо к почкам. Также мало информативно и его содержание в клеточных элементах крови из-за неоднородности распределения. Поэтому лабораторная оценка магниевого обмена наиболее достоверна, если анализируется экскреция Mg ++ с мочой.
Обычно выведение Mg ++ из организма осуществляется почками, через которые теряется примерно 100 мг/сут., то есть все всосавшееся из пищи количество. При его дефиците почечная экскреция снижается или прекращается вовсе; при увеличении поступления Mg ++ увеличивается и экскреция. Его потери с мочой возрастают под влиянием катехоламинов и кортикоидных гормонов, чем объясняется возможность возникновения магниевого дефицита при стрессе. Существенные количества Mg ++ могут теряться и в случае усиления потоотделения при напряженной физической работе или тепловой нагрузке; при этом его потери с потом могут достигать 15%, в то время как в обычных условиях они не превышают 1,5 мг/сут. (последним при анализе магниевого гомеостаза пренебрегают).
Таблица 1. Клинические проявления дефицита магния
Mg ++ как фармакологическое средство обладает множеством разнообразных клинических эффектов, в частности гипотензивным. антиишесическим, диуретическим и др., а также обилием показаний. В большинстве случаев фармакологическое действие Mg ++ проявляется и при отсутствии явных признаков его дефицита. Возможно, это объясняется тем, что при многих патологических процессах развивается вторичный (общий или местный) магниевый дефицит, выступающий одним из патогенетических механизмов, способствуя прогрессированию заболевания и усугублению клинического состояния больного. Получение фармакологических эффектов Mg ++ во многих случаях с недоказанным его дефицитом можно связать и с антикальциевым действием.
Магниевая соль оротовой кислоты выпускается под названием «магнерот» в таблетках по 500 мг (32,8 мг элементарного магния). К настоящему времени накоплен значительный клинический материал об эффективности этого препарата в различных областях медицины и в первую очередь в кардиологии (табл. 2).
Таблица 2. Клинически подтвержденное действие оротата магния (Schmidt, 1998)
Таким образом, магниевая терапия в кардиологии сегодня имеет надежную теоретическую основу и убедительное практическое подтверждение.
Роль препаратов магния в ведении пациентов терапевтического профиля
Огромная роль магния (Mg ++ ) в обеспечении самого широкого спектра физиологических процессов в организме человека несомненна [5, 30, 33]. Магний является незаменимым макроэлементом организма и занимает четвертое место после натрия, калия и кальц
Огромная роль магния (Mg ++ ) в обеспечении самого широкого спектра физиологических процессов в организме человека несомненна [5, 30, 33]. Магний является незаменимым макроэлементом организма и занимает четвертое место после натрия, калия и кальция по своей распространенности в организме человека. Однако до настоящего времени определение его уровня в плазме крови не стало нормой в условиях реальной клинической практики, так как считается, что он только косвенно и очень приблизительно отражает его содержание внутри клетки.
Роль магния для организма человека
В норме за сутки в организм должно поступать около 300 мг магния для женщин и 350 мг — для мужчин. Общее количество магния у человека составляет около 24 г, причем около 40% находится внутри клеток. Наибольшее количество магния находится в костной (около 60%) и мышечной (около 20%) тканях. Около 40% от общего количества содержится в клетках сердца, головного мозга, почек, 20–30% от этого количества может быть достаточно быстро мобилизовано в условиях его повышенного потребления. Около 60% сывороточного магния находится в ионизированном виде, остальная часть связана с протеинами, фосфатами, цитратами. В плазме крови и эритроцитах находится менее 1% от общего количества магния. На сердце приходится около 20% всего магния, содержащегося в организме человека, что говорит о его большом значении для нормальной сердечной деятельности.
Потребность в магнии существенно возрастает при физических нагрузках, стрессе, в условиях жаркого климата, в период беременности и лактации, при посещении бани, злоупотреблении алкоголем, несбалансированных ограничительных диетах и синдроме хронической усталости [5, 17]. В этих ситуациях потребность повышается в среднем на 150 мг в сутки. Основными источниками поступления магния в организм являются бобовые и злаковые, шпинат, салаты, руккола, брокколи, ревень. Особенно богаты магнием орехи и шоколад, но существенное увеличение потребления данных продуктов может привести к прибавке в весе в связи с их высокой калорийностью. Кроме этого, необходимо помнить, что усваивается не более 30–40% магния, поступающего с пищей. При этом для его хорошей усвояемости также требуется поступление в организм в достаточном количестве кофакторов: молочной, аспарагиновой, оротовой кислот и, что особенно важно, витамина В6 [33]. В развитии алиментарного дефицита магния важную роль играют такие факторы, как его низкое содержание в пище, воде, а также избыточное потребления кальция, натрия, белка или жира с пищей, что существенно снижает поступление магния в организм из-за образования его невсасывающихся комплексов. Частота гипомагниемии у людей достаточна высокая и составляет от 10 до 40% [5, 19]. Для обозначения нарушений обмена магния используют два термина. Под «магниевым дефицитом» понимают снижение общего содержания магния в организме. Под «гипомагниемией» подразумевают снижение концентрации магния в сыворотке (в норме 0,8–1,2 ммоль/л). Умеренной недостаточности магния в организме соответствует его уровень в сыворотке крови 0,5–0,7 ммоль/л, выраженной (угрожающей жизни) — ниже 0,5 ммоль/л. Также выделяют первичный (генетически обусловленный) и вторичный (алиментарный, физиологический и т. д.) дефицит магния.
Частота выявления гипомагниемии зависит от особенностей исследуемой популяции, критериев диагностики и использованных методов диагностики. Обнаружение нормальных показателей магния в сыворотке крови не исключает его общего дефицита и гипокалиегистии, так как при возникновении дефицита магния он может высвобождаться из костей, предотвращая снижение его сывороточной концентрации. Поэтому клиническая ценность определения концентрации Mg ++ в сыворотке крови, в том числе и в ее форменных элементах, имеет клиническое значение только при наличии гипомагниемии.
Гомеостаз Mg ++ также очень сильно зависит от возраста (пожилые люди склонны к гипокалиемии, а у молодых среднесуточная потребность на 150 мг больше) и состояния кишечной абсорбции (например, уровень магния резко снижен при синдроме мальабсорбции и диарее) [33], которая в основном происходит в двенадцатиперстной кишке и проксимальном отделе тощей кишки. Снижают всасывание магния железо, кальций, фосфор, щавелевая кислота, фитаты и танин, содержащиеся в крепко заваренном чае. До 30% магния, получаемого с пищей, выводится через почки. Экскреция магния значительно возрастает при повышении уровня катехоламинов и глюкокортикостероидов. В условиях дефицита магния его выведение через почки существенно снижается. Также существенные потери магния могут иметь место при усиленном потоотделении. Основные причины дефицита магния представлены в табл. 1.
В настоящее время магний считается одним из основных регуляторов обменных процессов и его физиологические эффекты в организме человека хорошо изучены. Магний оказывает влияние на:
Известно, что магний является естественным антагонистом кальция, что обусловливает наличие у него миотропного, спазмолитического и дезагрегационного эффектов и участие в обеспечении нормальных электрофизиологических процессов клеток за счет влияния на трансмембранный потенциал [1].
В последнее время установлена важная роль магния в развитии эндотелиальной дисфункции. Было показано, что назначение препаратов магния способно через 6 мес существенно улучшить (почти в 3,5 раза больше по сравнению с плацебо) эндотелийзависимую дилятацию плечевой артерии. При этом также была выявлена прямая линейная корреляция — зависимость между степенью эндотелийзависимой вазодилятации и концентрацией внутриклеточного магния [22]. Одним из возможных механизмов, объясняющих благоприятное влияние магния на эндотелиальную функцию, может быть его антиатерогенный потенциал.
Дефицит магния может проявляться самой различной симптоматикой:
Также дефицит магния негативно сказывается на течении беременности, провоцируя преждевременные роды и повышая сократимость матки.
Состояние обмена магния при патологических состояниях
Артериальная гипертензия. Считается, что ионы магния подавляют активность ренин-ангиотензин-альдостероновой системы, поэтому на фоне гипомагниемии часто имеет место выраженная вазоконстрикция [2, 7, 16, 22].
Экспериментальные данные указывают на важную роль ионов магния в регуляции сосудистого тонуса. При снижении уровня внеклеточного магния увеличивается поступление кальция внутрь клетки, что вызывает вазоконстрикцию. При парентеральном введении магния наблюдается выраженная вазодилятация, сопоставимая с эффектом антагонистов кальция. Коррекция поступления в организм магния с помощью пищевых добавок позволяет добиться нормализации уровня АД при мягкой артериальной гипертонии у пожилых [9], в том числе и в условиях двойного слепого плацебо-контролируемого исследования [26].
В настоящее время явно недостаточно клинических данных для окончательного вывода о возможности использования магния с гипотензивной целью. У больных артериальной гипертензией, особенно при наличии гипертонической энцефалопатии, длительный прием магния в суточной дозе 15 ммоль сопровождался снижением АД в среднем на 12/8 мм рт. ст. В 29 ретроспективных исследованиях была выявлена связь между уровнем АД и потреблением магния. В то же время данные клинических исследований не подтвердили факт снижения АД при увеличении потребления магния. Только в одном из них, выполненном в Японии, увеличение потребления магния до 20 ммоль в день через 8 недель сопровождалось снижением АД на 2,5 мм рт. ст. и 3,7 мм рт. ст. по результатам суточного мониторирования артериального давления (СМАД).
Вместе с тем дополнительный прием магния можно рекомендовать больным с артериальной гипертензией, у которых имеется высокий риск гипомагниемии (например, при терапии тиазидными диуретиками [32]).
Ишемическая болезнь сердца (ИБС). По данным эпидемиологических исследований дефицит магния в питьевой воде повышает риск развития сердечно-сосудистых заболеваний (особенно ИБС) и внезапной смерти. Известно, что миокард больных, умерших от сердечно-сосудистой патологии, содержит почти в 2 раза меньше магния, чем у пациентов, скончавшихся от других причин.
Показано, что дефицит магния ассоциируется с повышением уровня атерогенных липидов [14, 20, 32]. Более того, по данным исследования ARIC (The Atherosclerosis Risk in Communities), частота развития ИБС выше у тех лиц, у которых выявляется более низкий уровень магния в крови. Причем эта закономерность сохраняется после стандартизации пациентов по их демографическим характеристикам, уровню холестерина, фибриногена и других факторов риска.
В Финляндии в результате реализации правительственной программы по профилактике магниевого дефицита у населения страны в течение последних 15 лет удалось снизить частоту инфарктов миокарда в популяции почти в 2 раза.
Анализ обобщенных данных 7 рандомизированных исследований у 1301 больного острым инфарктом миокарда выявил благоприятное влияние магния на больничную летальность [4, 8, 21, 24].
В многоцентровом исследовании LIMIT–II (Second Leicester Intravenous Magnesium Intervention Trial) (2316 пациентов) было выявлено снижение риска смерти на 24%, риска развития сердечной недостаточности на 25% (в группе больных острым инфарктом миокарда, которые в течение первых 28 дней получали дополнительно к стандартной терапии инфузии сульфата магния). Однако в более позднем исследовании (58 050 пациентов) при лечении сульфатом магния и изосорбидом мононитрата в сравнении с каптоприлом не было выявлено снижения летальности в группе больных, получавших магний, хотя на фоне терапии препаратами магния, несмотря на отсутствие снижения летальности у больных с гипомагниемией, существенно реже встречались аритмии, судороги в мышцах, чувство тревоги и другие проявления его дефицита.
Хроническая сердечная недостаточность. Дефицит магния был обнаружен при сердечной недостаточности, развившейся на фоне артериальной гипертензии и ИБС [25]. Причем тяжесть хронической сердечной недостаточности прямо коррелировала со степенью дефицита магния: это связывают с тем, что на фоне гипомагниемии существенно уменьшается диурез [12]. Кроме этого показано, что на фоне дефицита магния гораздо чаще развиваются нарушения ритма и проводимости при терапии сердечными гликозидами [29].
Нарушения сердечного ритма. Исследование Framinghem Heart Study продемонстрировало, что длительная гипомагниемия коррелирует с высокой частотой возникновения желудочковых экстрасистол, тахикардии, фибрилляции желудочков. В исследовании PROMISE Study была выявлена большая частота желудочковой экстрасистолии и высокая летальность в группе пациентов с гипомагниемией в сравнении с группами, в которых отмечалась нормо- и гипермагниемия.
Препараты магния давно используются как антиаритмические средства, сочетающие свойства антиаритмиков I (мембраностабилизирующие) и IV классов (антагонисты кальция). Магний предотвращает потерю калия клеткой и уменьшает вариабельность длительности интервала QT, которая является прогностически неблагоприятным фактором развития фатальных аритмий. Кроме того, магний способен ингибировать симпатические влияния на сердце [23, 33].
В качестве антиаритмика соли магния наиболее эффективны (препарат выбора) при пируэт-желудочковой аритмии (torsades de pointes), благодаря способности угнетать развитие следовых деполяризаций и укорачивать длительность интервала QT [11, 35]. Магний также используется как при врожденном синдроме удлиненного интервала QT, так и при его удлинении вследствие применения антиаритмиков I класса.
Препараты магния широко используются при лечении аритмий на фоне дигиталисной интоксикации благодаря способности восстанавливать функцию калий-натриевой помпы [8].
Результаты рандомизированного многоцентрового плацебо-контролируемого двойного слепого исследования MAGICA позволили рассматривать препараты магния и калия как общепринятый европейский стандарт при лечении аритмий у пациентов на фоне приема сердечных гликозидов, диуретиков, антиаритмиков. Антиаритмический эффект препаратов магния проявляется спустя 3 недели от начала лечения и позволяет снизить число желудочковых экстрасистол на 12% и общее число экстрасистол на 60–70%.
Пролапс митрального клапана. По данным эпидемиологических исследований у пациентов с пролапсом митрального клапана дефицит магния выявляется почти в 2/3 случаев [6, 13]. Прием препаратов магния данной категорией пациентов позволяет уменьшить проявления вегетативного дисбаланса: уменьшить симпатические влияния вегетативной нервной системы и усилить парасимпатическую активность. При этом наблюдается увеличение интервалов RMSSD днем и снижение в ночные часы.
Сахарный диабет. Гипомагниемия часто встречается при сахарном диабете 2-го типа [15]. Также считается, что дефицит магния повышает риск развития нарушения толерантности к глюкозе [4], так как ионы магния улучшают инсулинозависимую утилизацию глюкозы.
Алкогольная интоксикация. При злоупотреблении алкоголем дефицит магния играет важную роль в развитии психосоматического симптомокомплекса, миопатий, нейропатий, аритмий и абстинентного синдрома и аритмий [17].
Предменструальный синдром. Рассматривается как вариант стресса, сопровождающийся дефицитом магния и склонностью к спазму гладких мышц.
Таким образом, препараты магния играют важную роль в ведении пациентов с сердечно-сосудистой патологией прежде всего благодаря их способности благоприятно влиять на имеющиеся факторы риска и снижать риск сердечно-сосудистых заболеваний на уровне популяции.
В настоящее время существует несколько препаратов, содержащих магний для заместительной терапии (табл. 2). Выбор препаратов магния для коррекции его дефицита лежит между неорганическими и органическими солями магния. Первое поколение магнийсодержащих препаратов в своем составе имело неорганические соли, из которых магния усваивалось не более 5%. Кроме того, пациенты их плохо переносили из-за частого развития диареи, так как магний стимулирует перистальтику кишечника. Второе поколение магнийсодержащих препаратов значительно лучше усваивается и не провоцирует развитие диспепсии и диареи.
Поливитаминные комплексы с минералами не могут рассматриваться как источник магния для заместительной терапии, так как обычно содержат несколько микроэлементов, мешающих усвоению друг друга (например, всасывание магния снижается в присутствии кальция), поэтому эффективность поливитаминов с минералами значительно ниже, чем у специальных препаратов, содержащих магний.
При дефиците магния требуется его дополнительное введение из расчета 10–30 мг на килограмм массы тела в сутки на протяжении не менее 2 месяцев, что обусловлено медленным насыщением тканевых депо. Естественно, что обеспечить такое повышенное поступление магния только за счет изменения пищевого рациона нереально.
Одним из наиболее эффективных препаратов является Магнерот, который помимо магния содержит оротовую кислоту, которая способствует росту клеток, участвует в процессе обмена веществ. Поэтому Магнерот считается препаратом выбора в комплексном лечении и профилактике инфаркта миокарда, хронической сердечной недостаточности, аритмий сердца, вызванных дефицитом магния, спастических состояний, атеросклероза, гиперлипидемий. Противотревожное действие Магнерота существенно расширяет спектр его клинического применения. Имеющаяся клиническая доказательная база позволяет комбинировать его с антидепрессантами, противосудорожными и снотворными средствами при комплексной терапии депрессий, судорожных состояний и инсомнических расстройств.
Литература
С. В. Недогода, доктор медицинских наук, профессор
ВолГМУ, Волгоград