код по мкб 10 саркома юинга
Саркома Юинга
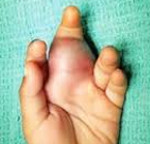
Саркома Юинга – это злокачественное новообразование, развивающееся из костной ткани. Чаще возникает в подростковом или юношеском возрасте. Поражает плоские и длинные трубчатые кости. Является одной из наиболее агрессивных опухолей, склонна к раннему метастазированию. Проявляется болью, затем – отеком, местной гиперемией и гипертермией, а также локальным расширением венозной сети. На поздних стадиях определяется опухоль, нередко возникает патологический перелом пораженной кости. Лечение комбинированное, включает в себя операцию (при возможности – радикальное удаление новообразования) в сочетании с лучевой терапией, а также пред- и послеоперационной химиотерапией.
МКБ-10
Общие сведения
Саркома Юинга – злокачественная опухоль костей, характеризующаяся быстрым ростом и ранним появлением метастазов. Обычно развивается у детей, подростков и лиц молодого возраста. Сопровождается болями и местными изменениями мягких тканей (отек, гиперемия, гипертермия). На поздних стадиях опухоль становится заметна при осмотре и пальпации. Лечение осуществляется врачом-онкологом, включает в себя оперативное удаление новообразования, химио- и лучевую терапию.
Саркома Юинга – вторая по частоте злокачественная опухоль костной ткани, возникающая в детском возрасте, составляет от 10 до 15% от общего числа злокачественных новообразований костей. У взрослых старше 30 и детей младше 5 лет встречается редко. Наибольшее количество случаев заболевания приходится на возраст от 10 до 15 лет. Мальчики болеют чаще девочек, европеоиды – чаще представителей негроидной и монголоидной расы.
В отдельных случаях первичное новообразование при этом заболевании возникает в мягких тканях, а не в костях. Такая форма заболевания называется экстраоссальной (внекостной) саркомой Юинга. Кроме того, существуют сходные по характеру и структуре агрессивные злокачественные опухоли, относящиеся к группе так называемых опухолей семейства саркомы Юинга. В эту группу, кроме внекостной и костной саркомы относят ПНЭО (периферические примитивные нейроэктодермальные опухоли). Внекостные формы и ПНЭО в сумме составляют около 15% от всего числа случаев саркомы Юинга.
Причины
Причины развития саркомы Юинга в настоящее время точно не установлены. Однако ряд исследователей в сфере современной онкологии считает, что определенную роль в возникновении этого заболевания играет наследственная предрасположенность. Примерно в 40% случаев выявляется связь с предшествующей травмой. Существуют данные, свидетельствующие о повышении вероятности развития болезни у пациентов с некоторыми разновидностями скелетных аномалий (аневризмальной костной кистой, энхондромой и др.), а также нарушениями внутриутробного развития мочеполовой системы (редупликацией почечной системы, гипоспадиями). Какой-либо связи с воздействием ионизирующей радиации не установлено.
Патанатомия
Чаще всего саркома Юинга выявляется в бедренной кости, костях таза, большеберцовой и малоберцовой кости, лопатке, ребрах, плечевой кости и позвонках. При возникновении в длинных трубчатых костях опухоль обычно локализуется в области диафиза, а затем по мере роста распространяется в сторону эпифизов. Более чем в 90% случаев отмечается интрамедуллярное расположение новообразования и тенденция к распространению опухолевых клеток по костномозговому каналу.
Саркома Юинга наиболее часто метастазирует в легкие. На втором месте по распространенности – метастазы в костный мозг и костную ткань. На поздних стадиях практически у всех больных определяются метастазы в центральную нервную систему. В редких случаях выявляются отдаленные метастазы в плевру, лимфатические узлы средостения, внутренние органы и забрюшинное пространство. Из-за раннего метастазирования к моменту постановки диагноза от 15 до 50% пациентов уже имеют метастазы, которые можно выявить при помощи рутинных исследований. У подавляющего количества больных есть микрометастазы.
Симптомы саркомы Юинга
Первым, самым ранним признаком заболевания становится боль в области поражения. Вначале она слабая или умеренная, самопроизвольно ослабевает или исчезает, а затем появляется снова. В отличие от болей при воспалительных процессах такая боль не ослабевает в покое, по ночам или при фиксации конечности. Напротив, для саркомы Юинга характерно усиление болей в ночное время.
По мере прогрессирования боли становятся более интенсивными, лишают сна и ограничивают повседневную активность. В близлежащем суставе развивается болевая контрактура. Пальпация области поражения болезненна. Температура кожи над ней повышена. Отмечается пастозность мягких тканей, местная гиперемия и расширение подкожных вен. Опухоль быстро увеличивается и (обычно спустя несколько месяцев после возникновения первых симптомов) становится настолько крупной, что ее можно прощупать. На поздних стадиях в области новообразования нередко возникает патологический перелом.
Местные клинические признаки сочетаются с нарастающими симптомами общей опухолевой интоксикации. Больные предъявляют жалобы на слабость и потерю аппетита. Отмечается снижение веса вплоть до истощения. Температура тела повышена до субфебрильных или даже фебрильных цифр. Определяется регионарный лимфаденит. По анализам крови выявляется анемия.
Некоторые симптомы зависят от локализации новообразования. Так, при возникновении саркомы Юинга на костях нижних конечностей появляется хромота. При поражении позвонков возможно развитие компрессионно-ишемической миелопатии с нарушением функции тазовых органов и явлениями параплегии. При новообразованиях в области костей грудной клетки может возникнуть дыхательная недостаточность, плевральный выпот и кровохарканье.
Диагностика
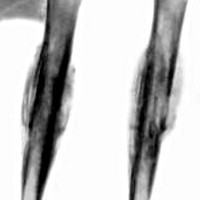
Как правило, на начальном этапе пациенты обращаются к врачам-травматологам. И первым исследованием, позволяющим заподозрить саркому Юинга, становится рентгенография пораженной кости. Для данного патологического процесса характерно сочетание реактивного и деструктивного процессов костеобразования. Контуры кортикального слоя нечеткие, определяется расслоение и разволокнение кортикальной пластинки.
При вовлечении в процесс надкостницы на рентгенограмме выявляются мелкие пластинчатые или игольчатые образования. Кроме того, на снимках видна область изменения мягких тканей, по своему размеру превышающая первичную костную опухоль. При этом мягкотканный опухолевый компонент отличается однородностью, хрящевые включение, очаги обызвествления или патологического костеобразования отсутствуют.
При выявлении типичных рентгенологических признаков саркомы Юинга больного направляют в отделение онкологии, где проводится расширенное обследование для оценки состояния первичного очага и выявления метастазов. В ходе такого обследования выполняется компьютерная томография или магнитно-резонансная томография костей и мягких тканей, пораженных злокачественным процессом. Данные исследования позволяют точно определить размер новообразования, степень его распространения по костно-мозговому каналу, связь с сосудисто-нервным пучком и окружающими тканями.
Для выявления метастазов в легочную ткань применяется компьютерная томография и рентгенография легких. Для обнаружения метастазов в костях, костном мозге и внутренних органах – позитронно-эмиссионная томография, УЗИ и остеосцинтиграфия. Кроме того, выполняется ряд исследований для точной оценки характера новообразования.
Производится биопсия, при этом материал берут из участка костной ткани рядом с костномозговым каналом, либо, если это невозможно – из мягкотканого компонента опухоли. Поскольку для саркомы Юинга характерно местное и отдаленное поражение костного мозга, выполняется билатеральная трепанобиопсия, в ходе которой производится забор костного мозга из крыльев подвздошной кости. Для оценки характера процесса также может проводиться иммуногистохимическое исследование и молекулярно-генетические исследования (флуоресцентная гибридизация – для подтверждения диагноза, полимеразная цепная реакция – для выявления микрометастазов).
Лечение саркомы Юинга
Поскольку данная опухоль относится к категории высокоагрессивных неоплазий, рано дающих метастазы, ее лечение должно включать в себя воздействие на весь организм, а не только на первичный очаг, даже в тех случаях, когда метастазы не были обнаружены. Дело в том, что существует очень высокая вероятность раннего появления микрометастазов, которые на момент постановки диагноза невозможно выявить при помощи существующих методов. Лечение саркомы Юинга комбинированное, включает в себя как консервативную терапию, так и хирургические вмешательства и состоит из следующих компонентов:
В прошлом при саркоме Юинга обычно проводились калечащие операции – ампутации и экзартикуляции. Современные техники позволяют выполнять органосохраняющие оперативные вмешательства не только на мелких (малоберцовой, лучевой, локтевой, лопатке, ключице и ребрах), но и на крупных костях (плечевой, бедренной и даже костях таза). При метастазировании в костный мозг и кости назначается интенсивная терапия, включающая в себя тотальное облучение всего тела, химиотерапию с использованием мегадоз препаратов и трансплантацию периферических стволовых клеток или костного мозга.
Прогноз и профилактика
Своевременное комбинированное лечение обеспечивает 70% общую выживаемость пациентов с локализованной саркомой Юинга. При наличии метастазов в кости и костный мозг прогноз существенно ухудшается, однако сочетание высокодозной химиотерапии, тотальной лучевой терапии и трансплантации костного мозга дает возможность повысить выживаемость больных с метастатической формой заболевания с 10% до 30% и более.
Все пациенты после излечения должны проходить регулярное обследование для раннего выявления рецидивов и контроля над побочными эффектами. Следует учитывать, что ряд побочных эффектов может возникать не только при прохождении курса лечения, но и спустя длительное время после его окончания. К числу таких эффектов относится мужское и женское бесплодие, кардиомиопатия, нарушение роста костей и увеличение вероятности развития вторичных злокачественных новообразований. Однако многие пациенты, прошедшие лечение по поводу саркомы Юинга могут жить полноценной жизнью. Профилактика не разработана.
Саркомы мягких тканей
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «14» марта 2019 года
Протокол №58
Название протокола: Саркомы мягких тканей
Код (ы) МКБ 10:
С 47.0 Злокачественное новообразование периферических нервов и вегетативной нервной системы головы, лица и шеи
С 47.1 Злокачественное новообразование периферических нервов и вегетативной нервной системы верхних конечностей
С 47.2 Злокачественное новообразование периферических нервов и вегетативной нервной системы нижних конечностей
С 47.3 Злокачественное новообразование периферических нервов и вегетативной нервной системы груди
С 47.4 Злокачественное новообразование периферических нервов и вегетативной нервной системы живота
С 47.5 Злокачественное новообразование периферических нервов и вегетативной нервной системы таза
С 47.6 Злокачественное новообразование периферических нервов и вегетативной нервной системы туловища
С 47.8 Комбинированное злокачественное новообразование периферических нервов и вегетативной нервной системы
С 47.9 Злокачественное новообразование периферических нервов и вегетативной нервной системы БДУ
С 48.0 Забрюшинное пространство
С 48.1 Особые отделы брюшины
С 48.2 Брюшина, БДУ
С 48.8 Комбинированное поражение забрюшинного пространства
С 49 Злокачественной новообразование других типов соединительной и мягких тканей
С 49.0 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани головы и шеи
С 49.1 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани верхних конечностей
С 49.2 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани нижних конечностей
С 49.3 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани груди
С 49.4 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани живота
С 49.5 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани таза
С 49.6 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани туловища
С 49.8 Комбинированное поражение соединительной ткани, подкожной жировой клетчатка и иных мягких тканей
С 49.9 Соединительная ткань, подкожная жировая клетчатка, а также иные мягкие ткани, БДУ
Дата разработки/пересмотра протокола: 2015 г./2018 г.
Пользователи протокола: онкологи, хирурги, врачи общей практики, терапевты.
Категория пациентов: взрослые.
Оценка на степень доказательности приводимых рекомендаций
Таблица 1. Шкала уровней доказательности
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Анатомическая классификация:
1. Соединительная ткань, подкожная и другие мягкие ткани (С49), периферические нервы (С47)
2. Забрюшинное пространство (С48.0)
3. Средостение: переднее (С38.1); заднее (С38.2); средостение, БДУ (С38.3).
Таблица 2. Международная классификация по системе TNM (VIII–й пересмотр, 2017 г. [2].
Первичная опухоль
Тх первичная опухоль не может быть оценена
| Пораженный орган | Обозначение | Пораженный орган | Обозначение |
| Легкие | PUL | Костный мозг | MAR |
| Кости | OSS | Плевра | PLE |
| Печень | HEP | Брюшина | PER |
| Мозг | BRA | Надпочечники | ADR |
| Лимфоузлы | LUM | Кожа | SKI |
| Другие | OTN |
| Стадия IA | T1 | N0 | M0 | G1, GX Low Grade |
| Стадия IB | T2, T3, T4 | N0 | M0 | G1, GX Low Grade |
| Стадия II | T1 | N0 | M0 | G2, G3 High Grade |
| Стадия IIIA | T2 | N0 | M0 | G2, G3 High Grade |
| Стадия IIIB | T3, T4 | N0 | M0 | G2, G3 High Grade |
| Стадия IIIB | Любой T | N1* | M0 | Любой G |
| Стадия IV | Любой T | Любой N | M1 | Любой G |
* AJCC классифицирует N1 как IV стадия для конечностей и поверхностных опухолей туловища.
R классификация
Отсутствие или наличие остаточной опухоли после лечения описывается символомR:
RX – наличие остаточной опухоли не может быть оценено;
R0 – нет остаточной опухоли;
R1 – микроскопическая остаточная опухоль;
R2 – макроскопическая остаточная опухоль.
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии постановки диагноза
Клинические данные:
Жалобы [9](УД-В) и анамнез [9](УД-В): наличие опухолевого образования мягких тканей, увеличение периферических лимфатических узлов.
Физикальный осмотр [9,В]
Лабораторные исследования:
Изменения в клинических, биохимических анализах при отсутствии сопутствующей патологии не специфичны.
Цитологическое исследование
Гистологическое исследование
Инструментальные исследования
Являются дополнительными методами диагностики для определения распространенности заболевания, и установления стадии заболевания
Показания для консультации узких специалистов
Дифференциальный диагноз
Фиброма – доброкачественная опухоль из соединительной ткани.
Липома – доброкачественная соединительнотканная опухоль; развивается в слое подкожной соединительной рыхлой ткани.
Рабдомиома – доброкачественная опухоль из мышечной ткани
Шваннома – доброкачественная опухоль из периферических нервов
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Апрепитант (Aprepitant) |
| Винбластин (Vinblastine) |
| Винкристин (Vincristine) |
| Винорелбин (Vinorelbine) |
| Гемцитабин (Gemcitabine) |
| Гранисетрон (Granisetron) |
| Дакарбазин (Dacarbazine) |
| Дарбэпоэтин альфа (Darbepoetin alfa) |
| Дексаметазон (Dexamethasone) |
| Доксорубицин (Doxorubicin) |
| Доцетаксел (Docetaxel) |
| Железа (III) гидроксид декстран (Ferric (III) hydroxide destrane) |
| Железа (III) гидроксид сахарозный комплекс (Ferric (III) hydroxide sacharose complex) |
| Железа карбоксимальтозат (Ferric carboxymaltosate) |
| Иматиниб (Imatinib) |
| Ифосфамид (Ifosfamide) |
| Месна (Mesna) |
| Метоклопрамид (Metoclopramide) |
| Метотрексат (Methotrexate) |
| Нетупитант (Netupitant) |
| Оланзапин (Olanzapine) |
| Оларатумаб (Olaratumab) |
| Ондансетрон (Ondansetron) |
| Пазопаниб (Pazopanib) |
| Палоносетрон (Palonosetron) |
| Ролапитант (rolapitant) |
| Сорафениб (Sorafenib) |
| Сулиндак (Sulindac) |
| Тамоксифен (Tamoxifen) |
| Торемифен (Toremifene) |
| Трабектедин (Trabectedin) |
| Трописетрон (Tropisetron) |
| Филграстим (Filgrastim) |
| Фолиевая кислота (Folic acid) |
| Фосапрепитант (Fosaprepitant) |
| Цианокобаламин (Cyanocobalamin) |
| Циклофосфамид (Cyclophosphamide) |
| Эпоэтин альфа (Epoetin alfa) |
| Эпоэтин бета (Epoetin Beta) |
| Эпоэтин тета (Epoetin theta) |
| Эрибулин (Eribulin) |
| Этопозид (Etoposide) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Медикаментозное лечение, оказываемое на амбулаторном уровне:
— нет специфических препаратов для лечения сарком мягких тканей на амбулаторном уровне (возможно применение таргетной терапии препаратами пазопаниб, сорафениб и иматиниб по строгому назначению онколога).
Профилактические мероприятия:
Профилактические мероприятия
Первичная профилактика:
Вторичная профилактика:
Третичная профилактика:
Применение лекарственных препаратов позволяющих восстановить иммунную систему после противоопухолевого лечения (антиоксиданты, поливитаминные комплексы), полноценные режим питания богатый витаминами, белками, отказ от вредных привычек (курение, употребление алкоголя), профилактика вирусных инфекций и сопутствующих заболеваний, регулярные профилактические осмотры у онколога, регулярные диагностические процедуры (рентгенография легких, УЗИ печени, почек, лимфоузлов шеи)
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ:
Цель лечения: удаление опухоли мягких тканей и регионарных метастатически пораженных лимфоузлов (при их наличии)
Тактика лечения
Критерии эффективности лечения:
Полный эффект – исчезновение всех очагов поражения на срок не менее 4х недель.
Частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов.
Стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения.
Прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения
Общие принципы лечения
Основные методы лечения сарком мягких тканей – хирургический, лекарственный, лучевая терапия. Хирургический метод в качестве самостоятельного вида используется при лечении первичных low grade (T1) опухолей при условии возможности выполнения радикального хирургического вмешательства. В остальных случаях лечение комбинированное или комплексное, ведущим и решающим компонентом которого является хирургическое удаление опухоли. Лечебная программа строится с учетом гистологической степени злокачественности, распространения процесса, размеров и локализации опухоли.
Лучевая терапия:
Виды лучевой терапии:
6. VAI
Винкристин 2мг в/в 1й день
Доксорубицин 75 мг/м2 в/в в течение 72 часовая инфузия 1дн
Ифосфамид 2,5г/м2г в/в 3 часовая инфузия 1-4-й дн
Месна 500мг/м2 в 1-й день вместе с ифосфамидом, далее 1500мг/м2 в/в 24-часовая инфузия в течение 4 дней
Филграстим 300мкг п/к 5-15дн или до восстановления уровня нейтрофилов.
Интервал 3 недели
7. Vadriac
Винкристин 1.5мг/м2 в/в 1,8,15й день в течение первых 2х курсов, далее только в 1й день
Циклофосфан 600 мг/м2 в/в 1,2 дни
Доксорубицин 60 мг/м2 в/в 48часовая инфузия
Интервал 3 недели
и далее
Ифосфамид 1800мг/м2 в/в 1-5й дни, месна 1-5й дни
Этопозид 100мг/м2 в/в 1-5й дни.
Интервал 3 недели.
Таргетная терапия:
Пазопаниб 800 мг 1р/день внутрь длительно (до прогрессирования). Пациентам с саркомами мягких тканей (кроме липосарком и GIST) при прогрессировании в течение 12 месяцев после начала неоадъювантной или адъювантной терапии, или предварительно получавших стандартную химиотерапию по поводу метастатической саркомы мягких тканей [1, В], [12].
Оларатумаб* 15мг/кг веса в/в 1,8-дни 21-дневного цикла.
* при регистрации препарата в Республике Казахстан
Лекарственной терапия опухолей мягких тканей десмоидного типа (агрессивный фиброматоз):
Сулиндак или другие НПВС
Тамоксифен ± сулиндак
Торемифен
Метотрексат + винбластин
Низкие дозы интерферона (3-6 млн МЕ)
Доксорубицин
Иматиниб
Сорафениб
Метотрексат + винорельбин
Липосомальный доксорубицин
Перед назначением лекарственной терапии все пациенты должны быть обсуждены мультидисциплинарой группой специалистов. Антрациклиновые схемы рекомендованы в неоадъювантных и адъювантных режимах [13].
| Химио/таргетные препараты | |
| Ифосфамид | 500, 1000, 2000мг |
| Дакарбазин | 200, 500мг |
| Этопозид | 100 мг |
| Винкристин | 2мг |
| Доксолек | 10, 25, 50 мг |
| Гемцитабин | 200, 1000мг |
| Таксотер | 20, 40, 80мг |
| Трабектидин | 1мг |
| Пазопаниб | 200, 400мг |
| Оларатумаб | 190, 500мг |
| Эрибцлин | 1мг |
Хирургическое вмешательство
Принципы оперативных вмешательств:
Основные типы операций при саркомах мягких тканей
Простое иссечение используется исключительно в качестве этапа морфологической диагностики злокачественных опухолей.
Широкое иссечение. При этой операции опухоль удаляют в пределах анатомической зоны, в едином блоке с псевдокапсулой и отступя от видимого края опухоли на 4–6 см и более. Широкая местная резекция применяется при опухолях низкой степени злокачественности, поверхностных, располагающихся выше поверхностной фасции, в коже, подкожной клетчатке (небольшие фибросаркомы, липосаркомы, десмоиды, дерматофибросаркомы). Эту операцию не выполняют при саркомах высокой степени злокачественности.
Радикальная операция. Эта операция предпринимается при глубоко располагающихся саркомах высокой степени злокачественности. Она предусматривает удаление опухоли и окружающих ее нормальных тканей с включением в единый блок фасций и неизмененных окружающих мышц, которые удаляются полностью с отсечением у места прикрепления. При необходимости производят резекцию сосудов, нервов, костей, прибегая одномоментно к соответствующим реконструктивным пластическим операциям на сосудах, нервах, костях, суставах. Органосохраняющие и функционально-щадящие хирургические вмешательства при местно-распространенных злокачественных опухолях мягких тканей конечностей выполняются исключительно в рамках комбинированного и комплексного лечения. Контроль радикальности оперативного вмешательства осуществляют путем срочного интраоперационного гистологического исследования краев отсечения опухоли от нормальных тканей.
Ампутации и экзартикуляции. Ампутация и экзартикуляция конечности показаны в случаях, когда выполнение радикальной сберегающей операции не представляется возможным из-за массивного поражения (вовлечение в опухолевый процесс суставов, костей, магистральных сосудов и нервов на большом протяжении) и/или при неэффективности курсов неоадъювантного лечения.
Дальнейшее ведение
Диспансерное наблюдение за излеченными больными:
в течение первого года после завершения лечения – 1 раз каждые 3 месяца;
в течение второго года после завершения лечения – 1 раз каждые 6 месяцев;
с третьего года после завершения лечения – 1 раз в год в течение 3 лет.
ИНДИКАТОРЫ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
Показания для экстренной госпитализации:
Информация
Источники и литература
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Приложение 1
СОПРОВОДИТЕЛЬНАЯ ТЕРАПИЯ
Антиэметическая терапия
Тошнота и рвота являются одним из наиболее частых побочных эффектов химио- терапии (ХТ) и существенно ухудшают качество жизни больных.
Тошнота и рвота, сопутствующие химиотерапии, относятся к числу наиболее неприятных аспектов этого вида лечения (1,2). Не будучи самым серьезным побочным эффектом химиотерапии, рвота, тем не менее, сильно ухудшает качество жизни и снижает ощущение благополучия (1,3). В некоторых случаях пациенты откладывают или полностью прекращают химиотерапию из-за непереносимой тошноты и рвоты (1).
Кроме того, рвота, как таковая, может представлять угрозу здоровью, поскольку неконтролируемая рвота приводит к обезвоживанию, нарушению баланса метаболитов и к анорексии (4,5).
Факторы, связанные с терапией:
Высокая эметогенная способность некоторых препаратов,
Комбинированная терапия
Режим и способ введения препаратов
Высокие дозы химиотерапевтических препаратов (6).
Под уровнем эметогенности понимается риск развития рвоты у больных, получающих тот или иной цитостатик в монорежиме без противорвотной терапии. Например, высокий уровень эметогенности означает, что после введения препарата рвота будет развиваться более чем у 90 % больных. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO представлена в табл. 1.
Таблица 1. Классификация противоопухолевых препаратов в зависимости от уровня эметогенности по рекомендациям MASCC / ESMO.
ТИПЫ ТОШНОТЫ И РВОТЫ
По срокам и механизму развития выделяют 3 основных типа тошноты и рвоты, вызванной цитостатиками: острую, отсроченную и условно-рефлекторную (anticipatory – переводят также как «предшествующую», «преждевременную», «рвоту ожидания»), дополнительно выделяют неконтролируемую (breakthrough – «прорывную») и рефрактерную (7, 8).
Острая рвота развивается в первые 24 ч после химиотерапии, отличается высокой интенсивностью, редко сопровождается тошнотой.
Отсроченная рвота развивается на 2-е–5-е сутки после начала химиотерапии, менее интенсивна, чем острая, и, как правило, сопровождается постоянной тошнотой. Механизмы развития остаются неясными. Ведущая роль отводится субстанции P, серотонин имеет меньшее значение.
Условно-рефлекторная рвота представляет собой классический условный рефлекс на химиотерапию и / или сопутствующие ей манипуляции и окружающую обстановку. Формируется в тех случаях, когда противоопухолевая терапия сопровождается тошнотой и рвотой. Риск ее развития увеличивается пропорционально числу проведенных курсов и может сохраняться в течение длительного времени после окончания химиотерапии. Ведущую роль в формировании условного рефлекса играет многодневная умеренная или тяжелая тошнота. Лучшим методом профилактики условно-рефлекторной тошноты и рвоты является адекватная антиэметическая защита пациента уже с первого курса химиотерапии.
Неконтролируемая (breakthrough – «прорывная») тошнота и рвота развивается на фоне адекватной антиэметической профилактики и требует дополнительной коррекции. Рефрактерная рвота возникает на последующих циклах химиотерапии при неэффективности противорвотной профилактики и / или препаратов резерва на предыдущих курсах лечения.
ПРИНЦИПЫ СОВРЕМЕННОЙ ПРОТИВОРВОТНОЙ ТЕРАПИИ
1. Обязательность проведения, начиная с первого курса химиотерапии.
2. Введение антиэметиков до начала введения первого цитостатика.
3. Применение наиболее эффективных стандартных противорвотных комбинаций.
4. Применение каждого антиэметика, входящего в комбинацию, в адекватных дозах.
5. Соблюдение адекватной продолжительности противорвотной терапии.
6. Соблюдение необходимых для сохранения эффективной концентрации интервалов между приемами антиэметиков.
Критерием эффективности противорвотной терапии является полное отсутствие (полный контроль) рвоты и тошноты в течение 24 часов (период развития острой рвоты) с момента введения противоопухолевых препаратов.
Алгоритм профилактики и терапии тошноты и рвоты
1. Определить эметогенный потенциал назначенного режима ХТ.
2. Назначить профилактическую терапию, исходя из эметогенности режима ХТ.
3. Назначить лечение в случае развития тошноты и рвоты на фоне профилактической терапии.
4. Внести изменения в профилактическую терапию тошноты / рвоты на последующих циклах ХТ.
Антиэметики:
Таблица 2. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Острая тошнота и рвота.
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | 5-НТ3 + DEX + NK 1 |
| Высокий (АС) | 5-НТ3 + DEX + NK 1 |
| Карбоплатин | 5-НТ3 + DEX + NK 1 |
| Умеренный (кроме карбоплатина) | 5-НТ3 + DEX |
| Низкий | 5-НТ3 или DEX или DOP |
| Минимальный | Нет рутинной профилактики |
Таблица 3. Обновленные рекомендации MASCC/ESMO 2016 ТРВХ.
Отсроченная тошнота и рвота.
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | DEX или (если APR 125мг для острой: (МСР+DEX) или (DEX+APR) |
| Высокий (АС) | Нет или (если APR 125мг для острой: APR+DEX) |
| Карбоплатин | Нет или (если APR 125мг для острой: APR) |
| Средний (не карбоплатин) | DEX можно использовать |
| Низкий | Профилактика не предусмотрена |
| Минимальный | Профилактика не предусмотрена |
DEX — дексаметазон
APR — апрепитант
MCP — метоклопромид
Ключевые обновления в рекомендациях по контролю ТРВХ, NCCN 2017:
Карбоплатин категоризируется как высокоэметогенный препарат при введении с площадью под кривой (ППК) ≥4, при введении с ППК
| Группы эметогенного риска | Антиэметики |
| Высокий (не АС) | 5-НТ3 + DEX* + NK 1+Olanzapine* |
| Высокий (АС) | 5-НТ3 + DEX* + NK 1+Olanzapine* |
| Карбоплатин | 5-НТ3 + DEX + NK 1 |
| Умеренный (кроме карбоплатина) | 5-НТ3 + DEX |
| Низкий | 5-НТ3 или DEX или DOP |
| Минимальный | Нет рутинной профилактики |
Таблица 5. Рекомендуемые дозы антогонистов серотониновых рецепторов (5-НТ) для острой тошноты и рвоты.
| Препарат | Путь введения | Доза |
| Ондансетрон | в/в | 8мг или 0,15мг/кг |
| пероральный | 16мг* | |
| Гранисетрон | в/в | 1мг или 0,01мг/кг |
| пероральный | 2мг (или 1мг**) | |
| Трописетрон | в/в | 5мг |
| пероральный | 5мг | |
| Палоносетрон | в/в | 0,25мг |
| пероральный | 0,5мг |
* В рандомизированных исследованиях был протестирован режим 8 мг два раза в день.
** Некоторыми панелистами доза 1 мг более предпочтительна
Таблица 6. Рекомендуемые дозы кортикостероидов (дексаметазон)*
| Дексаметазон | Дозы и Кратность | |
| Высокий риск | Острая рвота | 20мг однократно (12мг когда используется апрепитант или нетупитант) )** |
| Отсроченная рвота | 8мг в течение 3-4 дней (8мг один раз в день когда используется апрепитант или нетупитант ) | |
| Умеренный риск | Острая рвота | 8 мг однократно |
| Отсроченная рвота | 8 мг ежедневно в течение 2-3 дней | |
| Низкий риск | Острая рвота | 4-8 мг один раз в день |
* Несмотря на то, что другие кортикостероиды также являются эффективными антиэметиками, режим дозирования для дексаметазона, как препарата выбора, основан на широком распространении препарата, с несколькими формами дозирования
** Только 12 мг дексаметазона было исследовано с (фос) апрепитантами/нетупитантами в рандомизированных исследованиях
Таблица 7. Рекомендуемые дозы антагонистов NK1 рецепторов.
| Антагонисты NK1 Рецепторов | Дозы и кратность |
| Апрепитант* и фосапрепитант острая рвота | Апрепитант 125мг внутрь однократно в день химиотерапии* -или- Фосапрепитант 150 в/в, однократно в день химиотерапии |
| Апрепитант* и фосапрепитант отсроченная рвота | Апрепитант 80мг внутрь однократно в течении 2-х дней после химиотерапии |
| Ролапитант | 180мг внутрь однократно в день химиотерапии |
| Нетупитант | 300 мг нетупитант / 0,5 мг палоносетрон перорально один раз в день химиотерапии |
* Апрепитант 165 мг, одна доза перед химиотерапией (не применяется на 2-3 день). Рекомендовано ЕМА и другими органами.
Рекомендации по профилактики преждевременной тошноты и рвоты
Наилучший подход для профилактики преждевременной рвоты это наилучший контроль над острой и отсроченной рвотой.
Психотерапия, особенно прогрессивное обучение мышечной релаксации, систематическая десенситизация и гипноз, могут быть использованы для лечения преждевременной тошноты и рвоты.
Только бензодиазепины уменьшают частоту преждевременной тошноты и рвоты, но их эффективность имеет тенденцию к снижению при продолжающейся химиотерапии.
Большинство медицинских онкологических сообществ (NCCN, ASCO, EORTC, RUSSCO) рекомендуют использовать следующие Г-КСФ: липэгфилграстим, эмпэгфилграстим, пэгфилграстим (филграстим, соединенный с полиэтиленгликолем), филграстим (негликозилированный Г-КСФ), ленограстим (гликозилированный Г-КСФ). Липэгфилграстим, эмпэгфилграстим и пэгфилграстим представляют собой препараты пролонгированного действия и вводятся однократно после курса ХТ. Пролонгированное действие обусловлено тем, что препарат не выводится с мочой и дольше циркулирует в крови.
| МНН | Группа КСФ | Режим введения |
| Филграстим | Рекомбинантный человеческий негликолизированный Г-КСФ | 5 мкг/кг массы тела 1 раз/сут. п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до необходимого стабильного АЧН |
| Пэгфилграстим | Рекомбинантный пегилированный Г-КСФ (филграстим), конъюгированный с полиэтиленгликолем, пролонгированного действия | 6 мг (без учета массы тела) однократно п/к не ранее чем через 24 часа и не позднее 14-ых сут. после курса ХТ |
| Липэгфилграстим | Гликопегилированный Г-КСФ пролонгированного действия | 100 мкг/кг или 6 мг (без учета массы тела) п/к однократно через 24 ч после окончания цикла ХТ |
| Эмпэгфилграстим | Ковалентный коньюгат филграстима с одной молекулой полиэтиленгликоля, пролонгированного действия | 7,5 мг (без учета массы тела) п/к однократно не ранее чем через 24 часа и не позднее 14-ых сут. после курса ХТ |
| Ленограстим | Рекомбинантный человеческий гликолизированный Г-КСФ | 19,2 млн. МЕ (или 150 мкг) на м² поверхности тела (0,64 млн. МЕ или 5 мкг на кг массы тела) в день п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до достижения необходимого стабильного АЧН |
Коррекция анемии:
Анемия при новообразованиях (В63.0 код по МКБ 10) определяется как снижение концентрации Hb ниже нормального значения (обычно 120 г/л) и может быть обусловлена как наличием самой опухоли, так и ее лечением. Слабая степень анемии представляет собой снижение концентрации Hb в диапазоне от 100 до 119 г/л, анемия средней степени – концентрация Hb от 80 до 99 г/л, тяжелая анемия – концентрация Hb ниже 80 г/л.
Препараты рекомендованные для лечения анемии у онкологических больных