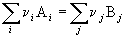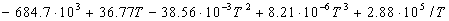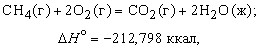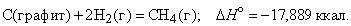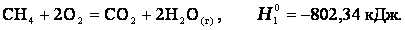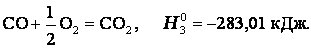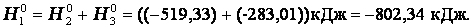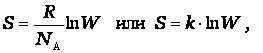Как посчитать энтальпию реакции формула
Как посчитать энтальпию реакции формула
Термохимия изучает тепловые эффекты химических реакций. Во многих случаях эти реакции протекают при постоянном объеме или постоянном давлении. Из первого закона термодинамики следует, что при этих условиях теплота является функцией состояния. При постоянном объеме теплота равна изменению внутренней энергии:
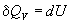
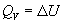
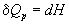
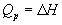
Эти равенства в применении к химическим реакциям составляют суть закона Гесса:
Тепловой эффект химической реакции, протекающей при постоянном давлении или постоянном объеме, не зависит от пути реакции, а определяется только состоянием реагентов и продуктов реакции.
Из закона Гесса вытекают важные следствия, которые позволяют рассчитывать энтальпии химических реакций.
Следствие 1. Стандартная энтальпия химической реакции
равна разности стандартных энтальпий образования продуктов реакции и реагентов (с учетом стехиометрических коэффициентов):
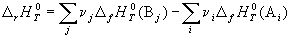
Стандартной энтальпией (теплотой) образования вещества 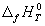
Следствие 2. Стандартная энтальпия химической реакции
равна разности энтальпий сгорания реагентов и продуктов реакции (с учетом стехиометрических коэффициентов):
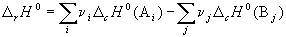
(c означает «combustion»). Стандартной энтальпией (теплотой) сгорания вещества называют энтальпию реакции полного окисления одного моля вещества. Это следствие обычно используют для расчета тепловых эффектов органических реакций.
Следствие 3. Энтальпия химической реакции равна разности энергий разрываемых и образующихся химических связей.
Энергией связи A- B называют энергию, необходимую для разрыва связи и разведения образующихся частиц на бесконечное расстояние:
Энергия связи всегда положительна.
Большинство термохимических данных в справочниках приведено при температуре 298 К. Для расчета тепловых эффектов при других температурах используют уравнение Кирхгофа:
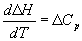
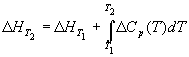
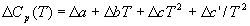
ПРИМЕРЫ
Решение. Энтальпии образования соответствуют следующим реакциям:
Вторую реакцию можно провести в две стадии: сначала сжечь водород с образованием жидкой воды по первой реакции, а затем испарить воду:
Тогда, согласно закону Гесса,
Пример 3-2. Рассчитайте энтальпию реакции
а) по энтальпиям образования; б) по энергиям связи, в предположении, что двойные связи в молекуле C6H6 фиксированы.
б) В данной реакции химические связи не разрываются, а только образуются. В приближении фиксированных двойных связей молекула C6H6 содержит 6 связей C- H, 3 связи C- C и 3 связи C=C. Энергии связей (в кДж/моль) (P.W.Atkins, Physical Chemistry, 5th edition, p. C7): E(C- H) = 412, E(C- C) = 348, E(C=C) = 612. Энтальпия реакции равна:
Пример 3-3. Пользуясь справочными данными, рассчитайте энтальпию реакции
Решение. Сокращенное ионное уравнение реакции имеет вид:
По закону Гесса, энтальпия реакции равна:
(энтальпии образования меди и иона H + равны, по определению, 0). Подставляя значения энтальпий образования (P.W.Atkins, Physical Chemistry, 5th edition, pp. C9-C15), находим:
(в расчете на три моля меди).
Решение. Энтальпия реакции сгорания метана
Найдем разность теплоемкостей как функцию температуры:
Энтальпию реакции при 1000 К рассчитаем по уравнению Кирхгофа:
ЗАДАЧИ
3-2. Стандартная энтальпия реакции CaCO3(тв) = CaO(тв) + CO2(г), протекающей в открытом сосуде при температуре 1000 К, равна 169 кДж/моль. Чему равна теплота этой реакции, протекающей при той же температуре, но в закрытом сосуде?
3-3. Рассчитайте стандартную внутреннюю энергию образования жидкого бензола при 298 К, если стандартная энтальпия его образования равна 49.0 кДж/моль.
3-4. Рассчитайте энтальпию образования N2O5(г) при T = 298 К на основании следующих данных:
3-6. Определите энтальпию образования диборана B2H6(г) при T = 298 К из следующих данных:
3-7. Рассчитайте теплоту образования сульфата цинка из простых веществ при T = 298 К на основании следующих данных:
3-9. Рассчитайте тепловой эффект реакции
при T = 298 K, если известны следующие данные:
3-12. Рассчитайте стандартный тепловой эффект реакции нейтрализации
NaOH + HCl = NaCl + H2O,
протекающей в водном растворе при 298 К.
3-13. Рассчитайте стандартный тепловой эффект реакции
3-14. Напишите уравнение Кирхгофа для реакции, протекающей при постоянном объеме.
3-15. Зависимость теплового эффекта реакции CH3OH(г) + 3/2O2 = CO2 + 2H2O(г) от температуры выражается уравнением:


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Энергетика химических процессов. Закон Гесса
Материалы портала onx.distant.ru
Тепловой эффект процесса
Количество выделенной (или поглощенной) теплоты Q в данном процессе называют тепловым эффектом процесса. Экзотермической является реакция, протекающая с выделением теплоты, а эндотермической – с поглощением теплоты из окружающей среды.
Для лабораторных и промышленных процессов наиболее типичен изобарный режим (Р=const). Поэтому обычно рассматривают тепловой эффект при Р,Т = const, т.е. изменение энтальпии процесса ΔН.
Следует отметить, что абсолютные значения энтальпии Н определить не представляется возможным, так как не известна абсолютная величина внутренней энергии.
Для экзотермической реакции (Q > 0) ΔН 0.
Термохимические уравнения
Химические уравнения, в которых дополнительно указывается величина изменения энтальпии реакции, а также агрегатное состояние веществ и температура, называются термохимическими уравнениями.
В термохимических уравнениях отмечают фазовое состояние и аллотропные модификации реагентов и образующихся веществ: г – газообразное, ж – жидкое, к – кристаллическое; S(ромб), S(монокл), С(графит), С(алмаз) и т.д.
Важно подчеркнуть, что с термохимическими уравнениями можно проводить алгебраические операции сложения, вычитания, деления, умножения.
Закон Гесса
Изменение энтальпии (внутренней энергии) химической реакции зависит от вида, состояния и количества исходных веществ и продуктов реакции, но не зависит от пути процесса.
Следствия из закона Гесса
Стандартные термодинамические величины
Стандартные термодинамические величины – это такие величины, которые относятся к процессам, все ингредиенты которых находятся в стандартных состояниях.
Стандартным состоянием вещества, находящегося в конденсированной фазе (кристаллической или жидкой), является реальное состояние вещества, находящегося при данной температуре и давлении 1 атм.
Следует подчеркнуть, что стандартное состояние может иметь место при любой температуре.
Обычно тепловой эффект (изменение энтальпии) реакции приводится для температуры 25 о С (298,15 К) и давления 101,325 кПа (1 атм), т.е. указывается стандартная энтальпия ΔН о 298.
Стандартные энтальпии образования и сгорания
Стандартная энтальпия образования ΔН о f,298 (или ΔН о обр,298) – это изменение энтальпии в процессе образования данного вещества (обычно 1 моль), находящегося в стандартном состоянии, из простых веществ, также находящихся в стандартном состоянии, причем простые вещества присутствуют в наиболее термодинамически устойчивых состояниях при данной температуре.
при Т = 298,15 К и Р = 1 атм.
Стандартная энтальпия образования простых веществ равна нулю по определению (для наиболее устойчивых их модификаций при данной температуре).
Стандартной энтальпией сгорания ΔН o сгор,298 называют энтальпию сгорания вещества (обычно 1 моль), находящегося в стандартном состоянии с образованием СО2(г), Н2О(ж) и других веществ, состав которых должен быть специально указан. Все продукты сгорания также должны находиться в стандартном состоянии.
Примеры решения задач
Задача 1. Используя справочные термодинамические данные вычислить ΔН o 298 реакции:
Решение. Решим задачу, используя оба следствия из закона Гесса. Ниже для исходных веществ и продуктов реакции приведены значения энтальпий образования и сгорания в кДж/моль (энтальпия сгорания сероводорода до SO2(г) и H2O(ж)):
| Вещество | H2S(г) | O2(г) | SO2(г) | H2O(ж) |
| ΔН o f,298 | -20,60 | 0 | -296,90 | -285,83 |
| ΔН o сгор,298 | -562,10 | 0 | 0 | 0 |
Cогласно первому следствию закона Гесса энтальпия этой реакции ΔН о х.р. равна:
В соответствии со вторым следствием закона Гесса получаем:
ΔН о х.р.,298 = 2ΔН о сгор,298(H2S(г)) = 2(-562,10) = — 1124,20 кДж.
Задача 2. Вычислите ΔН о 298 реакции N2(г) + 3H2(г) = 2NH3(г), используя следующие данные:
Определите стандартную энтальпию образования NH3(г).
Решение. Поскольку с термохимическими уравнениями можно производить все алгебраические действия, то искомое уравнение получится, если:
Таким образом, тепловой эффект реакции N2(г) + 3H2(г) = 2NH3(г) равен:
Δ Н о 298 = (- ΔН о 1/2) + (- 3/2·ΔН о 2) = 765,61 + (- 857,49) = — 91,88 кДж.
Поскольку в рассматриваемой реакции образуется 2 моль NH3(г), то
ΔН о f,298(NH3(г)) = — 91,88/2 = — 45,94 кДж/моль.
Задача 3. Определите энтальпию процесса
если при 298,15 К энтальпия растворения CuSO4(к) в n моль Н2О с образованием раствора CuSO4(р-р, nH2O) равна –40, а энтальпия растворения CuSO4·5H2O(к) с образованием раствора той же концентрации равна +10,5 кДж/моль.
Решение. Составляем цикл Гесса:
ΔН о 1 = ΔН о 2 + ΔН о х (по закону Гесса). Отсюда получаем:
Другой вариант решения.
По закону Гесса: ΔН о 1 = ΔН о х+ ΔН о 3, т.е. при сложении уравнений (2) и (3) получим уравнение (1).
Задача 4. Вычислите энтальпию образования химической связи С= С в молекуле этилена, если его стандартная энтальпия образования равна 52,3 кДж/моль, энтальпия возгонки графита составляет 716,7 кДж/моль, энтальпия атомизации водорода равна +436,0 кДж/моль, энтальпия образования связи С–Н равна –414,0 кДж/моль.
Решение. Составляем цикл Гесса:
ΔН о (С = С) = 52,3 — 2·716,7 — 2·436,0 + 4·414,0 = — 597,1 кДж/моль.
Задачи для самостоятельного решения
1. Составьте уравнение реакции, для которой ΔН о соответствует стандартной энтальпии образования ВaCl2·2H2O(к).
Энтальпи́я, также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.
Проще говоря, энтальпия — это та энергия, которая доступна для преобразования в теплоту при определенном постоянном давлении.
Так как энтальпия зависит от со стояния системы, но не зависит от пути процесса, то, если при проведении процесса система вернулась в исходное состояние, суммарное изменение энтропии системы равно нулю (dH = 0). Процессы, в которых система после последовательных превращений возвращается в исходное состояние, называются круговыми процессами или циклами. Итак, закон Гесса показывает, что каким бы путем не протекала реакция, ее тепловой эффект будет одинаков, если при этом не меняется конечное и исходное состояния системы.
Энтальпия химических реакций.Закон Гесса позволяет рассчитать энтальпию химических реакций. Согласно следствию из закона Гесса, энтальпия химической реакции равна сумме энтальпии образования продуктов реакций за вычетом суммы энтальпий образования веществ исходных с учетом стехиометрических коэффициентов Стандартный тепловой эффект реакции получения водорода из природного газа:
СН4 + 2Н2О(г) = СО2 + 4Н2 определяется по уравнению:
Подставляя значения величин энтальпий образования из приложения 2 (в кДж/моль), получаем
Термохимические уравнения.
Теплота, высвобождаемая или поглощаемая конкретной химической реакцией, пропорциональна степени превращения реагентов, определяемой по количеству любого из расходуемых либо образующихся продуктов. Изменение внутренней энергии или энтальпии реагирующей системы определяют по химическому уравнению реакции. Например, сгорание смеси газообразных метана и кислорода описывается термохимическим уравнением
7. Стандартные теплоты образования и сгорания. Термохимические расчеты и их использование для энергетической характеристики биохимических процессов
Стандартная теплота образования.
Из закона сохранения энергии следует, что, когда вещество образуется из атомов и (или) более простых веществ, внутренняя энергия или энтальпия системы меняется на определенную величину, называемую теплотой образования данного вещества. Теплота образования может быть определена различными способами, в том числе прямыми калориметрическими измерениями и путем косвенного расчета (на основе закона Гесса) из теплоты реакции, в которой участвует данное вещество. При проведении расчетов пользуются стандартными (при p = 1 атм и T = 298 K) теплотами образования веществ, входящих в уравнение реакции. Например, стандартную теплоту (энтальпию) образования метана можно вычислить с помощью термохимического уравнения
Хотя эта реакция практически неосуществима при 25 С, стандартная теплота образования метана косвенно рассчитывается по измеренным теплотам сгорания метана, водорода и графита. На основе закона Гесса устанавливается, что теплота реакции равна разности между теплотами сгорания веществ, указанных в левой части уравнения, и теплотами сгорания веществ, указанных в правой части уравнения реакции (взятых с соответствующими знаками и стехиометрическими коэффициентами).
Помимо использования термохимических данных для решения проблем практического использования тепловой энергии, они широко применяются при теоретической оценке энергий химических связей.
Тепловой эффект реакции зависит от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути реакции.
Закон лежит в основе термохимических расчетов. Рассмотрим реакцию сгорания метана:
Эту же реакцию можно провести через стадию образования СО:
Итак, видно, тепловой эффект реакции, протекающей по двум путям, одинаков.
При термохимических расчетах для определения тепловых эффектов применяют следствия из закона Гесса.
8. Второе начало термодинамики. Энтропия.
Состояние некоторого количества вещества можно охарактеризовать, указав, например, температуру, давление – это характеристики макросостояния или указать мгновенные характеристики каждой частицы вещества – ее положение в пространстве (xi, yi, zi) и скорости перемещения по всем направлениям (vx, vy, vz) – это характеристики микросостояния вещества. Так как вещество состоит из огромного числа частиц, то данному макросостоянию отвечает огромное число микросостояний.Число микросостояний, которое соответствует данному макросостоянию вещества, называется термодинамической вероятностью состояния системы – W.
Величина W есть число различных способов, посредством которых реализуется данное состояние вещества. Макросостояние тем вероятнее, чем большим числом микросостояний оно осуществляется. Так для системы из 10 молекул W близко к 10000. Оказалось удобнее и проще характеризовать состояние системы не самой вероятностью осуществления данного макросостояния, а величиной, пропорциональной ее логарифму.
Эта величина называется энтропией и обозначается буквой S.
Как показано Больцманом,
·
S – характеризует состояния системы и возможные изменения состояний, поэтому является функцией термодинамического состояния. Каждому состоянию системы соответствует определенное значение энтропии. Следовательно, вероятность различных состояний системы (газовое, жидкое, твердое) можно количественно выразить значением энтропии. Абсолютные значения энтропии можно определить экспериментально для простых и сложных веществ или взять из справочника термодинамических величин.
Величину S можно рассматривать как меру неупорядоченности состояния системы, то есть как количественную меру беспорядка.
2 закон термодинамики
В изолированных системах самопроизвольно протекают только те процессы, которые сопровождаются ростом энтропии системы.
В справочниках приводится, так называемая, стандартная энтропия 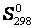
bB + dD = lL + mM изменение энтропии (энтропия реакции) можно рассчитать как разницу между суммарной энтропией продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов в соответствии с уравнением
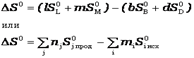
где nj, mi – коэффициенты уравнения реакции для продуктов и исходных веществ; 
Энтропия растет (ΔS > 0) в процессах, связанных с повышением температуры, при плавлении вещества, при испарении, при расширении системы, растворении. В этих случаях увеличение числа частиц и энергии теплового движения увеличивает беспорядок и, следовательно, увеличивается энтропия, и наоборот – охлаждение, конденсация, кристаллизация, реакции с уменьшением объема – сопровождаются уменьшением энтропии (ΔS 0). «Движущая сила» реакции определяется разностью между этими величинами и обозначается ΔG.
и называется изменением энергии Гиббса (изобарно-изотермический потенциал).
энергию Гиббса химической реакции можно рассчитать как сумму энергий Гиббса образования продуктов реакции за вычетом энергий Гиббса образования исходных веществ с учетом стехиометрических коэффициентов по формуле:
где ΔfG –энергия Гиббса образования веществ.
Энергия Гиббса образования веществ это изменение энергии Гиббса системы при образовании 1 моль вещества из простых веществ, устойчивых при 298 К.
Полученное значение ΔG является критерием самопроизвольного течения реакции в прямом направлении, если ΔG 0. Если ΔG = 0, то реакция может протекать как в прямом, так и в обратном направлениях, т.е. реакция обратима.
Так как энтальпия зависит от со стояния системы, но не зависит от пути процесса, то, если при проведении процесса система вернулась в исходное состояние, суммарное изменение энтропии системы равно нулю (dH = 0). Процессы, в которых система после последовательных превращений возвращается в исходное состояние, называются круговыми процессами или циклами. Итак, закон Гесса показывает, что каким бы путем не протекала реакция, ее тепловой эффект будет одинаков, если при этом не меняется конечное и исходное состояния системы.
Энтальпия химических реакций.Закон Гесса позволяет рассчитать энтальпию химических реакций. Согласно следствию из закона Гесса, энтальпия химической реакции равна сумме энтальпии образования продуктов реакций за вычетом суммы энтальпий образования веществ исходных с учетом стехиометрических коэффициентов Стандартный тепловой эффект реакции получения водорода из природного газа:
СН4 + 2Н2О(г) = СО2 + 4Н2 определяется по уравнению:
Подставляя значения величин энтальпий образования из приложения 2 (в кДж/моль), получаем
Термохимические уравнения.
Теплота, высвобождаемая или поглощаемая конкретной химической реакцией, пропорциональна степени превращения реагентов, определяемой по количеству любого из расходуемых либо образующихся продуктов. Изменение внутренней энергии или энтальпии реагирующей системы определяют по химическому уравнению реакции. Например, сгорание смеси газообразных метана и кислорода описывается термохимическим уравнением
7. Стандартные теплоты образования и сгорания. Термохимические расчеты и их использование для энергетической характеристики биохимических процессов
Стандартная теплота образования.
Из закона сохранения энергии следует, что, когда вещество образуется из атомов и (или) более простых веществ, внутренняя энергия или энтальпия системы меняется на определенную величину, называемую теплотой образования данного вещества. Теплота образования может быть определена различными способами, в том числе прямыми калориметрическими измерениями и путем косвенного расчета (на основе закона Гесса) из теплоты реакции, в которой участвует данное вещество. При проведении расчетов пользуются стандартными (при p = 1 атм и T = 298 K) теплотами образования веществ, входящих в уравнение реакции. Например, стандартную теплоту (энтальпию) образования метана можно вычислить с помощью термохимического уравнения
Хотя эта реакция практически неосуществима при 25 С, стандартная теплота образования метана косвенно рассчитывается по измеренным теплотам сгорания метана, водорода и графита. На основе закона Гесса устанавливается, что теплота реакции равна разности между теплотами сгорания веществ, указанных в левой части уравнения, и теплотами сгорания веществ, указанных в правой части уравнения реакции (взятых с соответствующими знаками и стехиометрическими коэффициентами).
Помимо использования термохимических данных для решения проблем практического использования тепловой энергии, они широко применяются при теоретической оценке энергий химических связей.
Тепловой эффект реакции зависит от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути реакции.
Закон лежит в основе термохимических расчетов. Рассмотрим реакцию сгорания метана:
Эту же реакцию можно провести через стадию образования СО:
Итак, видно, тепловой эффект реакции, протекающей по двум путям, одинаков.
При термохимических расчетах для определения тепловых эффектов применяют следствия из закона Гесса.
8. Второе начало термодинамики. Энтропия.
Состояние некоторого количества вещества можно охарактеризовать, указав, например, температуру, давление – это характеристики макросостояния или указать мгновенные характеристики каждой частицы вещества – ее положение в пространстве (xi, yi, zi) и скорости перемещения по всем направлениям (vx, vy, vz) – это характеристики микросостояния вещества. Так как вещество состоит из огромного числа частиц, то данному макросостоянию отвечает огромное число микросостояний.Число микросостояний, которое соответствует данному макросостоянию вещества, называется термодинамической вероятностью состояния системы – W.
Величина W есть число различных способов, посредством которых реализуется данное состояние вещества. Макросостояние тем вероятнее, чем большим числом микросостояний оно осуществляется. Так для системы из 10 молекул W близко к 10000. Оказалось удобнее и проще характеризовать состояние системы не самой вероятностью осуществления данного макросостояния, а величиной, пропорциональной ее логарифму.
Эта величина называется энтропией и обозначается буквой S.
Как показано Больцманом,
·
S – характеризует состояния системы и возможные изменения состояний, поэтому является функцией термодинамического состояния. Каждому состоянию системы соответствует определенное значение энтропии. Следовательно, вероятность различных состояний системы (газовое, жидкое, твердое) можно количественно выразить значением энтропии. Абсолютные значения энтропии можно определить экспериментально для простых и сложных веществ или взять из справочника термодинамических величин.
Величину S можно рассматривать как меру неупорядоченности состояния системы, то есть как количественную меру беспорядка.
2 закон термодинамики
В изолированных системах самопроизвольно протекают только те процессы, которые сопровождаются ростом энтропии системы.
В справочниках приводится, так называемая, стандартная энтропия 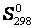
bB + dD = lL + mM изменение энтропии (энтропия реакции) можно рассчитать как разницу между суммарной энтропией продуктов реакции и исходных веществ с учетом стехиометрических коэффициентов в соответствии с уравнением
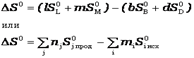
где nj, mi – коэффициенты уравнения реакции для продуктов и исходных веществ; 
Энтропия растет (ΔS > 0) в процессах, связанных с повышением температуры, при плавлении вещества, при испарении, при расширении системы, растворении. В этих случаях увеличение числа частиц и энергии теплового движения увеличивает беспорядок и, следовательно, увеличивается энтропия, и наоборот – охлаждение, конденсация, кристаллизация, реакции с уменьшением объема – сопровождаются уменьшением энтропии (ΔS 0). «Движущая сила» реакции определяется разностью между этими величинами и обозначается ΔG.
и называется изменением энергии Гиббса (изобарно-изотермический потенциал).
энергию Гиббса химической реакции можно рассчитать как сумму энергий Гиббса образования продуктов реакции за вычетом энергий Гиббса образования исходных веществ с учетом стехиометрических коэффициентов по формуле:
где ΔfG –энергия Гиббса образования веществ.
Энергия Гиббса образования веществ это изменение энергии Гиббса системы при образовании 1 моль вещества из простых веществ, устойчивых при 298 К.
Полученное значение ΔG является критерием самопроизвольного течения реакции в прямом направлении, если ΔG 0. Если ΔG = 0, то реакция может протекать как в прямом, так и в обратном направлениях, т.е. реакция обратима.
Направление химических реакций зависит от их характера. Так, условие ΔG 0). У таких реакций обе движущие силы (ΔН) и (ТΔS) направлены в сторону протекания прямой реакции и ΔG