с чем взаимодействует сульфат железа
Сульфат железа и железный купорос, характеристика, свойства и получение, химические реакции
Сульфат железа и железный купорос, характеристика, свойства и получение, химические реакции.
Сульфат железа – неорганическое вещество, имеет химическую формулу FeSO4.
Краткая характеристика сульфата железа:
Сульфат железа – неорганическое вещество белого или бесцветного цвета.
Химическая формула сульфата железа FeSO4.
С водой сульфат железа образует кристаллогидраты: гептагидрат сульфата железа FeSO4·7H2O, именуемый также железный купорос (прозрачные кристаллы светлого голубовато-зелёного цвета), тетрагидрат сульфата железа FeSO4·4H2O (прозрачные кристаллы зелёного цвета), моногидрат сульфата железа FeSO4·H2O.
Сульфат железа негорюч, пожаро- и взрывобезопасен.
В природе сульфат железа встречается в виде минерала мелантерита (FeSO4·7H2O).
Краткая характеристика железного купороса:
Железный купорос – неорганическое вещество светлого голубовато-зелёного цвета.
Химическая формула железного купороса FeSO4·7H2O.
Железный купорос – гептагидрат сульфата железа.
Хорошо растворяется в воде.
На воздухе постепенно выветривается (теряет кристаллизационную воду).
Железный купорос негорюч, пожаро- и взрывобезопасен.
Железный купорос относится к веществам 3-го класса опасности в соответствии с ГОСТ 12.1.007.
Физические свойства сульфата железа:
| Наименование параметра: | Значение: |
| Химическая формула | FeSO4 |
| Синонимы и названия иностранном языке | iron (II) sulfate (англ.) |
| Тип вещества | неорганическое |
| Внешний вид | бесцветные кристаллы |
| Цвет | белый, бесцветный |
| Вкус | —* |
| Запах | без запаха |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м 3 | 1898 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см 3 | 1,898 |
| Температура кипения, °C | — |
| Температура плавления, °C | — |
| Температура разложения, °C | 680 |
| Гигроскопичность | гигроскопичен |
| Молярная масса, г/моль | 151,932 |
| Растворимость в воде (20 o С), г/100 г | 26,3 |
Физические свойства железного купороса:
| Наименование параметра: | Значение: |
| Химическая формула | FeSO4·7H2O |
| Синонимы и названия иностранном языке | гептагидрат сульфата железа (II) |
iron (II) sulfate heptahydrate (англ.)
железный купорос (рус.)
Получение сульфата железа:
В промышленности сульфат железа получают как побочный продукт при травлении железных листов, проволоки, удалении окалины и пр., а также как побочный продукт производства оксида титана из ильменита.
Сульфат железа в промышленности может быть получен путем окислительного обжига пирита (FeS2).
В лаборатории сульфат железа получают в результате следующих химических реакций:
Сульфат Железа
Химическое название
Железа(II) сульфат, сульфат железа (III).
Химические свойства
Двухвалентное сернокислое железо – неорганическое соединение, соль образованная серной кислотой и железом. Вещество не имеет запаха, не летуче. Безводная форма имеет вид бесцветных не прозрачных мелких гигрокопичных кристаллов. Кристаллогидраты имеют характерный зеленовато-голубой окрас, тетрагидраты зеленого цвета. Химическая формула Сульфата Железа 2: FeSO4, рацемическая: O4SFe. На вкус соединение вяжущее, с привкусом металла. Средство хорошо растворяется в воде. Молекулярная масса = 151,9 грамм на моль.
Вещество выделяется из железного купороса. Раствор сульфата Fe(2) под действием кислорода окисляется в переходит в Сульфат Железа 3. Разлагается при температуре выше 480 градусов Цельсия на оксиды.
Сульфат Железа 2 можно получить при воздействии разбавленной серной кислоты на обрезки железа; в виде побочного продукта реакции травления железных листов, при удалении окалины, при окислительном обжиге пирита.
Гидролиз Сульфата Железа 2 протекает по катиону в кислой среде. Первая ступень гидролиза: Fe2+ + SO42- + HOH ↔ FeOH+ + SO42- + H+; теоретически может протекать и вторая ступень гидролиза: FeOH+ + SO42- + HOH ↔ Fe(OH)2↓ + SO42- + H+.
Сернокислое железо 3 или тетрасульфид 6 железа 3 – это светло-желтые парамагнитные мелкие кристаллы. Вещество хорошо растворяется в воде, медленно – в этиловом спирте. Химическая формула Сульфата Железа 3: Fe2(SО4)3, рацемическая: Fe2O12S3. Вещество обладает способностью кристаллизоваться в форме кристаллогидратов Fe2(SO4)3•n H2O. Наибольшее значение имеет нонагидрат сульфата железа(III). Водные растворы приобретают красно-коричневую окраску из-за реакции гидролиза, протекающей по катиону. Соединение разлагается под действие горячей воды и высоких температур. При 98 градусах нонагидрат превращается в тетрагидрат, при температуре выше 125 градусов – в моногидрат и выше 175 – в безводный сульфат Fe, который при температуре более 600 градусов разлагается на оксиды серы и железа.
Фармакологическое действие
Противоанемическое, устраняющее железодефицит. Кровоостанавливающее (Сульфат Железа 3).
Фармакодинамика и фармакокинетика
Железо является основным микроэлементом, входящим в состав гемоглобина, миоглобина и прочих компонентов крови. Вещество принимает участие в окислительно-восстановительных реакциях, связывается и переносит молекулы кислорода по организму, стимулирует гемопоэз и эритропоэз. Сульфат Железа обеспечивает синтез всех железосодержащих метаболитов. После поступления Fe с пищей, оно усваивается в двенадцатиперстной кишке и переносится в депо тканей с помощью ферментов трансферетинов.
После приема лекарства внутрь, его активные компоненты полностью усваиваются организмом. Максимальная концентрация в крови наблюдается через 2-4 часа.
Показания к применению
Противопоказания
Сульфат Железа 2 противопоказан к приему:
Побочные действия
Побочные реакции во время лечения Сульфатом Железа возникают не часто.
Инструкция по применению (Способ и дозировка)
Лекарство назначают внутрь. Минимальная эффективная дозировка в пересчете на элементарное железо составляет 100 мг. Максимальное количество лекарства, которое можно принять – до 400 мг.
В профилактических целях назначают от 30 до 60 мг элементарного железа в сутки.
Передозировка
При передозировке усиливаются побочные реакции от приема лекарства. Возникают: диарея, тошнота, болезненные ощущения в животе, рвота, аритмия и рост ЧСС, повышается проницаемость капилляров, возможен сердечно-сосудистый коллапс. В качестве терапии промывают желудок, вводят дефероксамин для связывания ионов железа.
Взаимодействие
При сочетании с аскорбиновой кислотой улучшается всасывание препаратов железа.
Сочетанный прием сульфата и антацидных средств с магнием, алюминием, кальцием, пеницилламином и колестирамином замедляет всасывание железа.
Не рекомендуется сочетать лекарство с тетрациклиновыми антибиотиками, так как происходит взаимное снижение системной абсорбции обоих препаратов.
При сочетании лекарства с ГКС взаимно усиливается эритропоэз.
Условия хранения
Препараты хранят в сухом, темном, прохладном месте в оригинальной упаковке. Нельзя использовать лекарство после истечения срока годности.
Особые указания
Во время лечения Сульфатом Железа ii может наблюдаться окрашивание кала в черный цвет и потемнение эмали зубов.
При заболеваниях почек и печени железо может накапливаться в организме.
Особую осторожность соблюдают при лечении пациентов с язвенной болезнью желудка и 12-персной кишки, при язвенном колите и энтерите.
Вещество рекомендуется комбинировать с Фолиевой кислотой при железодефицитной анемии с дефицитом фол. к-ты.
При курсовом приеме лекарства рекомендуют периодически проводить контроль гемоглобина и уровня сывороточного железа.
При беременности и лактации
Лекарство можно использовать во время кормления грудью и при беременности по показаниям.
Препараты, в которых содержится (Аналоги)
Отзывы
Некоторые отзывы о применении препаратов Сульфата Железа:
Цена Сульфата Железа, где купить
Цена на лекарство варьирует в зависимости от производителя и лек. формы. Купить Сульфат Железа можно в любой аптеке. Например, стоимость таблеток пролонгированного действия Тардиферон составляет порядка 200 рублей за 30 штук.
Образование: Окончила Ровенский государственный базовый медицинский колледж по специальности «Фармация». Окончила Винницкий государственный медицинский университет им. М.И.Пирогова и интернатуру на его базе.
Опыт работы: С 2003 по 2013 г. – работала на должностях провизора и заведующего аптечным киоском. Награждена грамотами и знаками отличия за многолетний и добросовестный труд. Статьи на медицинскую тематику публиковались в местных изданиях (газеты) и на различных Интернет-порталах.
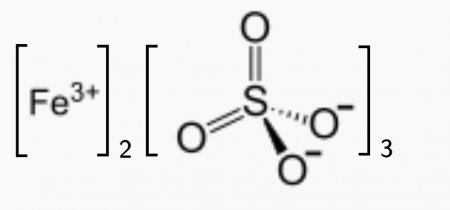
Сульфат железа (III)
| Сульфат железа (III) | |
|---|---|
 | |
| Систематическое наименование | сульфат железа (III) |
| Традиционные названия | сернокислое железо (III), тетрасульфид (VI) железа (III) |
| Хим. формула | Fe2(SO4)3 |
| Рац. формула | Fe2O12S3 |
| Состояние | безводный — светло-жёлтый порошок |
| Молярная масса | |
| • разложения | 600 |
| Мол. теплоёмк. | 271,75 Дж/(моль·К) |
| Энтальпия | |
| • образования | −2580 кДж/моль |
| Растворимость | |
| • в воде | (безв.) растворим(нонагидрат) 440 г/100 мл |
| • в этаноле | (нонагидрат) растворим |
| Рег. номер CAS | 15244-10-7 (для всех гидратов с формулой Fe2(SO4)3·nH2O (где n=1, 3, 4, 6, 7, 9, 10, 12) |
| RTECS | NO8505000 |
| ChEBI | 53438 |
| ChemSpider | 23211 и 21493902 |
| ЛД50 | (крысы, орально) 500 мг/кг |
| Пиктограммы ECB |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Содержание
Физические свойства
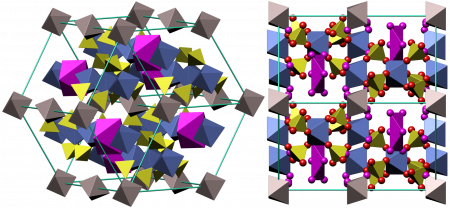
Безводный сульфат железа (III) — светло-жёлтые парамагнитные очень гигроскопичные кристаллы моноклинной сингонии, пространственная группа P21/m, параметры элементарной ячейки a = 0,8296 нм, b = 0,8515 нм, c = 1,160 нм, β = 90,5°, Z = 4. Есть данные, что безводный сульфат железа образовывает орторомбическую и гексагональную модификации. Растворим в воде, трудно растворим в этаноле.
Из воды кристаллизуется в виде кристаллогидратов Fe2(SO4)3·n H2O, где n = 12, 10, 9, 7, 6, 4, 3, 1. Наиболее изученный кристаллогидрат — нонагидрат сульфата железа (III) Fe2(SO4)3·9H2O — жёлтые гексагональные кристаллы, параметры элементарной ячейки a = 1,085 нм, c = 1,703 нм, Z = 4. Хорошо растворяется в воде (440 г на 100 г воды). В водных растворах сульфат железа(III) из-за гидролиза приобретает красно-коричневый цвет.
При нагревании нонагидрат превращается при 98 °C в тетрагидрат, при 125 °C — в моногидрат и при 175 °C — в безводный Fe2(SO4)3, который выше 600 °C разлагается на Fe2O3 и SO3.
Нахождение в природе
Все перечисленные выше природные гидраты железа на поверхности Земли нестабильны. Но их запасы постоянно пополняются благодаря окислению других минералов (в основном пирита и марказита).
Сульфат железа и ярозит были обнаружены двумя марсоходами: «Спирит» и «Оппортьюнити». Эти вещества являются признаком сильных окислительных условий на поверхности Марса. В мае 2009 года «Спирит» застрял, когда ехал по мягкому грунту планеты и наехал на залежи сульфата железа, скрытые под слоем обычного грунта. Вследствие того, что сульфат железа имеет очень низкую плотность, марсоход застрял настолько глубоко, что часть его корпуса коснулась поверхности планеты.
Получение
В промышленности сульфат железа (III) получают прокаливанием пирита или марказита с NaCl на воздухе:
или растворяют оксид железа (III) в серной кислоте:
В лабораторной практике сульфат железа (III) можно получить из гидроокиси железа (III):
Препарат той же чистоты можно получить окислением сульфата железа (II) азотной кислотой:
также окисление можно провести кислородом или оксидом серы:
Концентрированные серная и азотная кислоты окисляют сульфид железа до сульфата железа (III):
Дисульфид железа можно окислить концентрированной серной кислотой:
Сульфат-аммоний железа (II) (соль Мора) также можно окислить дихроматом калия. Вследствие данной реакции выделятся сразу четыре сульфата — железа (III), хрома (III), аммония и калия, и вода:
Сульфат железа (III) можно получить как один из продуктов термического разложения сульфата железа (II):
Ферраты с разбавленной серной кислотой восстанавливаются до сульфата железа (III):
При нагревании пентагидрата до температуры 70—175 °C получается безводный сульфат железа (III):
Сульфат железа (II) можно окислить триоксидом ксенона:
Химические свойства
Сульфат железа (III) в водных растворах подвергается сильному гидролизу по катиону, при этом раствор окрашивается в красновато-коричневый цвет:
Горячая вода или пар разлагают сульфат железа (III):
Безводный сульфат железа (III) при нагревании разлагается:
Растворы щелочей разлагают сульфат железа (III), продукты реакции зависят от концентрации щёлочи:
Если с щёлочью взаимодействует эквимолярный раствор сульфатов железа (III) и железа (II), то в результате получится сложный оксид железа:
Активные металлы (такие как магний, цинк, кадмий, железо) восстанавливают сульфат железа (III):
Некоторые сульфиды металлов (например, меди, кальция, олова, свинца, ртути) в водном растворе восстанавливают сульфат железа (III):
С растворимыми солями ортофосфорной кислоты образует нерастворимый фосфат железа (III) (гетерозит):
Железо. Свойства железа и его соединений.
Железо
Положение в периодической системе химических элементов
Элемент железо расположен в побочной подгруппе VIII группы (или в 8 группе в современной форме ПСХЭ) и в четвертом периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение атома железа
Электронная конфигурация железа в основном состоянии :
+26Fe 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6
Железо проявляет ярко выраженные магнитные свойства.
Физические свойства
Железо – металл серебристо-белого цвета, с высокой химической активностью и высокой ковкостью. Обладает высокой тепло- и электропроводностью.

Температура плавления 1538 о С, температура кипения 2861 о С.
Нахождение в природе
Железо довольно распространено в земной коре (порядка 4% массы земной коры). По распространенности на Земле железо занимает 4-ое место среди всех элементов и 2-ое место среди металлов. Содержание в земной коре — около 8%.
В природе железо в основном встречается в виде соединений:

Магнитный железняк Fe3O4 или FeO·Fe2O3 (магнетит).
(изображение с портала emchi-med.ru)
В природе также широко распространены сульфиды железа, например, пирит FeS2.

Встречаются и другие минералы, содержащие железо.
Способы получения
Железо в промышленности получают из железной руды, гематита Fe2O3 или магнетита (Fe3O4или FeO·Fe2O3).
В печь загружают руду, кокс и флюсы.
Шихта – смесь исходных материалов, а в некоторых случаях и топлива в определённой пропорции, которую обрабатывают в печи.
Каменноугольный кокс – это твёрдый пористый продукт серого цвета, получаемый путем коксования каменного угля при температурах 950—1100 °С без доступа воздуха. Содержит 96—98 % углерода.
Флюсы – это неорганические вещества, которые добавляют к руде при выплавке металлов, чтобы снизить температуру плавления и легче отделить металл от пустой породы.
Шлак – расплав (а после затвердевания – стекловидная масса), покрывающий поверхность жидкого металла. Шлак состоит из всплывших продуктов пустой породы с флюсами и предохраняет металл от вредного воздействия газовой среды печи, удаляет примеси.
В печи кокс окисляется до оксида углерода (II):
2C + O2 → 2CO
Затем нагретый угарный газ восстанавливает оксид железа (III):
Процесс получения железа – многоэтапный и зависит от температуры.
Наверху, где температура обычно находится в диапазоне между 200 °C и 700 °C, протекает следующая реакция:
Ниже в печи, при температурах приблизительно 850 °C, протекает восстановление смешанного оксида железа (II, III) до оксида железа (II):
Встречные потоки газов разогревают шихту, и происходит разложение известняка:
Оксид железа (II) опускается в область с более высоких температур (до 1200 o C), где протекает следующая реакция:
FeO + CO → Fe + CO2
Углекислый газ поднимается вверх и реагирует с коксом, образуя угарный газ:
CO2 + C → 2CO

2. Также железо получают прямым восстановлением из оксида водородом:
При этом получается более чистое железо, т.к. получаемое железо не загрязнено серой и фосфором, которые являются примесями в каменном угле.
3. Еще один способ получения железа в промышленности – электролиз растворов солей железа.
Качественные реакции
Качественные реакции на ионы железа +2.
2NaOH + FeCl2 → Fe(OH)2 + 2NaCl
Видеоопыт взаимодействия раствора сульфата железа (II) с раствором гидроксида натрия (качественная реакция на ионы железа (II)) можно посмотреть здесь.
Гидроксид железа (II) на воздухе буреет, так как окисляется до гидроксида железа (III):
– ионы железа +2 окрашивают раствор в светлый желто-зеленый цвет.
– взаимодействие с красной кровяной солью K3[Fe(CN)6] – также качественная реакция на ионы железа +2. При этом образуется синий осадок «турнбулева синь».
Видеоопыт взаимодействия раствора хлорида железа (II) с раствором гексацианоферрата (III) калия (качественная реакция на ионы железа (II)) можно посмотреть здесь.
Качественные реакции на ионы железа +3

3NaOH + FeCl3 → Fe(OH)3 + 3NaCl
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором гидроксида натрия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
– ионы железа +3 окрашивают раствор в светлый желто-оранжевый цвет.
– взаимодействие с желтой кровяной солью K4[Fe(CN)6] ионы железа +3. При этом образуется синий осадок «берлинская лазурь».
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором гексацианоферрата (II) калия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
В последнее время получены данные, которые свидетельствуют, что молекулы берлинской лазури идентичны по строению молекулам турнбулевой сини. Состав молекул обоих этих веществ можно выразить формулой Fe4[Fe2(CN)6]3.
– при взаимодействии солей железа (III) с роданидами раствор окрашивается в кроваво-красный цвет.
FeCl3 + 3NaCNS → Fe(CNS)3 + 3NaCl
Видеоопыт взаимодействия раствора хлорида железа (III) с раствором роданида калия (качественная реакция на ионы железа (III)) можно посмотреть здесь.
Химические свойства
1.1. Железо реагирует с галогенами с образованием галогенидов. При этом активные неметаллы (фтор, хлор и бром) окисляют железо до степени окисления +3:
2Fe + 3Cl2 → 2FeCl3
Менее активный йод окисляет железо до степени окисления +2:
1.2. Железо реагирует с серой с образованием сульфида железа (II):
Fe + S → FeS
Fe + P → FeP
1.4. С азотом железо реагирует в специфических условиях с образованием нитрида дижелеза:
1.5. Железо реагирует с углеродом и кремнием с образованием карбида и силицида:
3Fe + C → Fe3C
1.6. При взаимодействии с кислородом железо образует окалину – двойной оксид железа (II, III):
При пропускании кислорода через расплавленное железо возможно образование оксида железа (II):
2Fe + O2 → 2FeO
2. Железо взаимодействует со сложными веществами.
2.1. При обычных условиях железо с водой практически не реагирует. Раскаленное железо может вступать в реакцию при температуре 700-900 о С с водяным паром:
3 Fe 0 + 4 H2 + O → Fe +3 3O4 + 4 H2 0
В воде в присутствии кислорода или во влажном воздухе железо медленно окисляется (корродирует):
2.2. Железо взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой). При этом образуются соль железа со степенью окисления +2 и водород.
Fe + 2HCl → FeCl2 + H2↑
2.3. При обычных условиях железо не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат железа (III) и вода:
2.4. Железо не реагирует при обычных условиях с концентрированной азотной кислотой также из-за пассивации. При нагревании реакция идет с образованием нитрата железа (III), оксида азота (IV) и воды:
С разбавленной азотной кислотой железо реагирует с образованием оксида азота (II):
При взаимодействии железа с очень разбавленной азотной кислотой образуется нитрат аммония:
Fe + CuSO4 → FeSO4 + Cu
Еще пример : простое вещество железо восстанавливает железо до степени окисления +2 при взаимодействии с соединениями железа +3:
2FeCl3 + Fe → 3FeCl2
Оксид железа (II)
Оксид железа (II) – это твердое, нерастворимое в воде вещество черного цвета.
Способы получения
Оксид железа (II) можно получить различными методами :
1. Частичным в осстановлением оксида железа (III).
Или частичным восстановлением оксида железа (III) угарным газом:
Еще один пример : восстановление оксида железа (III) железом:
2. Разложение гидроксида железа (II) при нагревании :
Химические свойства
1. При взаимодействии оксида железа (II) с кислотными оксидами образуются соли.
FeO + SO3 → FeSO4
FeO + 2HCl → FeCl2 + H2O
3. Оксид железа (II) не взаимодействует с водой.
4. Оксид железа (II) малоустойчив, и легко окисляется до соединений железа (III).
При взаимодействии с разбавленной азотной кислотой образуется оксид азота (II). Реакция идет при нагревании:
FeO + CO → Fe + CO2
Оксид железа (III)
Оксид железа (III) – это твердое, нерастворимое в воде вещество красно-коричневого цвета.
Способы получения
Оксид железа (III) можно получить различными методами :
1. Окисление оксида железа (II) кислородом.
2. Разложение гидроксида железа (III) при нагревании :
Химические свойства
1. При взаимодействии оксида железа (III) с кислотными оксидами и кислотами образуются соли.
3. Оксид железа (III) не взаимодействует с водой.
4. Оксид железа (III) окисляется сильными окислителями до соединений железа (VI).
Нитраты и нитриты в щелочной среде также окисляют оксид железа (III):
Также оксид железа (III) восстанавливается водородом:
Железом можно восстановить оксид железа только до оксида железа (II):
Оксид железа (III) реагирует также с некоторыми другими сильными восстановителями.
Fe2O3 + 3NaH → 3NaOH + 2Fe
6. Оксид железа (III) – твердый, нелетучий и амфотерный. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Оксид железа (II, III)
Оксид железа (II, III) (железная окалина, магнетит) – это твердое, нерастворимое в воде вещество черного цвета.
Фото с сайта wikipedia.ru
Способы получения
Оксид железа (II, III) можно получить различными методами :
1. Горение железа на воздухе:
2. Частичное восстановление оксида железа (III) водородом или угарным газом :
3. При высокой температуре раскаленное железо реагирует с водой, образуя двойной оксид железа (II, III):
Химические свойства
Свойства оксида железа (II, III) определяются свойствами двух оксидов, из которых он состоит: основного оксида железа (II) и амфотерного оксида железа (III).
1. При взаимодействии оксида железа (II, III) с кислотными оксидами и кислотами образуются соли железа (II) и железа (III).
Еще пример : оксид железа (II, III) взаимодействует с разбавленной серной кислотой.
2. Оксид железа (II, III) взаимодействует с сильными кислотами-окислителями (серной-концентрированной и азотной).
Разбавленной азотной кислотой окалина окисляется при нагревании:
Также оксид железа (II, III) окисляется концентрированной серной кислотой:
Также окалина окисляется кислородом воздуха :
3. Оксид железа (II, III) не взаимодействует с водой.
4. Оксид железа (II, III) окисляется сильными окислителями до соединений железа (VI), как и прочие оксиды железа (см. выше).
Также железная окалина восстанавливается водородом:
Оксид железа (II, III) реагирует также с некоторыми другими сильными восстановителями (йодидами и сульфидами).
Гидроксид железа (II)
Способы получения
1. Гидроксид железа (II) можно получить действием раствора аммиака на соли железа (II).
2. Гидроксид железа (II) можно получить действием щелочи на соли железа (II).
FeCl2 + 2KOH → Fe(OH)2↓ + 2KCl
Химические свойства
Гидроксид железа (II) взаимодействует с пероксидом водорода:
При растворении Fe(OH)2 в азотной или концентрированной серной кислотах образуются соли железа (III):
4. Г идроксид железа (II) разлагается при нагревании :
Гидроксид железа (III)
Способы получения
1. Гидроксид железа (III) можно получить действием раствора аммиака на соли железа (III).
2. Окислением гидроксида железа (II) кислородом или пероксидом водорода:
3. Гидроксид железа (III) можно получить действием щелочи на раствор соли железа (III).
FeCl3 + 3KOH → Fe(OH)3↓ + 3KCl
Видеоопыт получения гидроксида железа (III) взаимодействием хлорида железа (III) и гидроксида калия можно посмотреть здесь.
Например: бромид железа (III) реагирует с карбонатом натрия. При этом выпадает осадок гидроксида железа (III), выделяется углекислый газ и образуется бромид натрия:
Взаимодействие хлорида железа (III) с сульфитом, например, калия — очень интересная реакция. Во-первых, в некоторых источниках указывается, что в ней таки может протекать необратимый гидролиз. Но для ЕГЭ лучше считать, что при этом протекает ОВР. Во-вторых, ОВР можно записать в разных видах:
Также допустима такая запись:
Химические свойства
3. Гидроксид железа (III) взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—ферриты, а в растворе реакция практически не идет. При этом гидроксид железа (III) проявляет кислотные свойства.
4. Г идроксид железа (III) разлагается при нагревании :
Видеоопыт взаимодействия гидроксида железа (III) с соляной кислотой можно посмотреть здесь.
Соли железа
Нитраты железа
Нитрат железа (II) при нагревании разлагается на оксид железа (III), оксид азота (IV) и кислород:
Нитрат железа (III) при нагревании разлагается также на оксид железа (III), оксид азота (IV) и кислород:
Гидролиз солей железа
Растворимые соли железа, образованные кислотными остатками сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. частично:
I ступень: Fe 3+ + H2O ↔ FeOH 2+ + H +
II ступень: FeOH 2+ + H2O ↔ Fe(OH )2 + + H +
Однако сульфиты и карбонаты железа (III) и их кислые соли гидролизуются необратимо, полностью, т.е. в водном растворе не существуют, а разлагаются водой:
При взаимодействии соединений железа (III) с сульфидами протекает ОВР:
2FeCl3 + 3Na2S → 2FeS + S + 6NaCl
Более подробно про гидролиз можно прочитать в соответствующей статье.
Окислительные свойства железа (III)
Соли железа (III) под проявляют довольно сильные окислительные свойств. Так, при взаимодействии соединений железа (III) с сульфидами протекает окислительно-восстановительная реакция.
Например : хлорид железа (III) взаимодействует с сульфидом натрия. При этом образуется сера, хлорид натрия и либо черный осадок сульфида железа (II) (в избытке сульфида натрия), либо хлорид железа (II) (в избытке хлорида железа (III)):
2FeCl3 + 3Na2S → 2FeS + S + 6NaCl
2FeCl3 + Na2S → 2FeCl2 + S + 2NaCl
По такому же принципу соли железа (III) реагируют с сероводородом:
2FeCl3 + H2S → 2FeCl2 + S + 2HCl
2FeCl3 + 2KI → 2FeCl2 + I2 + 2KCl
Однако, соли железа со степенью окисления +3 в этом ряду являются небольшим исключением. Ведь для железа характерны две степени окисления: +2 и +3. И железо со степенью окисления +3 является более сильным окислителем. Таким образом, условно говоря, железо со степенью окисления +3 расположено в ряду активности после меди. И соли железа (III) могут реагировать еще и с металлами, которые расположены правее железа! Но до меди, включительно. Вот такой парадокс.
И еще один момент. Соединения железа (III) с этими металлами реагировать будут, а вот соединения железа (II) с ними реагировать не будут. Таким образом, металлы, расположенные в ряду активности между железом и медью (включая медь) при взаимодействии с солями железа (III) восстанавливают железо до степени окисления +2. А вот металлы, расположенные до железа в ряду активности, могут восстановить железо и до простого вещества.
А вот реакция нитрата железа (III) с цинком протекает уже по привычному механизму. И железо восстанавливается до простого вещества: