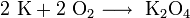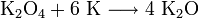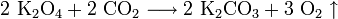с чем активно взаимодействует калий
Калий: способы получения и химические свойства
Калий К — это щелочной металл. Серебристо-белый, мягкий, легкоплавкий.
Относительная молекулярная масса Mr = 39,098; относительная плотность для твердого состояния d = 0,8629; относительная плотность для жидкого состояния d = 0,83; tпл = 63, 51º C; tкип = 760º C.
Способ получения
1. Калий получают в промышленности путем разложения гидрида калия при температуре 400º С в вакууме, при этом образуются калий и водород :
2KH = 2K + H2
2. В результате электролиза жидкого гидроксида калия образуются калий, кислород и вода :
4KOH → 4K + O2↑ + 2H2O
Качественная реакция
Химические свойства
1.1. Калий легко реагирует с водородом при 200–350º C образованием гидрида калия:
2K + H2 = 2KH
1.2. Калий сгорает в кислороде с образованием надпероксида калия:
2K + F2 = 2KF
2K + Cl2 = 2KCl
2K + Br2 = 2KBr
2K + I2 = 2KI
1.4. С серой, теллуром и селеном реагирует при температуре 100–200º C с образованием сульфида калия, селенида калия и теллурид калия :
2K + S = K2S
2K + Se = K2Se
2K + Te = K2Te
1.5. Калий реагирует с фосфором при 200º C в атмосфере аргона с образованием фосфида калия:
3K + P = K3P
2. Калий активно взаимодействует со сложными веществами:
2K 0 + 2 H2 O = 2 K + OH + H2 0
2.2.1. Ка лий реагирует с разбавленной соляной кислотой, при этом образуются хлорид калия и водород :
2K + 2HCl = 2KCl + H2 ↑
2.2.2. При взаимодействии с разбавленной с ерной кислотой образуется сульфат калия, сероводород и вода:
2.2.3. Реагируя с азотной кислотой калий образует нитрат калия, можно образовать газ оксид азота (II), газ оксид азота (I), газ азот и воду.
2.2.4. В результате реакции насыщенной сероводородной кислоты и калия в бензоле образуется осадок гидросульфид калия и газ водород:
2K + 2H2S = 2KHS↓ + H2↑
2.4. Калий может взаимодействовать с гидроксидами:
2K + 2KOH = 2K2O + H2
Калий
Серебристо-белый мягкий металл
39,0983 а. е. м. (г/моль)
418,5 (4,34) кДж/моль (эВ)
Калий — элемент главной подгруппы первой группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 19. Обозначается символом K (лат. Kalium). Простое вещество калий (CAS-номер: 7440-09-7) — мягкий щелочной металл серебристо-белого цвета. В природе калий встречается только в соединениях с другими элементами, например, в морской воде, а также во многих минералах. Он очень быстро окисляется на воздухе и очень легко вступает в химические реакции, особенно с водой, образуя щёлочь. Во многих отношениях химические свойства калия очень близки к натрию, но с точки зрения биологической функции и использования их клетками живых организмов они все же отличаются. История и происхождение названия калий
Калий (точнее, его соединения) использовался с давних времён. Так, производство поташа (который применялся как моющее средство) существовало уже в XI веке. Золу, образующуюся при сжигании соломы или древесины, обрабатывали водой, а полученный раствор (щёлок) после фильтрования выпаривали. Сухой остаток, помимо карбоната калия, содержал сульфат калия K2SO4, соду и хлорид калия KCl.
Присутствие в природе калия
В свободном состоянии не встречается. Калий входит в состав сильвинита KCl·NaCl, карналлита KCl·MgCl2·6H2O, каинита KCl·MgSO4·6H2O, а также присутствует в золе некоторых растений в виде карбоната K2CO3 (поташ). Калий входит в состав всех клеток (см. ниже раздел Биологическая роль).
Калий — получение калия
Калий, как и другие щелочные металлы, получают электролизом расплавленных хлоридов или щелочей. Так как хлориды имеют более высокую температуру плавления (600—650 °C), то чаще проводят электролиз расправленных щелочей с добавкой к ним соды или поташа (до 12 %). При электролизе расплавленных хлоридов на катоде выделяется расплавленный калий, а на аноде — хлор:
K + + e − → K
2Cl − − 2e − → Cl2
При электролизе щелочей на катоде также выделяется расплавленный калий, а на аноде — кислород:
4OH − − 4e − → 2H2O + O2
Вода из расплава быстро испаряется. Чтобы калий не взаимодействовал с хлором или кислородом, катод изготовляют из меди и над ним помещают медный цилиндр. Образовавшийся калий в расплавленном виде собирается в цилиндре. Анод изготовляют также в виде цилиндра из никеля (при электролизе щелочей) либо из графита (при электролизе хлоридов).
Физические свойства калия
Калий — серебристое вещество с характерным блеском на свежеобразованной поверхности. Очень лёгок и легкоплавок. Относительно хорошо растворяется в ртути, образуя амальгамы. Будучи внесённым в пламя горелки калий (а также его соединения) окрашивает пламя в характерный розово-фиолетовый цвет.
Химические свойства калия
Калий, как и другие щелочные металлы, проявляет типичные металлические свойства и очень химически активен, легко отдаёт электроны.
Является сильным восстановителем. Он настолько активно соединяется с кислородом, что образуется не оксид, а супероксид калия KO2 (или K2O4). При нагревании в атмосфере водорода образуется гидрид калия KH. Хорошо взаимодействует со всеми неметаллами, образуя галогениды, сульфиды, нитриды, фосфиды и т. д., а также со сложными веществами, такими как вода (реакция проходит со взрывом), различные оксиды и соли. В этом случае они восстанавливают другие металлы до свободного состояния.
Калий хранят под слоем керосина.
Оксиды калия и пероксиды калия
При взаимодействии калия с кислородом воздуха образуется не оксид, а пероксид и супероксид:
Оксид калия может быть получен при нагревании металла до температуры не выше 180 °C в среде, содержащей очень мало кислорода, или при нагревании смеси супероксида калия с металлическим калием:
Оксиды калия обладают ярко выраженными основными свойствами, бурно реагируют с водой, кислотами и кислотными оксидами. Практического значения они не имеют. Пероксиды представляют собой желтовато-белые порошки, которые, хорошо растворяясь в воде, образуют щёлочи и пероксид водорода:
Свойство обменивать углекислый газ на кислород используется в изолирующих противогазах и на подводных лодках. В качестве поглотителя используют эквимолярную смесь супероксида калия и пероксида натрия. Если смесь не эквимолярна, то в случае избытка пероксида натрия поглотится больше газа, чем выделится (при поглощении двух объёмов CO2 выделяется один объём O2), и давление в замкнутом пространстве упадёт, а в случае избытка супероксида калия (при поглощении двух объёмов CO2 выделяется три объёма O2) выделяется больше газа, чем поглотится, и давление повысится.
В случае эквимолярной смеси (Na2O2:K2O4 = 1:1) объёмы поглощаемого и выделяемого газов будут равны (при поглощении четырёх объёмов CO2 выделяется четыре объёма O2).
Пероксиды являются сильными окислителями, поэтому их применяют для отбеливания тканей в текстильной промышленности.
Получают пероксиды прокаливанием металлов на воздухе, освобождённом от углекислого газа.
Гидроксиды калия
Гидроксид калия (или едкое кали) представляет собой твёрдые белые непрозрачные, очень гигроскопичные кристаллы, плавящиеся при температуре 360 °C. Гидроксид калия относится к щелочам. Он хорошо растворяется в воде с выделением большого количества тепла. Растворимость едкого калия при 20 °C в 100 г воды составляет 112 г.
Реакции, взаимодействие калия. Уравнения реакции калия с веществами
Реакции, взаимодействие калия. Уравнения реакции калия с веществами.
Калий реагирует, взаимодействует с неметаллами, металлами, полуметаллами, оксидами, кислотами, гидроксидами, солями, органическими соединениями и пр. веществами.
Реакции, взаимодействие калия с неметаллами. Уравнения реакции:
1. Реакция взаимодействия калия и кислорода:
2. Реакция взаимодействия калия и селена:
2K + Se → K2Se (t = 100-200 °C).
Реакция взаимодействия калия и селена происходит с образованием селенида калия.
3. Реакция взаимодействия калия и серы:
2K + S → K2S (t = 100-200 °C).
Реакция взаимодействия калия и серы происходит с образованием сульфида калия.
4. Реакция взаимодействия калия и кремния:
Реакция взаимодействия кремния и калия происходит с образованием силицида калия. Реакция протекает при сплавлении реакционной смеси.
5. Реакция взаимодействия калия и красного фосфора:
3K + P → K3P (t = 200 °C).
Реакция взаимодействия калия и красного фосфора происходит с образованием фосфида калия. Реакция протекает в атмосфере аргона.
6. Реакция взаимодействия калия и хлора:
Реакция взаимодействия калия и хлора происходит с образованием хлорида калия. Реакция протекает при комнатной температуре.
7. Реакция взаимодействия калия и водорода:
2K + H2 → 2KH (t = 200-350 °C).
Реакция взаимодействия калия и водорода происходит с образованием гидрида калия.
8. Реакция взаимодействия калия и брома:
Реакция взаимодействия калия и брома происходит с образованием бромида калия.
9. Реакция взаимодействия калия и иода:
Реакция взаимодействия йода и калия происходит с образованием иодида калия.
10. Реакция взаимодействия калия и фтора:
Реакция взаимодействия фтора и калия происходит с образованием фторида калия. Реакция протекает при комнатной температуре.
11. Реакция взаимодействия калия, кислорода и воды:
Реакция взаимодействия калия, кислорода и воды происходит с образованием гидроксида калия.
Реакции, взаимодействие калия с металлами и полуметаллами. Уравнения реакции:
1. Реакция взаимодействия калия и сурьмы:
Реакция взаимодействия калия и сурьмы происходит с образованием стибида калия. Реакция протекает при сплавлении реакционной смеси.
2. Реакция взаимодействия калия и теллура:
2K + Te → K2Te (t = 100-200 °C).
Реакция взаимодействия калия и теллура происходит с образованием теллурида калия.
3. Взаимодействие натрия и калия:
При сплавлении натрия и калия образуется жидкий натрий-калиевый сплав – NaK.
Реакции, взаимодействие калия с оксидами. Уравнения реакции:
1. Реакция взаимодействия калия и воды:
Реакция взаимодействия калия и воды происходит с образованием гидроксида калия и водорода. Реакция протекает бурно.
2. Реакция взаимодействия калия и оксида кремния:
Реакция взаимодействия калия и оксида кремния происходит с образованием кремния и силиката калия.
3. Реакция взаимодействия калия и оксида углерода:
Реакция взаимодействия калия и оксида углерода происходит с образованием углерода и карбоната калия.
4. Реакция взаимодействия калия и оксида бора:
Реакция взаимодействия калия и оксида бора происходит с образованием бора и метабората калия.
5. Реакция взаимодействия калия и оксида ванадия (III):
Реакция взаимодействия калия и оксида ванадия (III) происходит с образованием оксида ванадия (II) и пероксида калия.
Реакции, взаимодействие калия с гидроксидами. Уравнения реакции:
1. Реакция взаимодействия калия и гидроксида натрия :
NaOH + K → KOH + Na (t = 380-450 °C).
Реакция взаимодействия гидроксида натрия и калия происходит с образованием гидроксида калия и натрия.
2. Реакция взаимодействия калия и гидроксида калия :
2K + 2KOH → 2K2O + H2 (t = 450 °C).
Реакция взаимодействия калия и гидроксида калия происходит с образованием оксида калия и водорода.
Реакции, взаимодействие калия с солями. Уравнения реакции:
1. Реакция взаимодействия калия и хлорида ниобия:
NbCl5 + 5K → Nb + 5KCl.
Реакция взаимодействия хлорида ниобия и калия происходит с образованием калия и хлорида ниобия.
2. Реакция взаимодействия калия и фторида кремния:
SiF4 + 4K → Si + 4KF (t = 500 °C).
Реакция взаимодействия фторида кремния и калия происходит с образованием кремния и фторида калия.
3. Реакция взаимодействия калия и хлорида кремния:
SiCl4 + 4K → Si + 4KCl (t = 600-700 °C).
Реакция взаимодействия хлорида кремния и калия происходит с образованием кремния и хлорида калия.
4. Реакция взаимодействия калия и бромида кремния:
SiBr4 + 4K → Si + 4KBr (t = 100-150 °C).
Реакция взаимодействия бромида кремния и калия происходит с образованием кремния и бромида калия.
5. Реакция взаимодействия калия и хлорида иттрия:
Реакции, взаимодействие калия с кислотами. Уравнения реакции:
1. Реакция взаимодействия калия и ортофосфорной кислоты:
6K + 2H₃PO₄ → 2K₃PO₄ + 3H₂.
Аналогичные реакции протекают и с другими минеральными кислотами.
Реакции, взаимодействие калия с водородосодержащими соединениями. Уравнения реакции:
1. Реакция взаимодействия калия и сероводорода :
Аналогичные реакции протекают и с другими водородосодержащими соединениями.
Реакции, взаимодействие калия с органическими соединениями. Уравнения реакции:
1. Реакция взаимодействия калия и этанола:
Реакция взаимодействия калия и этанола происходит с образованием этанолята калия и водорода. Реакция протекает при комнатной температуре.
2. Реакция взаимодействия калия с другими органическими соединениями:
Калий реагирует также со спиртами, фенолами, карбоновыми кислотами с образованием солей.
Примечание: © Фото https://www.pexels.com, https://pixabay.com
Мировая экономика
Справочники
Востребованные технологии
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Свойства калия и его взаимодействие с водой
Почему его нельзя хранить на открытом воздухе
Калий — девятнадцатый элемент периодической таблицы Менделеева, относится к щелочным металлам. Это простое вещество, которое при нормальных условиях пребывает в твердом агрегатном состоянии. Закипает калий при температуре 761 °С. Температура плавления элемента — 63 °С. Калий имеет серебристо-белую окраску с металлическим блеском.
Химические свойства калия
Калий — элемент, обладающий высокой химической активностью, поэтому его нельзя хранить на открытом воздухе: щелочной металл моментально вступает в реакцию с окружающими веществами. Этот химический элемент относится к I группе и IV периоду таблицы Менделеева. Калий обладает всеми характерными для металлов свойствами.
Он взаимодействует с простыми веществами, к которым относятся галогены (бром, хлор, фтор, иод) и фосфор, сера, азот и кислород. Взаимодействие калия с кислородом называется окислением. В течение этой химической реакции кислород и калий расходуются в молярном соотношении 4:1, в результате чего образуется оксид калия в количестве двух частей. Такое взаимодействие можно выразить уравнением реакции:
Во время горения калия наблюдается пламя ярко-фиолетового цвета.
Такое взаимодействие считается качественной реакцией на определение калия. Реакции калия с галогенами называются в соответствии с названиями химических элементов: это фторирование, иодирование, бромирование, хлорирование. Такие взаимодействия являются реакциями присоединения. Пример — реакция между калием и хлором, в результате которой образуется хлорид калия. Для проведения такого взаимодействия берут два моля калия и один моль хлора. В результате образуется два моля калия:
При горении на открытом воздухе калий и азот расходуются в молярном соотношении 6:1. В результате такого взаимодействия образуется нитрид калия в количестве двух частей:
Соединение представляет собой кристаллы зелено-черного цвета. С фосфором калий реагирует по такому же принципу. Если взять 3 моля калия и 1 моль фосфора, получится 1 моль фосфида:
Калий реагирует с водородом, образуя гидрид:
Все реакции присоединения происходят при высоких температурах
Взаимодействие калия со сложными веществами
К сложным веществам, с которыми вступает в реакцию калий, относятся вода, соли, кислоты и оксиды. Так как калий — активный металл, он вытесняет атомы водорода из их соединений. Пример — реакция, происходящая между калием и соляной кислотой. Для ее проведения берется по 2 моля калия и кислоты. В результате реакции образуется 2 моля хлорида калия и 1 моль водорода:
Более детально стоит рассмотреть процесс взаимодействия калия с водой. Калий бурно взаимодействует с водой. Он движется по поверхности воды, его подталкивает выделяющийся водород:
В ходе реакции в единицу времени выделяется много тепла, что приводит к воспламенению калия и выделяющегося водорода. Это очень интересный процесс: при контакте с водой калий мгновенно воспламеняется, фиолетовое пламя потрескивает и быстро передвигается по поверхности воды. В конце реакции происходит вспышка с разбрызгиванием капель горящего калия и продуктов реакции.
Основной конечный продукт реакции калия с водой — гидроксид калия (щелочь). Уравнение реакции калия с водой:
Внимание! Не пытайтесь повторить этот опыт самостоятельно!
При неправильном проведении эксперимента можно получить ожог щелочью. Для реакции обычно используют кристаллизатор с водой, в который помещают кусочек калия. Как только водород прекращает горение, многие хотят заглянуть в кристаллизатор. В этот момент происходит завершающая стадия реакции калия с водой, сопровождающаяся слабым взрывом и разбрызгиванием образовавшейся горячей щелочи. Поэтому в целях безопасности стоит держаться на некотором расстоянии от лабораторного стола, пока реакция не завершится полностью. Здесь вы найдете самые зрелищные опыты, которые можно проводить с детьми дома.
Строение калия
Атом калия состоит из ядра, в котором содержатся протоны и нейтроны, и электронов, вращающихся вокруг него. Количество электронов всегда равно количеству протонов, находящихся внутри ядра. При отсоединении электрона или при присоединении к атому он перестает быть нейтральным и превращается в ион. Ионы делятся на катионы и анионы. Катионы обладают положительным зарядом, анионы — отрицательным. При присоединении к атому электрона он превращается в анион; если же один из электронов покидает свою орбиту, нейтральный атом превращается в катион.
Порядковый номер калия в периодической таблице Менделеева — 19. Значит, протонов в ядре химического элемента находится тоже 19. Вывод: электронов вокруг ядра расположено 19. Количество протонов в структуре атома определяется так: от атомной массы отнять порядковый номер химического элемента. Вывод: в ядре калия находится 20 протонов. Калий принадлежит к IV периоду, имеет 4 «орбиты», на которых равномерно располагаются электроны, пребывающие в постоянном движении. На первой «орбите» расположены 2 электрона, на второй — 8; на третьей и на последней, четвертой «орбите», вращается 1 электрон. Этим объясняется высокий уровень химической активности калия: его последняя «орбита» не заполнена полностью, поэтому элемент стремится соединиться с другими атомами. В результате электроны последних орбит двух элементов станут общими.