митоз флюоресценция что изображено зеленым
Флуоресцентные белки: разнообразнее, чем вы думали!
«Флуоресцентные бéлки в клетке»
Автор
Редакторы
При упоминании флуоресцентных белков люди чаще всего представляют себе разноцветные клетки, забавные рисунки бактериями на чашках Петри, в крайнем случае, целые флуоресцирующие организмы — от медуз до кошек, — эдакая цветная палитра. Однако область применения этого замечательного инструмента расширяется с каждым годом, — как и разнообразие самих белков. В этой статье мы поговорим о новых поколениях флуоресцентных белков и рассмотрим некоторые интересные методы на их основе.
— Ой, я и не знала, что коты такие умные бывают.
Я думала, они только на деревьях кричать умеют.
— Подумаешь, я еще и вышивать могу. и на машинке тоже.
«Трое из Простоквашино».
Светящиеся белки из забавного явления довольно быстро превратились в ценный объект для науки, когда были созданы флуоресцентные микроскопы. (Флуоресцентная микроскопия — это метод получения увеличенного изображения с использованием люминесценции возбуждённых атомов и молекул образца. Подробнее о разных видах микроскопий можно прочитать в статьях «“Нарисуем” живую клетку» [27] и «Лучше один раз увидеть, или микроскопия сверхвысокого разрешения» [28].)
Оказалось, что родоначальник большинства используемых белков — зеленый флуоресцентный белок (GFP) из медузы Aequorea victoria (подробнее о его замечательной судьбе — в статье «Флуоресцирующая Нобелевская премия по химии» [29]), — равно как и его гомологи из различных морских животных, являются прекрасными маркерами для визуализации живых клеток и организмов.
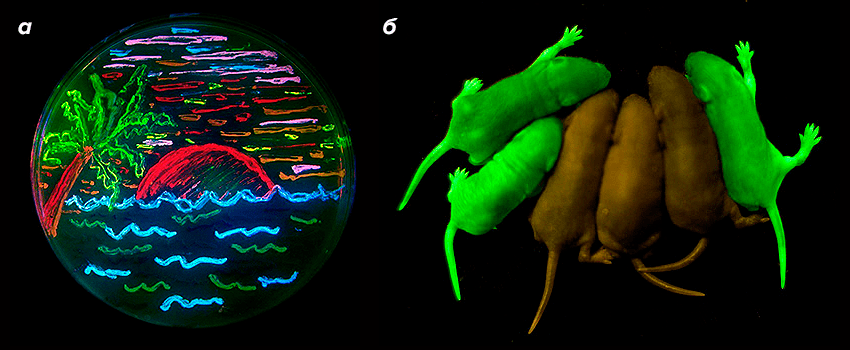
Главной особенностью флуоресцентных белков является способность формировать флуорофорную группу автокаталитически, без привлечения внешних кофакторов и ферментов — другими словами, они могут светиться внутри клетки сами по себе. Независимое созревание, в сочетании с низкой токсичностью и высокой стабильностью, позволяет использовать флуоресцентные белки в самых разных организмах, в которых исходно они не синтезировались (рис. 1).
Рисунок 1. Флуоресцентное «творчество». а — «Рисунок» бактериями, экспрессирующими гены различных флуоресцентных белков, на чашке петри. б — Мыши, несущие ген зеленого флуоресцентного белка, и обычные мыши.
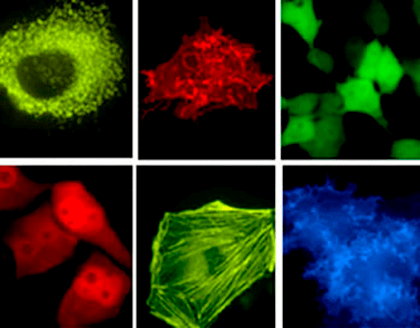
Рисунок 2. Визуализация различных компонент живых клеток с помощью флуоресцентных белков
Сейчас ученые используют GFP и его варианты и гомологи во многих методах для изучения организации и функционирования живых систем. Флуоресцентные белки, слитые в одной рамке считывания с интересующими белками, позволяют наблюдать за их локализацией, передвижением, оборотом и даже «старением» (т.е. временем, прошедшим после белкового синтеза). Нуклеиновые кислоты тоже могут быть помечены — с помощью РНК- или ДНК-связывающих белковых доменов.
Многие лаборатории сосредотачивают свои усилия на идентификации и создании флуоресцентных белков с новыми характеристиками и улучшенными свойствами: разнообразие существующих в настоящее время белков покрывает практически весь видимый спектр. В этой статье мы поговорим о новых поколениях флуоресцентных белков и рассмотрим некоторые интересные способы их применения, выходящие за рамки методики слияния GFP-подобного белка с интересующим объектом, — и последующего наблюдения за локализацией этого объекта с помощью микроскопа (рис. 2).
«Светящий теплом»
В настоящее время существует целая «палитра» белков, родственных знаменитому GFP, — от синих до дальнекрасных. Однако, флуоресцентные белки, принадлежащие другим крупным семействам, тоже довольно широко распространены.
iRFP — белок, флуоресцирующий не в видимой области спектра, а в инфракрасной (фактически, «отвечающий на свет теплом»), — был получен в 2011 году [1]. Его максимум поглощения находится в дальнекрасной области спектра (690 нм), а пик флуоресценции — в инфракрасной (713 нм). iRFP был получен на основе фитохрома из бактерии Rhodopseudomonas palustris (фитохромы — это фоточувствительные рецепторы с довольно консервативным белковым ядром, к которому нековалентно присоединяется тетрапиррольный хромофор). Из двух доменов фитохрома, скорректированных вдобавок точечными мутациями, и был создан iRFP.
Преимущество бактериофитохромов заключается в том, что их кофактор (например, биливердин) участвует в нормальном метаболизме гема млекопитающих. Визуализация различных процессов в этих организмах in vivo важна для таких задач как количественная и неинвазивная оценка роста и метастазирования опухоли, изучение экспрессии генов, отслеживание бактериальной инфекции и т.д. Вкратце, — можно наблюдать за этими процессами, поместив флуоресцентный белок под определенный промотор, который активируется только в конкретных условиях, или в опухолевые клетки; тогда регистрация сигнала от белка будет означать, что промотор активен, или что клетки трансформировались, или что определенный молекулярный путь запустился.
Визуализация глубоких тканей с помощью GFP-подобных белков, к сожалению, сильно затруднена из-за сильного поглощения света гемоглобином и меланином кожи. Оптимальный флуоресцентный белок для имиджинга in vivo должен обладать максимумами поглощения и флуоресценции в дальнекрасной-инфракрасной области, в которой поглощение света тканью минимально; таким образом, iRFP удовлетворяет данным условиям.
Помимо спектра, полностью подходящего для данных задач, iRFP отличается высокой внутриклеточной стабильностью и низкой цитотоксичностью. В совокупности с отсутствием необходимости добавления извне биливердинового хромофора, iRFP является отличным кандидатом для работы с млекопитающими in vivo, что уже было показано учеными нескольких стран. Группа Верхуши локализовала его в мышиной печени; Лю и др. изучали с помощью iRFP рак простаты (тоже на мышах) [2], а Хок и др. количественно оценивали рост опухоли in vivo [3]. Скорее всего, в ближайшее время будут разработаны и другие методики изучения различных клеточных процессов, использующие iRFP в своей основе.
Когда цвет один, но это не проблема
Несмотря на богатство палитры флуоресцентных белков, бывает так, что ее не хватает, — например, когда ученым необходимо отслеживать множество одновременно происходящих процессов (как в методике Brainbow), или когда те или иные каналы по каким-либо причинам использовать нельзя.
Для этого случая существует особая методика, которая позволяет различать объекты, помеченные разными белками одного цвета. Дело в том, что даже если максимумы флуоресценции двух белков близки и попадают в одну и ту же полосу пропускания фильтра на микроскопе, можно выбрать другое свойство, по которому они существенно различаются. Одно из таких часто используемых свойств — время жизни флуоресценции. Время жизни — это средний период времени, в течение которого флуорофор находится в возбужденном состоянии. Грубо говоря, после поглощения фотона один белок переизлучит другой фотон в среднем через меньшее время, а другой — через большее.
С помощью FLIM (Fluorescence lifetime imaging microscopy — микроскопии времени жизни флуоресценции) можно проследить за каждым фотоном, который будет выпущен образцом, и построить кривую зависимости количества испускаемых фотонов от времени. Поскольку время жизни флуоресценции флуорофора (τ) зависит от его непосредственного молекулярного окружения, технологию FLIM используют в клеточной биологии для измерения физиологических параметров в клетке, например, клеточного pH, концентраций ионов и мембранного потенциала [4], [5].
В настоящий момент главное применение FLIM заключается в измерении белок-белковых взаимодействий с помощью Фёрстеровского резонансного переноса энергии (FRET; см. «Рулетка для спектроскописта» [30]) между двумя флуоресцентно-меченными белками (поскольку присутствие акцептора влияет на время жизни флуоресценции донора) [6].
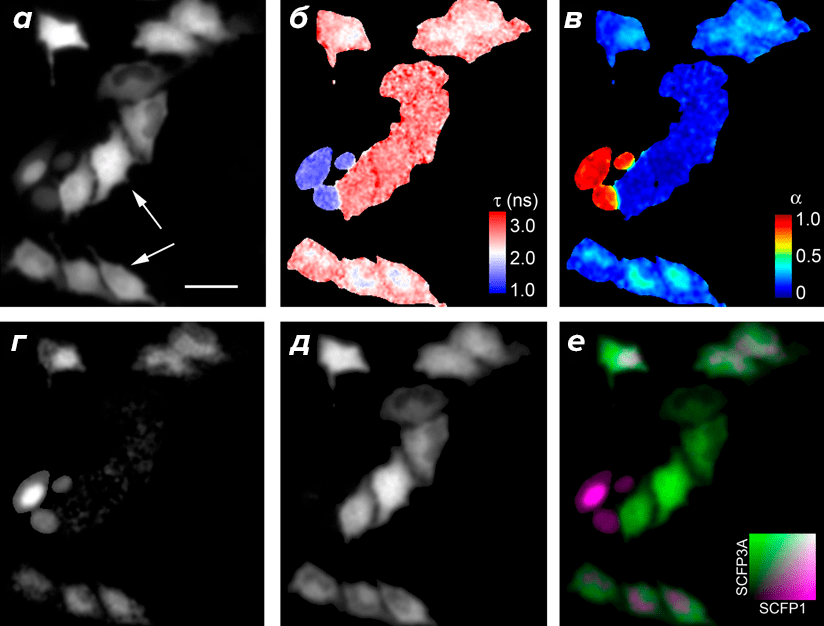
Кроме исследования изменений времени жизни одной конкретной метки, FLIM также начали использовать для количественного отображения пространственного и фракционного распределения двух невзаимодействующих флуоресцентных меток с разными временами жизни. В идеальном случае затухание флуоресценции моноэкспоненциально; в такой ситуации возможно различить два или три белка с известными временами жизни флуоресценции, математически проанализировав полученную кривую и разделив ее на пики, соответствующие каждому из образцов. После этого с помощью компьютерных программ каждый из белков можно покрасить в свой псевдоцвет, для облегчения визуального восприятия (рис. 3).
Рисунок 3. Белки SCFP1 и SCFP3A, отличающиеся временем жизни флуоресценции, в клетках HeLa. а — Флуоресцентная микрофотография клеток, экспрессирующих SCFP1-NLS и SCFP3A-NES — или только SCFP1-NLS. Стрелки указывают на клетки, которые нельзя различить по распределению флуоресценции. б — Карта времени жизни флуоресценции. в — Карта фракционного вклада SCFP1 во флуоресценцию в стационарном состоянии. г и д — Микроснимки фракционного молярного распределения SCFP1-NLS и SCFP3A-NES, соответственно. е — Наложение г и д, где SCFP1-NLS окрашен фиолетовым, а SCFP3A-NES — зеленым.
Флуоресцентные таймеры
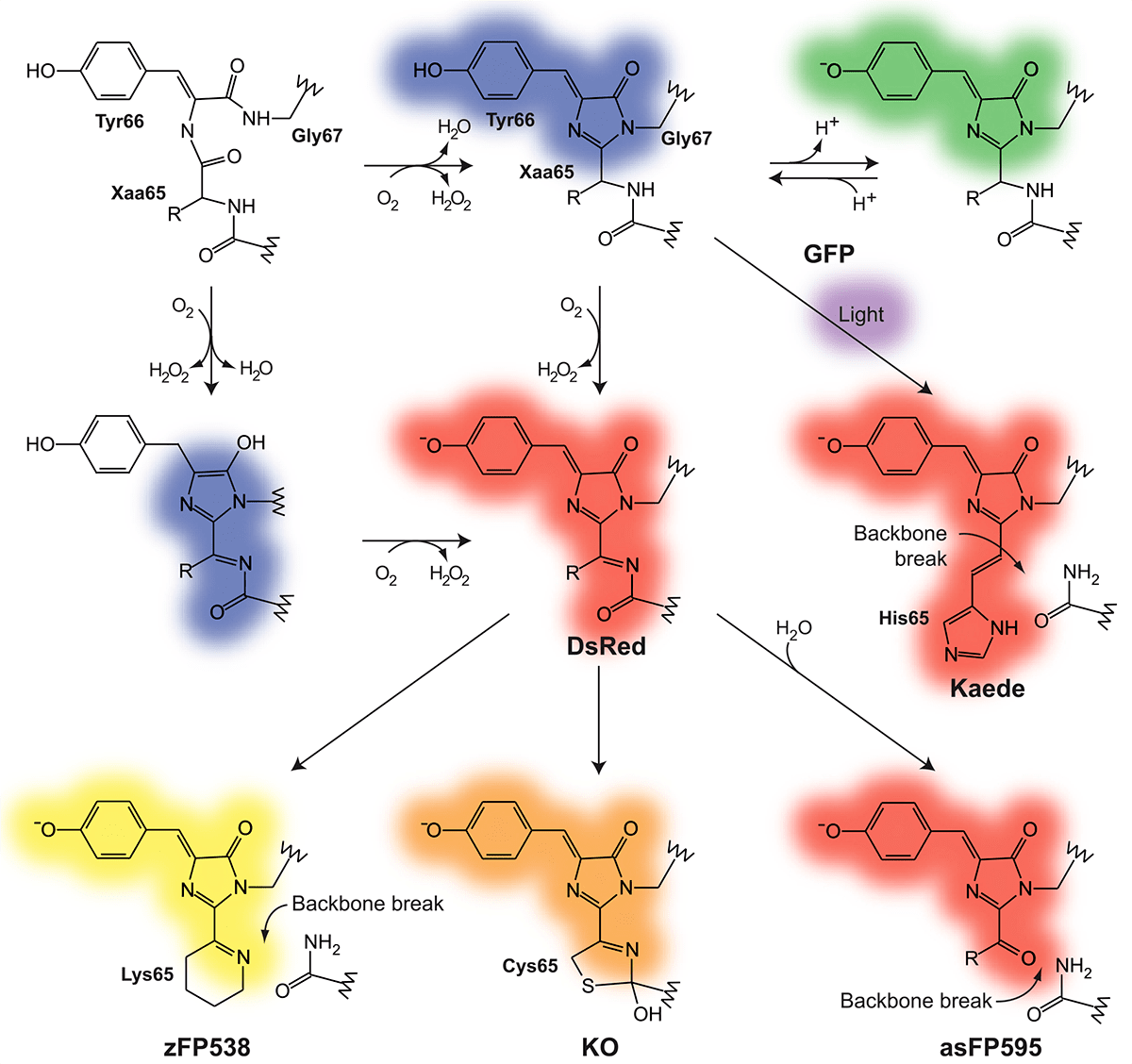
Белки начинают флуоресцировать после укладки белковой цепи и созревания хромофора, которое включает несколько последовательных ковалентных модификаций, занимающих довольно много времени, особенно у оранжевых и красных белков (рис. 4) [7]. Обычно именно стадия созревания хромофора является лимитирующей для того, чтобы белок начал флуоресцировать. В зависимости от вида флуоресцентного белка, концентрации кислорода и температуры фолдинг может длиться от нескольких минут до целых дней, как в случае флуоресцентных таймеров.
Рисунок 4. Химические структуры и пути созревания хромофоров GFP-подобных белков, встречающихся в природе
Для практического использования скорость созревания до яркого и стабильного флуоресцентного сигнала должна быть достаточно большой. У большей части флуоресцентных белков время полусозревания длится от
40 минут до 1–2 часов, что достаточно для мечения клеток, органелл и интересующих белков — и для различных количественных экспериментов. Впрочем, для некоторых особых применений (например, для ранней регистрации активации промоторов, мечения интересующих белков с коротким временем жизни или наблюдения за единичными актами трансляции) необходимы флуоресцентные белки с очень высокой скоростью фолдинга. Например, быстро созревающие желтые флуоресцентные белки позволяют напрямую наблюдать за продукцией единичной молекулы белка в реальном времени [8].
Целый ряд возможностей, которые и по сей день изучены в недостаточной степени, обеспечивается так называемыми флуоресцентными таймерами — белками, которые меняют цвет флуоресценции в течение жизни, таким образом позволяя определить время их экспрессии в ретроспективе. Что важно, различные флуоресцентные таймеры характеризуются разнообразными скоростями фолдинга — от минут до часов и даже дней — и таким образом, подходят для изучения процессов по различным временным шкалам.
Первый флуоресцентный таймер DsRed-E5 был опубликован в 2000 году [9]. В течение нескольких часов после синтеза DsRed-E5 обладает флуоресценцией в зеленой области спектра, но потом превращается в красную форму (рис. 5). Эти изменения происходят благодаря тому, что некоторые хромофоры в тетрамере созревают в зеленую GFP-подобную форму вместо красной, и их зеленая флуоресценция доминирует, пока более медленно созревающие красные хромофоры не появятся и не «украдут» возбуждающую энергию от зеленых с помощью крайне эффективного внутритетрамерного Фёрстеровского переноса энергии (FRET) [10].
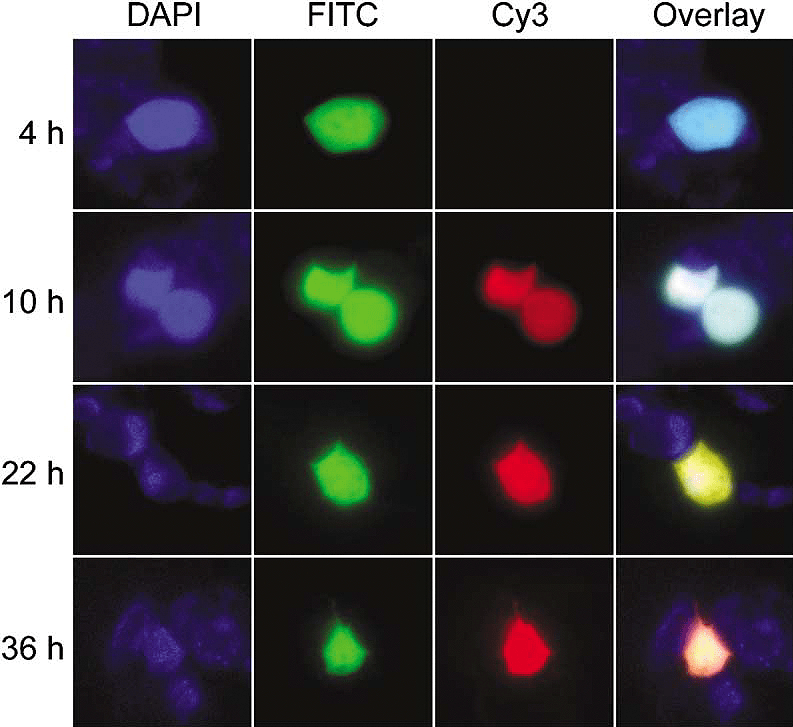
Рисунок 5. Визуализация цветов эмиссии флуоресцентного таймера DsRed-E5NA после индукции в системе Tet-On в человеческих клетках HEK293. В качестве контрольного белка использовали DAPI, а наблюдали за изменением соотноше-ния зеленого к красному сигналов (каналы FITC и Cy3 соответственно).
Таким образом, ткани, клетки или органеллы, которые окрашены зеленым, означают недавнюю продукцию DsRed-E5, в то время как красная флуоресценция отмечает области, в которых белок был синтезирован по крайней мере несколько часов назад. Отношение интенсивности красной флуоресценции к зеленой пропорционально возрасту синтезированного белка и таким образом может отмечать время, прошедшее с момента активации соответствующего промотора. На практике, это обеспечивает способ наблюдения за динамикой экспрессии генов в различных тканях [11]; позволяет отделить клетки, в которых промотор недавно активировался, от клеток с постоянной активностью данного промотора [12]; кроме того, с помощью такого таймера можно анализировать распределение органелл в зависимости от возраста [13] и отслеживать перемещение белков [14].
Светом можно не только возбуждать, но и переключать!
Фотоактивируемые флуоресцентные белки (ФАФБ) представляют собой отдельный класс белков, чьи флуоресцентные свойства могут быть «включены» с помощью импульса света определенной длины волны. Возбуждаясь из несветящегося состояния или меняя цвет, ФАФБ могут служить селективными фотометками белков, органелл, клеток и тканей. В ходе эксперимента можно активировать конкретную фракцию ФАФБ, также как и выбрать когда — и определить интересующий регион. Активированные ФАФБ можно визуализировать в отдельном спектральном канале, при этом неактивированные молекулы остаются «невидимыми». Это свойство обеспечивает уникальную возможность для точного мечения и отслеживания интересующих объектов в живых системах, увеличивая соотношение сигнал/шум и для флуоресцентной микроскопии высокого разрешения.
Плотное окружение хромофора у GFP-подобных белков может стабилизировать его в различных конформациях и значительно влиять на его спектральные характеристики, определяя его состояние протонирования, коэффициент экстинкции и квантовый выход флуоресценции, также как и точное положение пиков возбуждения/эмиссии. Таким образом, цис-транс переходы хромофора, в сочетании с конформационными перестройками близлежащих аминокислот, могут привести к обратимым светоиндуцируемым фотоконверсиям, которые значительно меняют спектральные свойства данного белка.
Необратимые изменения спектральных характеристик становятся возможными, если энергия поглощенного протона приводит к химической реакции внутри конкретного флуоресцентного белка, — например, к расщеплению пептидной связи в хромофоре [15] или декарбоксилированию 222 глутаминовой кислоты, которая играет ключевую роль в сети водородных связей вокруг хромофора [16]. Кроме того, недавно были описаны необратимые фотоконверсии, которые случаются при определенных условиях у тех белков, которые ранее считались не фотоактивируемыми. В частности, описано окислительное покраснение практически для всех зеленых флуоресцентных белков [17]. При интенсивном или двухфотонном возбуждении происходит красная → зеленая или оранжевая → дальнекрасная фотоконверсия у белков DsRed, mKate, mKO и mOrange, механизм которой пока не изучен. Некоторым из этих конверсий в будущем может найтись практическое применение.
«Опасные» флуоресцентные белки.
В настоящее время активно развивается область флуоресцентных белков, которые под действием света испускают активные формы кислорода (АФК; о некоторых их интересных аспектах можно почитать в статье «Активный кислород: друг или враг, или о пользе и вреде антиоксидантов» [31]). АФК могут быть использованы для локальной инактивации целевых белков, избирательного снижения жизнеспособности клеток и для изучения внутриклеточной сигнализации активными формами кислорода. В данной статье я расскажу о двух таких белках: miniSOG и KillerRed.
MiniSOG
MiniSOG (mini Singlet Oxygen Generator) — фототоксичный зеленый флуоресцентный флавопротеин, примерно вдвое меньший по размеру, чем GFP (всего лишь 106 аминокислот), — был получен в результате точечных замен в LOV2-домене белка фототропина-2 из Arabidopsis [18]. Модифицированный LOV-домен, как и исходный (рецептор синего света), связывает флавинмононуклеотид, который, будучи возбужден синим светом, передает энергию триплетному кислороду, который превращается в более «опасный» синглетный кислород.
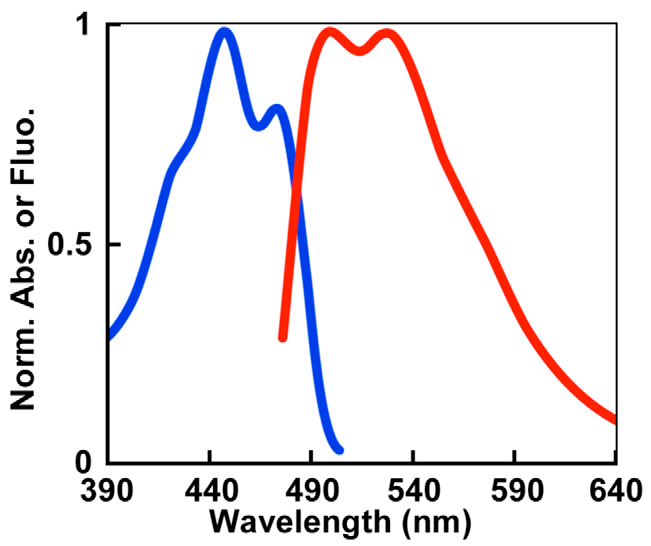
Максимальное поглощение происходит при длине волны 448 нм с плечом у 473 нм, т.е. в синем свете. Возбуждение miniSOG приводит к эмиссии зеленого света: два пика длиной волны 500 и 528 нм (рис. 6). MiniSOG в растворе ведет себя как мономерный белок, и в составе химерных белков не нарушает их локализации (рис. 7).
Рисунок 6. Спектры miniSOG. Спектр поглощения (синий) и эмиссии (красный) белка miniSOG.
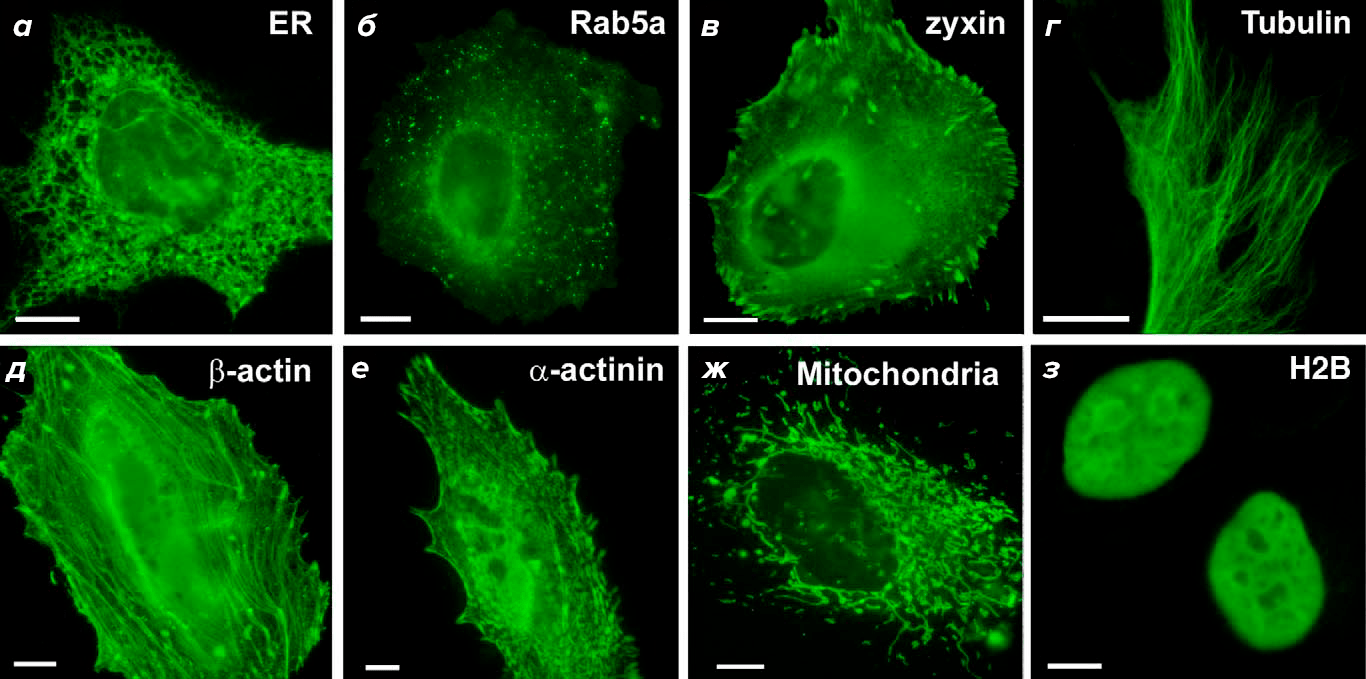
Рисунок 7. Полученные с помощью конфокальной микроскопии фотографии miniSOG в различных субклеточных локализациях: а — в эндоплазматическом ретикулуме; б — слитым с Rab5A; в — слитым с зиксином; г — слитым с тубулином; д — слитым с β-актином; е — слитым с α-актином; ж — в митохондрии; з — слитым с гистоном H2B.
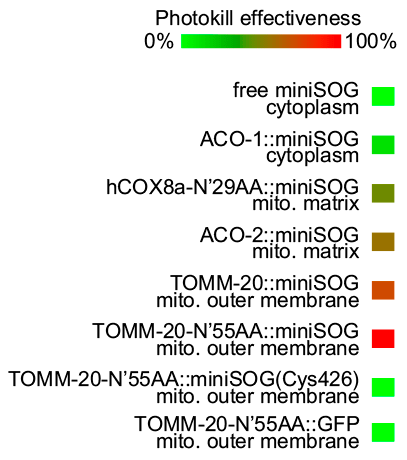
В темноте miniSOG не оказывает негативного влияния на клетки, однако на свету может вызывать токсический эффект вплоть до ее гибели, в зависимости от локализации (рис. 8) [19].
Рисунок 8. Токсический эффект miniSOG в зависимости от его локализации: ACO-1 — цитоплазматическая аконитаза; hCOX8a — субъединица 8а человеческой цитохром С оксидазы; ACO-2 — митохондриальная аконитаза; TOMM-20 — главный рецептор импорта полипептидов в митохондрию.
Однако, как показано выше, miniSOG при освещении отнюдь не всегда приводит к клеточной гибели; это указывает на возможность использования miniSOG не в качестве «орудия убийства», а как обычный источник синглетного кислорода. Подробнее о токсических свойствах miniSOG можно почитать в статье «Флуоресцентный белок miniSOG убивает клетки светом» [32].
KillerRed
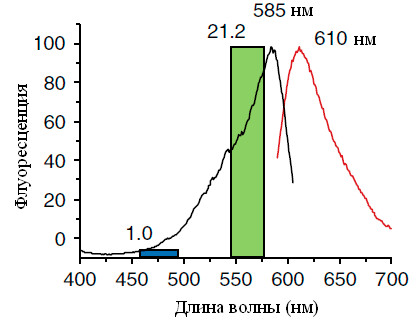
Рисунок 9. Спектры возбуждения (черная линия) и флуоресценции (красная линия) KillerRed. Синий и зеленый прямоугольники показывают относительный фототоксический эффект при облучении синим (460–490 нм) и зеленым (540–580 нм) светом мощностью 35 мВт/см 2 соответственно. Данные над прямоугольниками показывают количество раз, в которое уменьшилось число живых клеток E. coli после 30-минутного облучения.
KillerRed — фототоксичный димерный красный флуоресцентный мутант хромобелка anm2CP из гидроидной медузы (максимумы возбуждения и эмиссии — 585 и 610 нм, соответственно). Роль хромофора в определении фототоксических свойств была установлена с помощью теста на бактериях: он показал, что зеленый свет убивает клетки гораздо эффективнее синего. Эти результаты соответствуют спектру поглощения/возбуждения [20] (рис. 9).
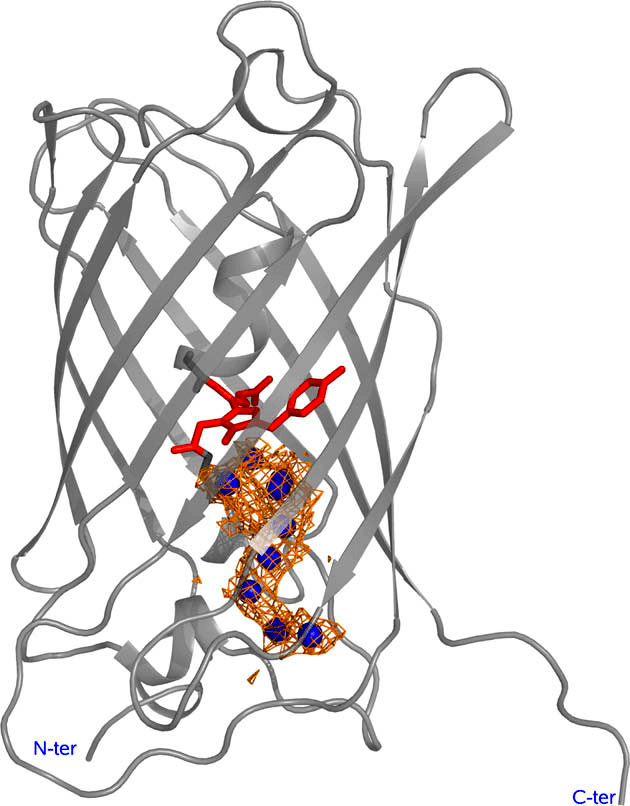
GFP и его гомологи является универсальными метками, которые могут быть слиты с целевыми белками, в том числе и ядерными, без влияния на жизнеспособность клетки. Благодаря чему наблюдается повышение фототоксических свойств KillerRed по сравнению с другими GFP-подобными белками? На данный момент нет точных объяснений этому феномену, но есть предположения, связанные со структурой белка KillerRed. Недавно полученное изображение высокого разрешения выявляет уникальный канал, соединяющий DsRed-подобный хромофор с внешней средой, в который помещается восемь молекул воды (рис. 10) [21].
Рисунок 10. Пространственная структура мономера KillerRed. Пептидный остов отмечен серым цветом, хромофор (Gln65—Tyr66—Gly67) — красным. Углубление, формирующее канал, показано в виде оранжевой сетки, охватывающей молекулы воды (синие сферы).
Исходя из данных анализа структуры, можно выдвинуть гипотезу о реакции кислорода с возбужденным хромофором, которая привела бы к образованию супероксид-анион-радикала (O2 •− ) [22]. Образование O2 •− может быть объяснено реакцией переноса электрона от хромофора к кислороду, оставляющей хромофор в состоянии радикала. Эта гипотеза подтверждается недавним открытием того факта, что флуоресцентные белки являются светоиндуцируемыми донорами электронов [17]. АФК, генерируемые KillerRed, могут затем реагировать со слитым с ним белком [23].
Эффективный фотосенсибилизатор должен защищать себя от АФК-опосредованного повреждения. Удивительная особенность KillerRed заключается в большом количестве серусодержащих остатков (6 цистеинов и 10 метионинов). Возможно, именно они играют роль в защите от фотоиндуцированного окисления.
Как уже было сказано ранее, KillerRed — димеризующийся белок; поэтому, будучи слитым с другими белками, он может приводить к потере их функциональности. Так, например, экспрессия химерного гена H2A—KillerRed даже без облучения приводит к утрате способности клеток делиться [24]. Для того чтобы избежать этой ситуации, используется тандемная версия KillerRed, содержащая две копии белка, соединенных гибким линкером. Для других димерных белков было показано, что в таком случае они формируют внутримолекулярные димеры и тем самым ведут себя как псевдомономерные метки [25], что подтвердилось и в данном случае [22].
Как и для других фотосенсибилизаторов, уровень фототоксичности и эффект белка KillerRed зависит от внутриклеточной локализации. KillerRed, слитый с сигналом направления в митохондрию, запускает апоптоз; будучи слитым с сигналом меристилирования, на плазматической мембране приводит, в основном, к некрозу [20]. Будучи слит с гистоном H2B, KillerRed при облучении вызывает активацию системы репарации клетки [22].
Совсем недавно, в 2013 году, с помощью нескольких точечных мутаций был получен мономерный вариант KillerRed (под названием SuperNova) [26]. Его цитоплазматическая экспрессия, как и экспрессия KillerRed, не мешает делению клеток, а уровень фототоксичности при этом довольно высок, что позволяет, в частности, функциональный анализ целевых белков с помощью технологии CALI (chromophore-assisted light-inactivation) без недостатка в виде димеризации, присущей исходному варианту KillerRed.
Безусловно, в своей статье я рассмотрела лишь небольшую часть возможностей применения флуоресцентных белков. В настоящее время это одна из наиболее динамично развивающихся областей молекулярной биологии как фундаментальной науки, с одной стороны, а с другой — как прикладной методологии. Флуоресцентные белки продолжают активно исследовать, благодаря чему они становятся все более технологичными инструментами как для самих исследований, так и для практического применения в биотехнологиях и медицине. Поиск и создание новых интересных форм и разнообразных методов, основанных на использовании флуоресцентных белков, наверняка приведут к неожиданным интригующим открытиям.
Цвет, 3D и сверхвысокое разрешение: новая разработка в микроскопии
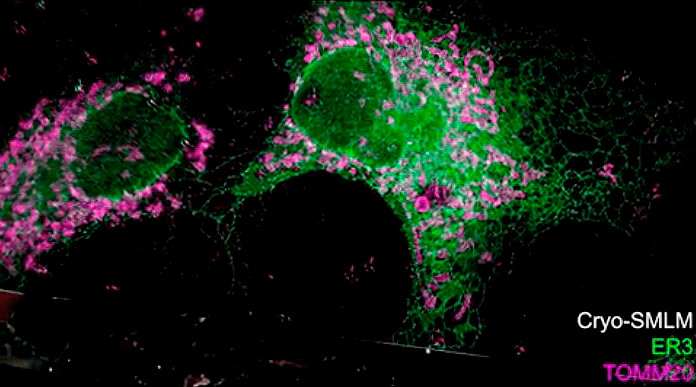
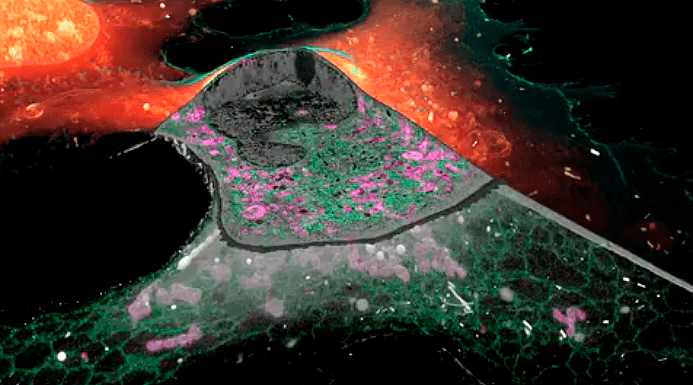
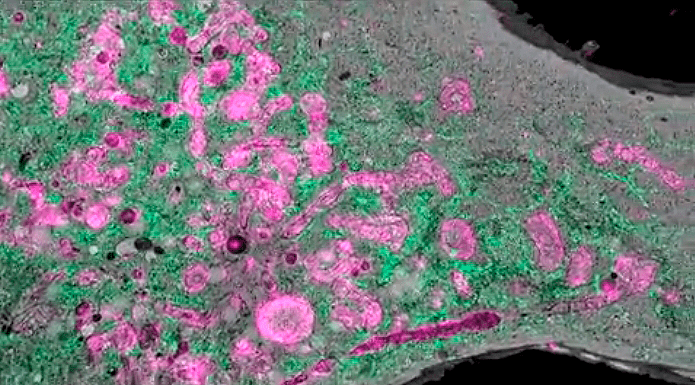
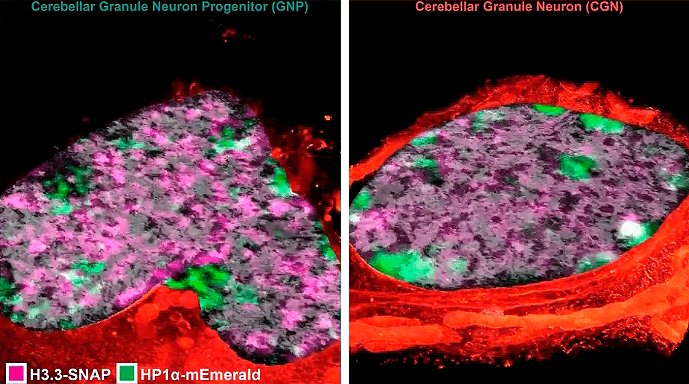
Заглавная иллюстрация из обсуждаемой статьи — коллаж из изображений, полученных авторами при помощи новой методики. По часовой стрелке, начиная с верхнего левого угла:
Автор
Редакторы
Недавно научный и околонаучный мир «взорвало» видео со сверхдетальным цветным трехмерным изображением межклеточных контактов в развивающихся нейронах. Такие контакты позволяют нейронам в процессе развития находить друг друга и организовываться в сети, благодаря которым мы испытываем радость, сочиняем стихи. или занимаемся наукой! В журнале Science ученые описали технологию получения таких изображений: как водится, в основу лег синтез. Исследователи соединили две самые передовые методики с помощью компьютерных технологий.
— Пусть они думают до утра. Пойдем к нам во двор.
У нас там все совсем другое. Будем гонять мяч,
настоящий, круглый, а не плоский.
И кошки у нас пушистые и мягкие.
— Я очень хочу играть в круглый мяч, — вздохнула
Анка. — Я очень хочу погладить пушистую кошку.
Но я не понимаю, что такое «круглый».
Наверное, я никогда не смогу увидеть круглое и пушистое!
Е. Велтистов. Приключения Электроника
Введение
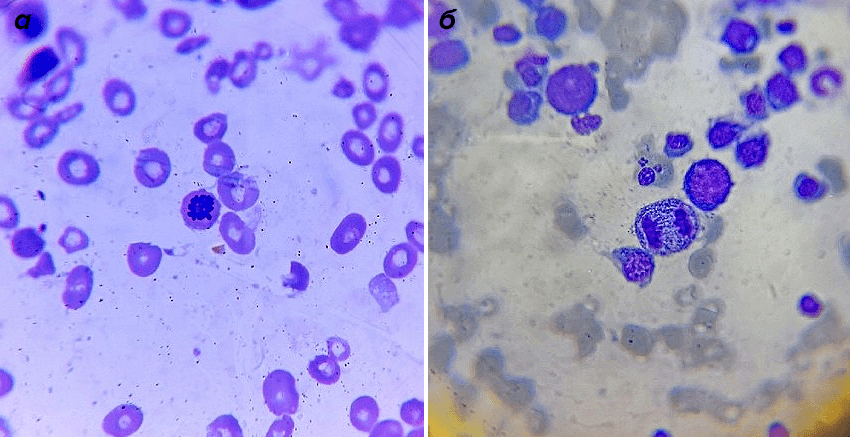
Все, кто когда-нибудь смотрел в обычный световой микроскоп, представляют себе эту картину: клетки выглядят плоскими, их можно рассмотреть лишь в общих чертах. Не видно митохондрий и лизосом, знакомых из школьных учебников, и даже деление клетки выглядит как череда размытых пятен и нитей (рис. 1).
Рисунок 1. Клетка костного мозга в профазе (а) и анафазе (б) митоза. Фотографии сделаны под световым микроскопом. Клетки человека сами прозрачны, цвета придают красители, которыми окрашен препарат.
собственное фото автора статьи
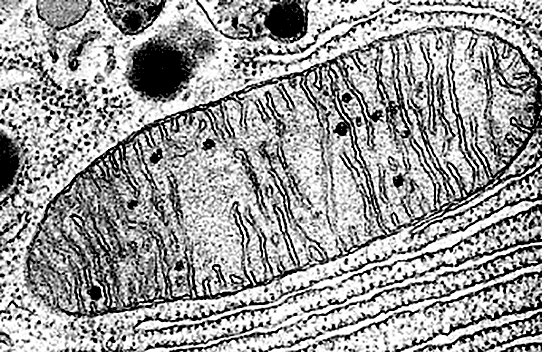
Электронная микроскопия позволяет рассмотреть куда более мелкие структуры. но при этом изображение всегда черно-белое (рис. 2а и 2б), иногда попадаются лишь искусственно раскрашенные картинки (рис. 2в).
Рисунок 2а. Митохондрия в просвечивающем электронном микроскопе (ПЭМ, англ. TEM). Электронный луч проходит сквозь образец, давая плоское черно-белое изображение.
Рисунок 2б. Домашняя пыль в сканирующем электронном микроскопе (СЭМ, англ. SEM). Изображения такого типа выглядят объемными, но такому микроскопу недоступна внутренняя часть объекта, он «видит» только его поверхность. И по-прежнему такие изображения черно-белые — не верьте тому, что увидите на рисунке 2в.
Рисунок 2в. Еще один снимок пыли в сканирующем электронном микроскопе. Он выглядит цветным лишь потому, что его искусственно раскрасили. Цвета здесь продиктованы только воображением художника или ученого. Какие они были «на самом деле» — мы не знаем.
А авторы недавно вышедшей статьи в Science представили научному миру потрясающую детализацию в цвете и 3D-формате [1]. Примеры их изображений можно увидеть на заглавной иллюстрации. Кстати, вот то самое видео — на нем можно в полной мере насладиться 3D-HD-микромиром:
Видео 1. Зернистые клетки мозжечка мыши, изображение которых получено с помощью новой методики. Вслед за авторами статьи заглядываем внутрь клеток и рассматриваем структуру контакта между ними – в цвете! Каждый цвет соответствует определенному белку.
Разработать такую технологию было совсем не просто — на пути у исследователей стояли фундаментальные физические ограничения. Обмануть физику стало возможно путем соединения в одной методике сразу нескольких передовых разработок, за две из которых даже была получена Нобелевская премия: в 2014 [2] и 2017 году [3].
Скучный черно-белый мир
Но почему так сложно? Почему нельзя просто увеличить изображение в обычном микроскопе с помощью очень сильных линз, чтобы разглядеть все до молекулы? Это невозможно в силу законов распространения света: в световом микроскопе любые две точки на расстоянии менее 0,2 мкм будут сливаться в одну. Такое ограничение и называется дифракционным пределом (физика этого явления рассмотрена в статье «12 методов в картинках: микроскопия» [4]).
Если использовать поток электронов вместо луча фотонов, то дифракционный предел будет намного меньше: на этом и основана электронная микроскопия. Но и она не панацея: слишком высоки требования к подготовке образца. Для электронного луча нужен вакуум, а значит, в вакууме должен быть и образец. А в вакууме вода вскипает при комнатной температуре (снова неумолимая физика!). Это означало бы моментальное разрушение образца — ведь цитоплазма клеток и содержимое органелл состоит большей частью из воды.
Чтобы этого избежать, для электронной микроскопии образцы обезвоживают, помещают в смолу и окрашивают. тяжелыми металлами! Да, я забыл сказать, что любые красители из нашего «фотонного» мира в «электронном» свете будут абсолютно блеклыми или вовсе прозрачными. Поэтому остаются только тяжелые металлы. И, раз «краска» только одна, то и картинка получается монохромной. И вдобавок сильно искаженной обезвоживанием и тяжелыми металлами. Серый скучный безжизненный мир.
Чтобы избежать искажений, был придуман метод криоэлектронной микроскопии [3], [5], за который в 2017 году вручили Нобелевскую премию по химии. Чтобы внутриклеточная вода не испарилась, ее замораживают. А чтобы получившиеся при заморозке кристаллы льда не разорвали мембраны, заморозку проводят очень быстро — так резко, что молекулы воды не успевают «построиться». Каждая молекула «замирает» на своем месте, и получается твердое, но некристаллическое вещество. Такое агрегатное состояние в физике называют аморфным — это нечто среднее между жидкостью и твердым телом. А замороженную таким образом воду называют аморфным льдом. А так как самое известное аморфное вещество нашего «обыденного» мира — стекло, то второе название такого состояния — стеклообразный лед (забегая вперед: именно его имели ввиду авторы обсуждаемой статьи [1], говоря о vitreously frozen cells — «стеклообразно замороженных клетках»).
А еще «остекление» внутриклеточной воды используют для консервации эмбрионов — об этом читайте в статье «Витрификация — контролируемая пауза развития в стеклоподобном состоянии» [6].
Но, как ни замораживай, изображение останется серым. А в современной молекулярной биологии, наоборот, все больше нужны «цветные» методики: она все активнее использует флуоресцентные красители. Таких красителей существует огромное множество: от зеленого флуоресцентного белка [7], за открытие которого тоже была вручена Нобелевская премия по химии, до «флуоресцентных репортеров» [8]. А флуоресцентные красители требуют световой микроскопии и цветного изображения.
Мир цветной. но все же скучный
А что, если совместить в одном изображении два вида микроскопии — световую и электронную? Получится коррелятивная свето-электронная микроскопия, или КСЭМ (correlative light-electron microscory, CLEM). В таком случае одни и те же структуры вначале фотографируются в световом и электронном микроскопах, а затем изображения совмещаются с помощью компьютера. Здесь мы вступаем в «продвинутую» микроскопию, когда сами не смотрим в окуляр микроскопа — изображение формируется методами компьютерной обработки данных.
Но при всей своей красоте метод полностью проблемы не решает — он лишь окрашивает детализированные структуры размытой «радугой», отражающей распределение флуоресцентной метки (рис. 3) [9]. Это позволяет изучить молекулярные особенности на уровне области клетки, но не специфично «подсветить» микроструктуры. Мир по-прежнему серый. Просто на него пролили полупрозрачную краску.
Рисунок 3. Коррелятивная свето-электронная микроскопия. На левом изображении — одноцветное фото элементов цитосклетета, на которое наложена цветовая «шкала» натяжения белка талина (сам белок при этом не виден в таком масштабе). На изображении справа внизу, где увеличение больше, цвета вновь исчезают. Таким образом, максимум, на что способна обычная КСЭМ, — изобразить в цветовой «кодировке» какую-либо величину, но она не придает изображению истинную цветность.
Тем не менее авторы статьи в Science взяли на вооружение именно идею коррелятивной микроскопии: совмещения двух видов микроскопии в одном изображении с помощью компьютера [1]. Просто «световое» изображение у них изначально было со сверхвысоким разрешением. Как же они его получили? С помощью тех же компьютеров!
Структурируем свет и зажигаем одиночные молекулы
Сфотографировать клетку с разрешением выше дифракционного предела нельзя. Но можно, используя различные ухищрения, «собрать» на экране компьютера одно изображение из множества снимков, получив гораздо большее разрешение. Такой подход называется микроскопией сверхвысокого разрешения, или СР-микроскопией (super-resolution microscopy, SR-microscopy). А конкретных методик довольно много — краткий их обзор представлен в статье «Лучше один раз увидеть, или Микроскопия сверхвысокого разрешения» [10]. Так что на выбор у авторов обсуждаемой статьи было несколько «прототипов».
Первый из них — микроскопия структурированного освещения (structured illumination microscopy, SIM). В ней образец окрашивается флуоресцентным красителем. Но возбуждающий свет фокусируется таким образом, чтобы в фокусе микроскопа получилась тонкая решетка из света. Она постоянно перемещается, и флуоресценция молекул, находящихся в фокусе, меняется. Объект не в фокусе продолжают светиться равномерно, что позволяет компьютерному алгоритму вычислить и «отсечь» его. Остается большой набор данных об изменении флуоресценции, по которому рассчитывается изображение с высоким разрешением (рис. 4). К сожалению, такой подход позволяет увеличить разрешение максимум в два раза [10]. Нет ли чего-нибудь еще?
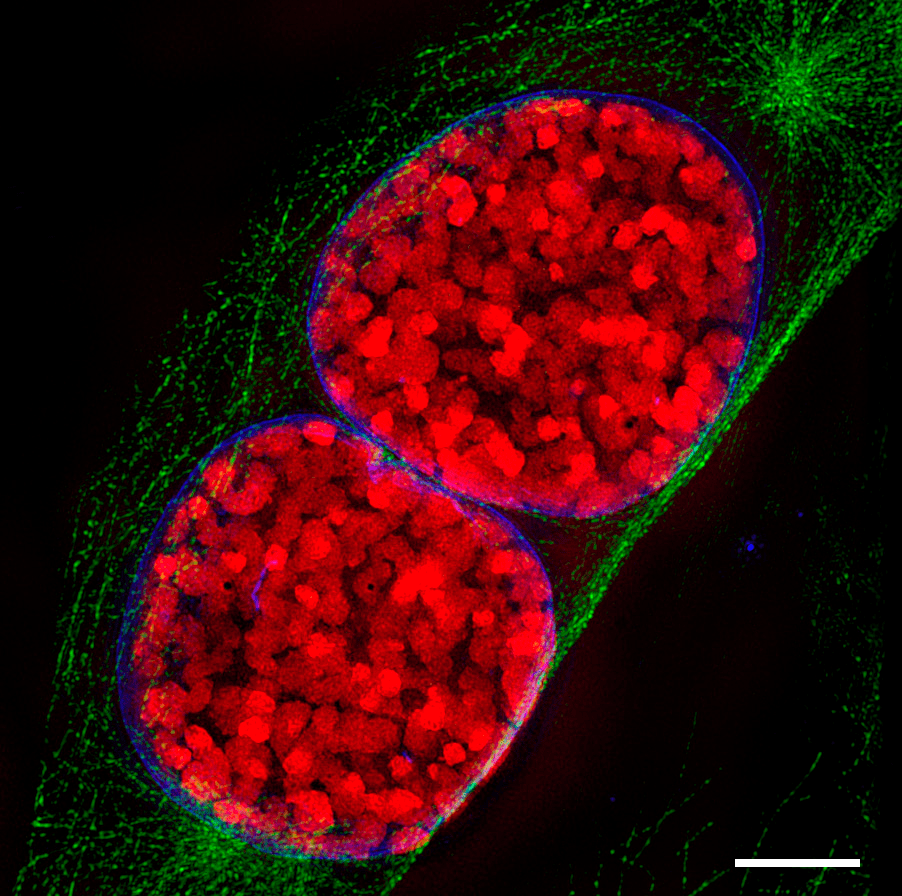
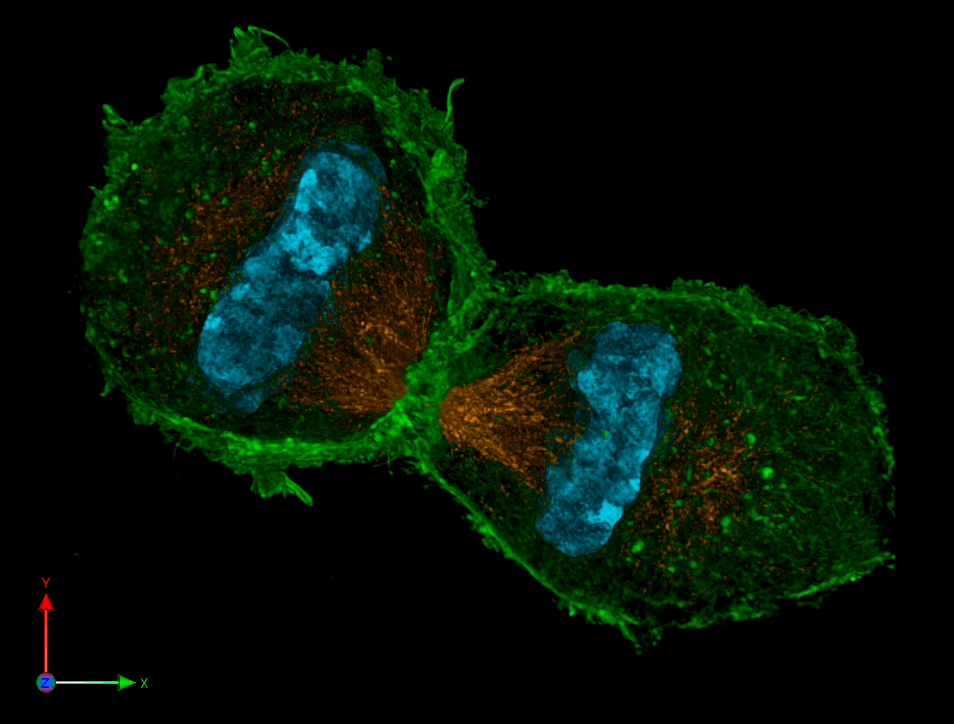
Рисунок 4б. Телофаза митоза, визуализированная методом SIM. Актиновый цитоскелет зеленый, тубулиновый — оранжево-бежевый, хроматин голубой. Сравните с рисунком 1б (где изображена анафаза митоза) — SIM явно выигрывает по детализации и информативности!
Коллектив исследователей тоже не остановился на SIM и в качестве второй отправной точки воспользовался одномолекулярной микроскопией, или микроскопией локализации одной молекулы (single-molecule localization microscopy, SMLM) [1]. За ее создание в 2014 году вручили Нобелевскую премию [2].
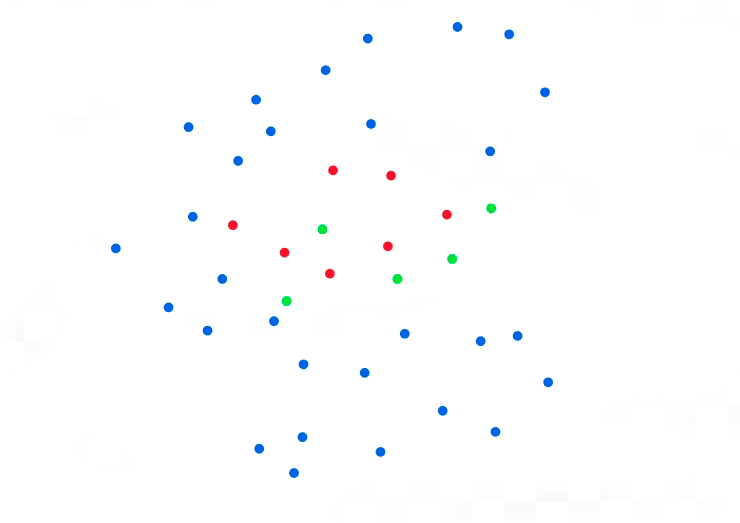
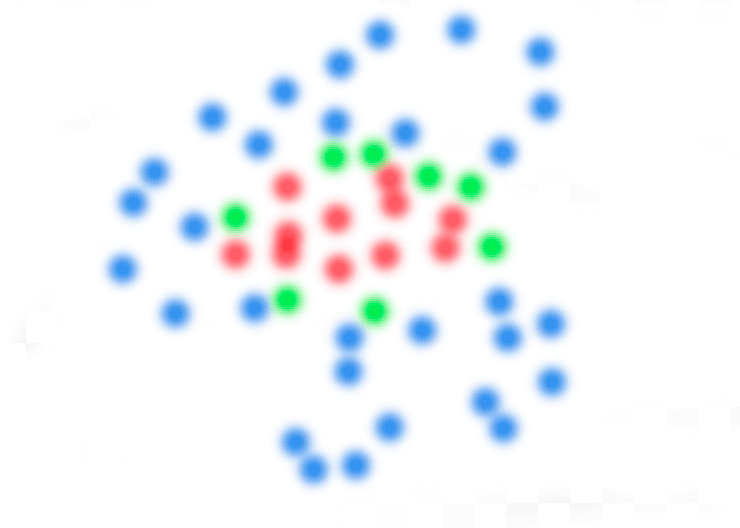
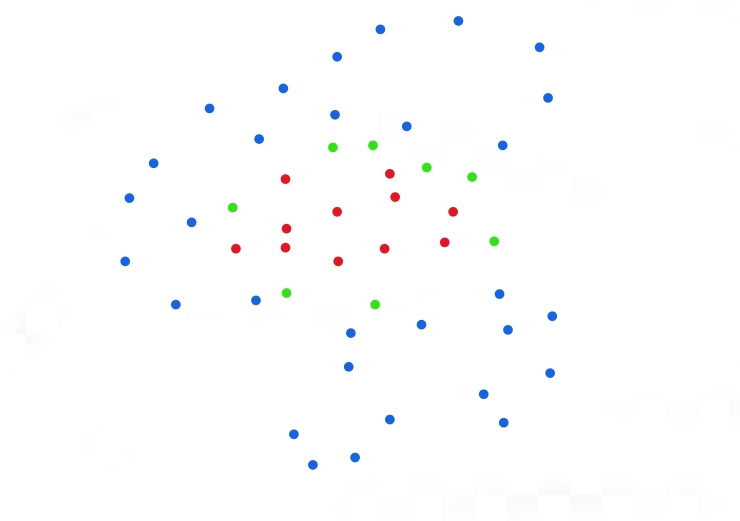
В этой методике флуоресценция красителя запускается слабым лазерным лучом — таким слабым, что лишь малая часть молекул начинает флуоресцировать. Какие именно молекулы засветятся — зависит только от случая, поэтому такой подход в микроскопии сверхвысокого разрешения называется стохастическим. Интенсивность луча подбирается таким образом, чтобы среднее расстояние между одиночными «засветившимися» молекулами было равно дифракционному пределу. Благодаря этому, каждое сфотографированное микроскопом светящееся пятно представляет собой одиночную молекулу (рис. 5а).
Далее компьютер точно вычисляет координаты молекулы, образовавшей каждое пятно, с помощью так называемой функции рассеяния точки (рис. 5б). А тем временем на образец подается другой лазерный луч определенной длины волны, который гасит флуоресценцию молекул. Затем снова включается «зажигающий» лазер. За счет случайности множество молекул, «вспыхнувших» во второй раз, не будет тем же самым (рис. 5в). И после компьютерной обработки появятся новые светящиеся точки (рис. 5г).
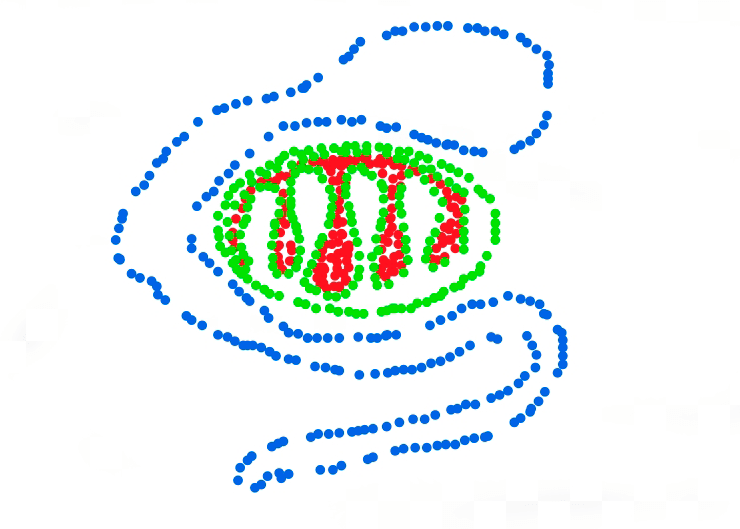
Цикл повторяется много раз, и на последнем этапе компьютер складывает все картинки со «светящимися точками». В итоге получается изображение, сложенное отдельными точечными источниками флуоресценции, расстояние между которыми намного меньше 0,2 мкм (рис. 5д). А это и есть сверхвысокое разрешение.
Рисунок 5а. Принцип действия одномолекулярной микроскопии. Представим, что у нас есть три флуоресцентных красителя. Синий метит мембраны эндоплазматического ретикулума, зеленый — мембраны митохондрий, красный — матрикс митохондрий. После слабого импульса возбуждающего лазера получились размытые пятна, каждое из которых соответствует одной молекуле флуорофора. Рисунок схематичный, масштаб не соблюден.
собственный рисунок автора статьи
Рисунок 5б. Принцип действия одномолекулярной микроскопии. Изображение подвергается компьютерной обработке — каждое пятно «сворачивается» в точку с помощью функции рассеяния. Положение точки соответствует положению светящейся молекулы.
собственный рисунок автора статьи
Рисунок 5в. Принцип действия одномолекулярной микроскопии. После второго возбуждающего импульса под микроскопом «вспыхнули» другие разноцветные пятна.
собственный рисунок автора статьи
Рисунок 5г. Принцип действия одномолекулярной микроскопии. Пятна вновь «превращаются» компьютером в точки.
собственный рисунок автора статьи
Рисунок 5д. Принцип действия одномолекулярной микроскопии. После многих повторений этого цикла компьютер объединяет все изображения с точками в одно. Готово! У нас есть изображение митохондрии с фрагментом ЭПР, составленное из множества флуоресцирующих точек. А так как расстояние между точками в итоге гораздо меньше дифракционного предела, то картинка получается в сверхвысоком разрешении, и на ней видны детали строения клетки.
собственный рисунок автора статьи
Помимо высокой детализации, еще одно преимущество микроскопии сверхвысокого разрешения (как SIM, так и SMLM) в том, что используемые функции позволяют «вычислить» на компьютере координаты каждой флуоресцирующей молекулы не только на плоскости, но и в пространстве. Поэтому у сверхразрешающей микроскопии есть 3D-модификации. Именно такой «разновидностью» SIM созданы изображения клеток в профазе и телофазе митоза на рисунках 4а и 4б. И именно такие методики использовали авторы статьи в Science [1]. Микромир наконец стал цветным и трехмерным. Что же к этому еще можно добавить?
Он живой и светится! А теперь сотрем его в пыль!
Так как в распоряжении ученых имеются методы с таким высоким разрешением, возникает резонный вопрос: а что, если вернуться к идее коррелятивной микроскопии, только теперь объединять изображения микроскопии высокого разрешения и электронной микроскопии? Именно это сделали авторы статьи в Science — и в этом основная новизна их методики [1]. Они соединили в одной технологии электронную микроскопию и световую 3D-микроскопию высокого разрешения.
Проблема в том, что классическая электронная микроскопия дает плоское изображение (сканирующая дает перспективное, но не может заглянуть внутрь объекта). Поэтому авторам статьи пришлось искать трехмерную методику электронной микроскопии.
К счастью, такая тоже существует и называется ФИЛ-СЭМ (англ. FIB-SEM) — сканирующая электронная микроскопия с фокусированным ионным лучом. К сожалению, она относится к деструктивным видам анализа — то есть при ее проведении образец разрушается.
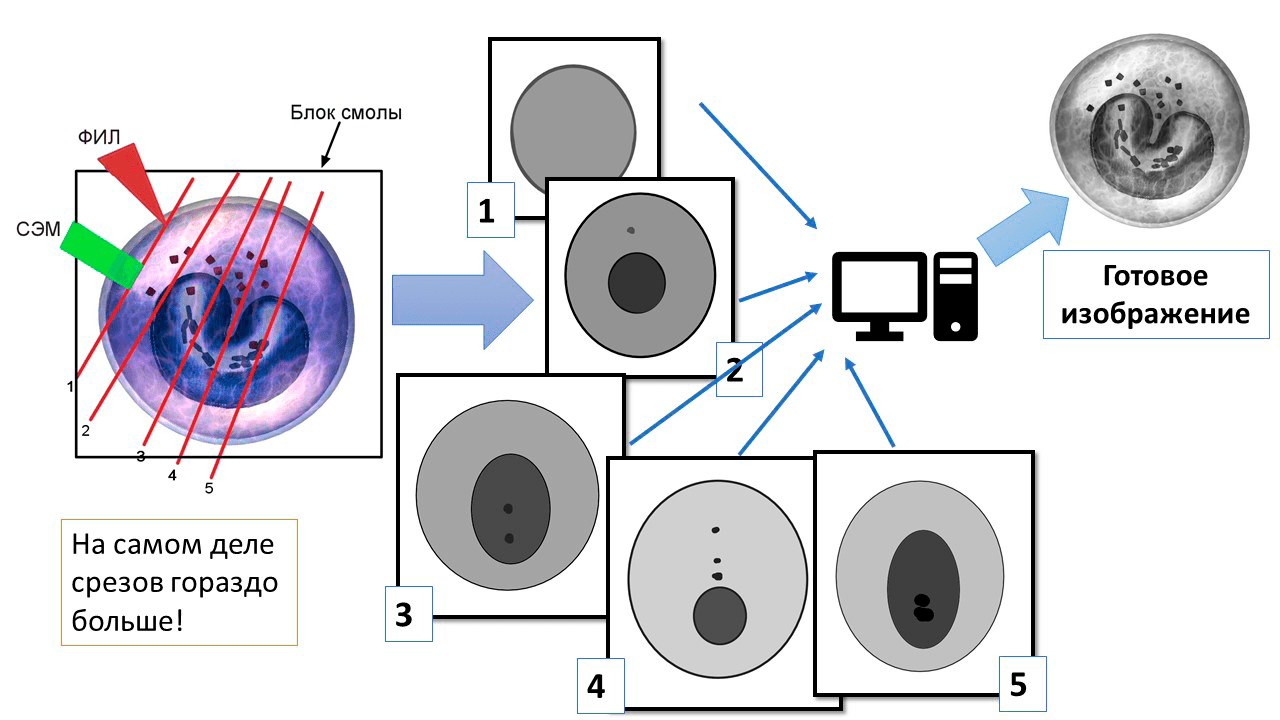
Вначале образец бомбардируется направленным пучком ионов, снимающим с него верхний слой. Обнажившаяся поверхность подвергается обычной сканирующей электронной микроскопии и получается срез клетки. Затем ионным лучом «снимается» еще один слой, и сканируется следующий срез. Цикл повторяется много раз, и в итоге — снова компьютерная обработка: компьютер объединяет все полученные срезы в одну трехмерную модель клетки. Это все, что от нее осталось — к концу опыта ионный луч буквально стирает образец в пыль (рис. 6, 7).
Рисунок 6. Принцип микроскопии сверхвысокого разрешения ФИЛ-СЭМ. Клетка помещается в блок из смолы, «лишние» части которого удаляются. Затем фокусированный ионный луч (ФИЛ) снимает с образца слой за слоем, а каждый срез фотографируется сканирующим электронными микроскопом (СЭМ). Получаются черно-белые срезы клетки в большом количестве (на рисунке их приведено 5, но в реальной микроскопии гораздо больше). Затем срезы объединяются на компьютере в одно трехмерное изображение — получается объемная, но, к сожалению, одноцветная модель. Мир приобрел объем, но он пока что черно-белый.
рисунок автора статьи с использованием фото EONexperience
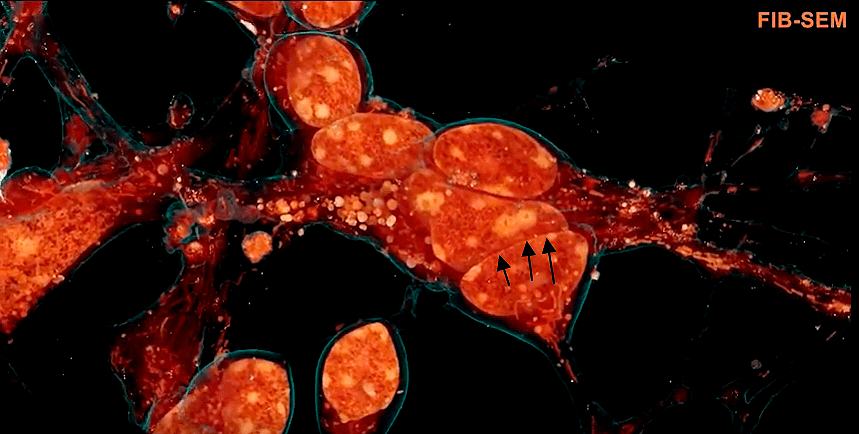
Рисунок 7а. Гранулярные клетки мозжечка мыши, визуализированные с помощью FIB-SEM авторами обсуждаемой статьи (кадр из видео во введении) [1]. Изображению при обработке приданы цвета, однако детали внутреннего строения клеток одноцветные — как и «полагается» при электронной микроскопии. Черными стрелками показана область межклеточного контакта (адгезии) между двумя нейронами, детальные изображения которой будут разбираться дальше.
Рисунок 7б. Трехмерная модель клетки, созданная с помощью ФИЛ-СЭМ, в разрезе. Обратите внимание, что внутри она такая же черно-белая, как обычная электронная микрофотография. На этом рисунке уже не нейрон (хотя похож): это клетки линии COS-7 — потомки фибробластов (клеток соединительной ткани) почек обезьяны. Поэтому они также имеют отростчатую форму.
Рисунок 7в. Снова трехмерные модели (ФИЛ-СЭМ) клеток COS-7 в разрезе. Сплошная серость внутри.
Разрушение образца ионным лучом при исследовании методом ФИЛ-СЭМ, само собой, лишает способности рассмотреть его методами высокого разрешения. Клетка, которую стерли в молекулярную пыль, не может выглядеть как живая и светиться. Поэтому исследователи сначала рассматривали образец методами СР-микроскопии, а потом использовали методику ФИЛ-СЭМ. Получались трехмерные модели, которые впоследствии с помощью компьютера объединялись в одну.
Такой подход — создание одного изображения из многих на основе технологии больших данных — резко сближает микроскопию с биоинформатикой, являющейся одной из любимых тем «Биомолекулы» (в частности, о биоинформатике написано в наших статьях «Я б в биоинформатики пошел, пусть меня научат!» [11], «12 методов в картинках: “сухая” биология» [12], и есть даже целая тема «“Сухая” биология»). Похоже, границы между областями науки сейчас стираются в невиданных масштабах, а методы информатики активно проникают во все области и помогают решать невообразимые доселе задачи.
В методику СР-микроскопии авторы тоже внесли усовершенствования. Обычно для замораживания образца в СР-микроскопии используется жидкий азот, где уверенно достигается температура лишь около 77 градусов выше абсолютного нуля температуры (77 K, или около −196 °C). Это адски низкие температуры, но ученые при подготовке образца достигли еще меньших! Они использовали жидкий гелий, который позволил заморозить образец до 8 градусов выше абсолютного нуля (−265 °C) и даже до более низких температур. Таким образом клетки были моментально заморожены до состояния аморфного льда, находившегося почти у самого предела холода.
При таких условиях физика (наконец-то!) сыграла на руку исследователям. В этом адском холоде среднее время пребывания флуоресцентного красителя в «погашенном» состоянии существенно выше, чем при −196 °C, что позволяет располагать молекулы флуорофора ближе друг к другу. Поэтому у авторов «светящиеся точки» на реконструируемом изображении были ближе, и само изображение получалось детальнее и контрастнее (рис. 8).
Рисунок 8. Те же клетки, что и на рисунках 7а и 7б, и на видео во введении, только изображение получено одномолекулярной микроскопией (SMLM). Зеленый флуорофор (ER3) окрашивает эндоплазматический ретикулум (ЭПР) — сеть канальцев внутри клетки. На рисунке хорошо видно, насколько он разветвлен и как плотно заполняет всю клетку. Ядра зеленые, потому что межмембранное пространство ядра — по сути, начало ЭПР. Фиолетовый флуорофор (TOMM20) окрашивает митохондрии, и большинство фиолетовых «колбасок» в клетках среди зеленых разветвлений ЭПР — это именно они. Но — сюрприз — исследователи обнаружили, что этот «митохондриальный» краситель окрасил не только их. Об этом — чуть ниже.
Следует отметить, что авторы также использовали два типа микроскопии сверхвысокого разрешения — SIM и SMLM. В общем, основательно подготовились к покорению дифракционного барьера. На последней стадии, как и в любой корреляционной микроскопии, трехмерные изображения клеток из ФИЛ-СЭМ и SMLM/SIM совмещались с помощью компьютерной техники. В итоге получилось трехмерное изображение, одновременно и детализированное, и цветное. Микромир наконец стал объемным и ярким (рис. 9).
Рисунок 9а. Корреляционная одномолекулярная-ФИЛ-СЭМ микроскопия клетки COS-7 заключается в компьютерном объединении трехмерных изображений, показанных на рисунках 7а–в и 8. Теперь «внутренности» клетки, в отличие от рисунков 7б и 7в, приобрели цвета, что позволяет их детально рассмотреть и понять структуру (цвета и красители те же, что на рисунке 8). Тонкая сеть ЭПР стала видна еще детальнее, хорошо видны митохондрии.
Рисунок 9б. Потрясающий «инопланетный» ландшафт — это всего лишь срез модели, показанной на рисунке 9а. Цвета и флуорофоры те же, что и на рисунке 8.
Но что способна дать миру новая микроскопия, помимо объема и яркости? Что нового увидели исследователи в свой микроскоп? Спойлер: им удалось сделать сразу три небольших открытия в ультраструктуре клетки — и это только начало!
Пузырьки, трубочки и красители не на своем месте
Эукариотические клетки, в том числе клетки человека и животных, изобилуют различными мембранными структурами — везикулами и сетью ЭПР, и это не считая митохондрий и пластид. Примером того, как они пронизывают всю клетку, могут послужить рисунки 8, 9а и 9б. И именно их труднее всего рассмотреть под микроскопом. В «серой и безжизненной» электронной микроскопии они могут быть недостаточно контрастны, а при криоэлектронной томографии (метод аналогичен компьютерной томографии для человека, только здесь томография делается клетке в просвечивающем электронном микроскопе) могут быть пропущены, оказавшись между срезами. Особенно это касается везикул (пузырьков) небольшого объема — поэтому мы сейчас не так много знаем об их форме, размерах и разновидностях.
Новый метод микроскопии позволил рассмотреть эти структуры как никогда ранее детально. Оказалось, что мелкие трубочки ЭПР усеяны вздутиями-пузырьками, которые раньше увидеть было затруднительно. Но это еще не самое интересное.
Рисунок 10. Так выглядит ER3-позитивная везикула в ядре — ярким зеленым пятном. Не очень четко, но загадочно: откуда она там взялась?
Краситель TOMM20, как оказалось, тоже окрашивал не только митохондрии, но и какие-то пузырьки в цитоплазме (рис. 11). Исследователи резонно предположили, что эти пузырьки — везикулы митохондриального происхождения (mitochondria-derived vesicles, MDVs). Об их функции пока мало что известно, но есть предположения, что они участвуют в «контроле качества» белков митохондрии, транспортируя поврежденные и ошибочно свернутые в эндосомы — к местам расщепления. Правда, неясно, почему другие белки они несут в пероксисомы. [13] Так или иначе, с новой методикой их стало гораздо легче изучать и рассматривать. Обсуждаемая статья напомнила, что в клетке больше, чем три вида везикул (эндосомы, лизосомы, пероксисомы), и мы еще не всё знаем о мире пузырьков и трубок, пронизывающих каждую клетку.
Рисунок 11. В цитоплазме клетки обнаружены пузырьки, которые окрашиваются красителем для митохондрий. Вопрос — что они там делают? Возможно, они уносят из митохондрий поврежденные белки на утилизацию. Так сказать, вывоз митохондриального мусора.
Еще авторы показали, что и хорошо известные нам везикулы — вовсе не скучные шарики. Шариками являются лишь небольшие пузырьки — и то лишь за счет поверхностного натяжения. А при увеличении размера они могут принимать причудливые формы. Пероксисомы в виде чашек, блюдец и полых сфер с отверстием, вытянутые эндосомы с расширением (рис. 12). Пока можно лишь предполагать, зачем клетке весь этот «сервиз». Например, изменчивость формы может пригодиться для регуляции скорости реакций, которые проходят в этих пузырьках, но как именно это происходит? С помощью своей технологии исследователи сформулировали несколько загадок для научного мира.
Рисунок 12. Варианты форм пероксисом и эндосом. Розовым обозначены пероксисомы, желтым — эндосомы, красным — эндоплазматический ретикулум, изумрудно-голубым — митохондрии, синим — неизвестные органеллы (да, исследователям и такие попались!).
Нейроны: идем на контакт!
С помощью новой методики исследователи рассмотрели некоторые детали зернистых нейронов мозжечка мыши и их клеток-предшественников. Зернистые клетки расположены в коре мозжечка, являясь участницами сложной нейронной сети для обработки сигналов о положении и равновесии и двигательного научения. Они являются самыми многочисленными в коре мозжечка.
В процессе созревания нейроны преодолевают огромные по меркам мозга расстояния, но безошибочно находят свое место, «подключаются» к нейронным сетям, учатся реагировать на входные сигналы, «взрослеют» и послушно умирают, если оказались лишними. Безошибочно найти свое место им помогают межклеточные контакты друг с другом, а процесс созревания сопряжен с изменением структуры хроматина в ядре. Эти две структуры и изучили исследователи.
Существует несколько видов межклеточных контактов. Здесь ученые рассматривали тот, который называется плотным соединением — участки мембран соседних клеток, крепко сшитых друг с другом определенными белками. Сюрпризом для ученых оказалось то, что мембраны нейронов сшиваются не на всем протяжении — плотные контакты образуют структуру, напоминающую паутину или швейцарский сыр [1], [14]. Такой причудливый рисунок прекрасно виден как с помощью методики крио-SIM, так и с помощью FIB-SEM, и становится еще более впечатляющим при совмещении изображений (рис. 13).
Рисунок 13. Слева — не полярное сияние, а справа — не сыр. Это все «сшивки» между мембранами соседних нейронов, изображенные в разном «свете»: слева SIM, где разными цветами помечены белки межклеточных контактов, а справа FIB-SEM.
Нейроны: «детский» и «взрослый» хроматин
Рассмотрев эту мембранную «вышивку» из белков межклеточного контакта, ученые заглянули в ядро этих же самых нейронов и их клеток-предшественников, незрелых форм. Новая технология предоставила потрясающую возможность рассмотреть в деталях хроматин клетки (современные представления об устройстве хроматина можно почерпнуть в статье «Новый взгляд на геном: не просто цепочка генов, а трехмерная сеть, интегрирующая функциональные домены ядра» [15]).
Можно предположить, что при созревании нейрона меняется набор генов, которые он «считывает» и делает по ним белки (это называется экспрессией генов). Одни гены «запаковываются» плотнее и делаются неактивными, а другие, наоборот, «разматываются» и начинают активно функционировать.
Вначале авторы получили трехмерное изображение хроматина нейронов методом ФИЛ-СЭМ. Но само по себе оно мало что дает: в таком варианте хроматин выглядит как серая каша (эухроматин) с комками (гетерохроматин). Единственное различие между нейронами-«малышами» и «взрослыми» нейронами, которое заметили авторы на таких изображениях, в том, что у «взрослого» хроматин более «жидкий»: эухроматина больше.
Но микроскопия сверхвысокого разрешения позволила авторам изучить распределение в этой «каше» двух важных белков хроматина — гетерохроматинового белка 1α (HP1α) и гистона H3.3 (который является ни чем иным, как вариантом гистона H3, составной части нуклеосомной «катушки»). Первый из них обычно обнаруживается в составе гетерохроматина (плотно упакованных неактивных частей ДНК), а второй — наоборот, присутствует в регионах, где с ДНК происходит активное «считывание».
Технология обеспечила потрясающе детальный моментальный снимок состояния ядра нейрона до и после дифференцировки.
Когда хроматин обрел цвет, оказалось, что он значительно различается у молодых и зрелых нейронов. В «черно-белом мире» два этих типа клеток не особо отличались друг от друга по количеству гетерохроматина в ядрах. Но «в цвете» стало заметно, что в процессе созревания нейрона количество гетерохроматина, содержащего HP1α, увеличивается почти вдвое (рис. 14, 15). Кроме того, этот гетерохроматин стал гораздо более компактным.
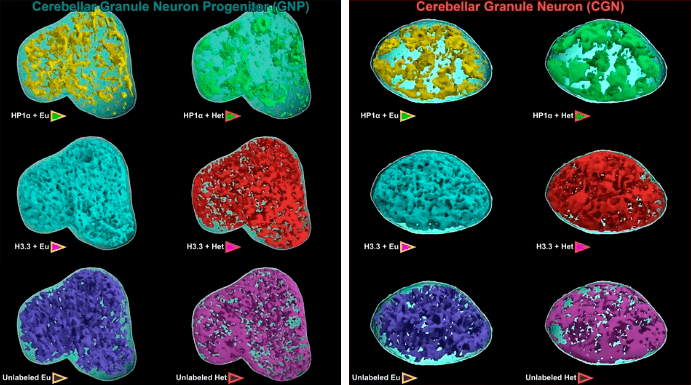
Рисунок 14. Срез ядер нейронов при микроскопии сверхвысокого разрешения. Слева — ядро клетки-предшественника зернистых клеток мозжечка в форме сердца. Справа — ядро зрелой зернистой клетки мозжечка (округлое). Розовым окрашен гистон H3.3, зеленым — белок HP1α. Заметно различное распределение этих двух маркеров в молодых и зрелых клетках.
Рисунок 15. Трехмерные модели ядер нейронов, полученные при коррелятивной микроскопии. Цветная масса внутри каждой из них представляет собой эу- или гетерохроматин, меченый одним из маркеров. Слева — ядра клеток-предшественников (в виде сердца), справа — округлые ядра зрелых клеток. Обратите внимание на:
Накопление HP1α в гетерохроматине — это еще классика жанра. Ведь, как я писал выше, HP1α — характерный для неактивного хроматина компонент. Но микроскопия сверхвысокого разрешения показала также. накопление гистона H3.3 в процессе созревания, что было неожиданным для исследователей. Этот гистон характерен для активно транскрибируемых («считываемых») участков ДНК. В гетерохроматине его до этого находили лишь в эмбриональных стволовых клетках, что понятно — они готовы к активации почти любого участка ДНК. Но в зрелых клетках, да еще в нейронах? Тем не менее он не только накапливается, но и, как классический HP1α-гетерохроматин, становится более компактным. Давая исследователям понять, что об укладке мы знаем еще далеко не все.
Заключение
Новый метод микроскопии оказался технически удачным: впервые мельчайшие детали строения и развития клеток предстали перед исследователями в цвете, в трехмерном виде, в высоком разрешении. Это то, чего так давно не хватало исследователям — увидеть внутренний мир клетки не плоским и скучным, а «круглым и пушистым».
Но, с другой стороны, увиденное пока принесло не столько ответы, сколько вопросы. Что за пузырьки, красящиеся митохондриальным красителем? Точно ли они происходят из митохондрий? Почему пероксисомы и эндосомы так различаются по форме, а в хроматине при созревании нейрона накапливаются неожиданные белки? Всего три дополнительных «мини-исследования» в статье показали, что наши знания о клетке пока крайне неполны. Это отмечают и сами исследователи:
Еще предстоит проделать так много экспериментов — изучить целый мир где-то там в клетках.
Харальд Хесс,
один из авторов статьи [1].
Между строк в статье [1] и пресс-релизе [14] читается удивление исследователей и желание поскорее во всем разобраться. Изучить цветной и объемный мир, о котором мы пока так мало знаем.