миофиброз что это такое
Что такое миофасциальный синдром? Причины возникновения, диагностику и методы лечения разберем в статье доктора Коршуновой Юлии Витальевны, невролога со стажем в 31 год.
Определение болезни. Причины заболевания
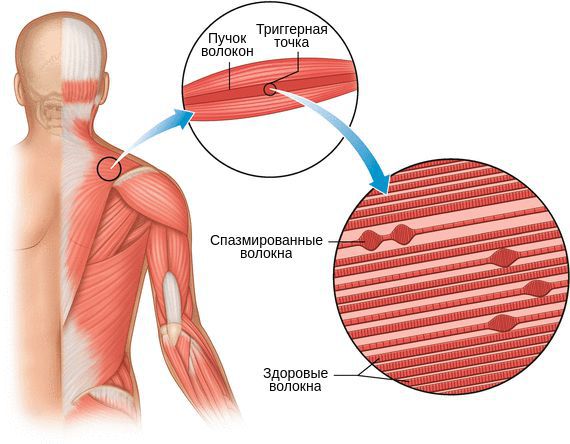
Миофасциальный синдром — это болезненное состояние, для которого характерна боль в любой части тела и болезненные мышечные напряжения с локальными уплотнениями — триггерными точками. Источником такой боли становятся мышцы и фасции — соединительная ткань, покрывающая мышцы.
Миофасциальная боль — одно из проявлений миофасциального синдрома. Она развивается при хронической скелетно-мышечной боли и может возникать в любых скелетных мышцах.
Триггерные точки, как и миофасциальная боль, могут располагаться в любой мышце. Их появление не зависит от расы и пола, однако с возрастом риск образования увеличивается.
Развитию миофасциальной боли способствуют многие факторы:
Боль в поражённых внутренних органах и суставах приводит к защитному напряжению мышц. Это позволяет разгрузить сустав и создать мышечный корсет вокруг внутреннего органа. Например, при некоторых болезнях желудка тонус сгибателей шеи снижается, а тонус разгибателей повышается. Это приводит к боли в области затылка.
Эмоциональный стресс также сопровождается мышечным напряжением, чем может активировать триггерные точки. При этом мышцы могут оставаться в спазмированном состоянии даже после прекращения стресса.
Другими причинами миофасциального синдрома могут стать длительное статическое напряжение мышц и стереотипные движения, особенно в условиях низкой температуры. К таким факторам относят частые повороты и наклоны туловища, однообразный тяжёлый физический труд, длительную сидячую работу в офисе или долгие поездки за рулём.
Спровоцировать появление триггерных точек может сдавление мышц ремнями, лямками рюкзака, узкими бретельками, тугими джинсами или тяжёлой шубой.
Ещё одна причина — длительная неподвижность мышцы, например сон в одной и той же позе или ношение гипса после перелома.
Свой вклад в формирование миофасциального синдрома также вносят:
Симптомы миофасциального синдрома
Классическими признаками миофасциальной боли являются:
Пациенты с миофасциальной болью обычно жалуются на местные ноющие и плохо локализуемые боли в мышцах и суставах, которые часто не дают им уснуть. Боль может быть очень сильной и отдавать в конечность. Такое состояние пациенты часто трактуют, как ущемление нерва.
Миофасциальная боль может вызывать напряжение, мышечную слабость, треск и щелчки в суставах, а также вегетативные явления, например потливость, ощущение «ползания мурашек» и изменения температуры кожи.
Спазмированная мышца, сдавившая проходящий рядом кровеносный/лимфатический сосуд или нерв, может вызвать дополнительные симптомы, такие как онемение и отёк части тела. При спазмировании мышц шеи может возникнуть головокружение, заложенность и шум в ухе.
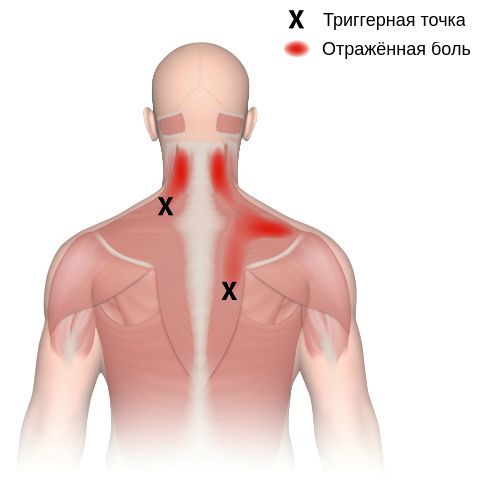
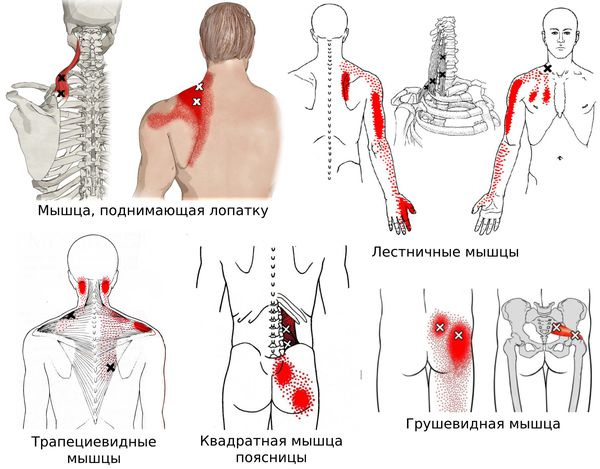
Согласно наблюдениям, чаще спазм возникает в мышце, поднимающей лопатку, грушевидной, трапециевидной, лестничной мышцах и квадратной мышце поясницы.
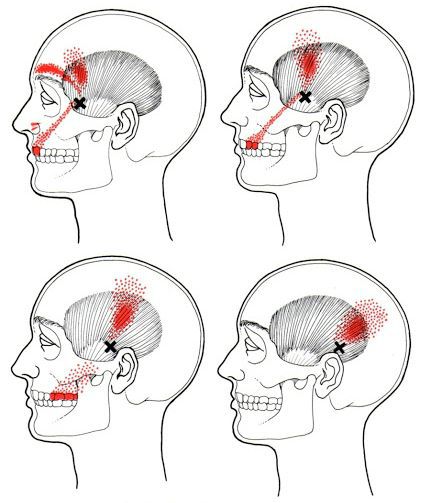
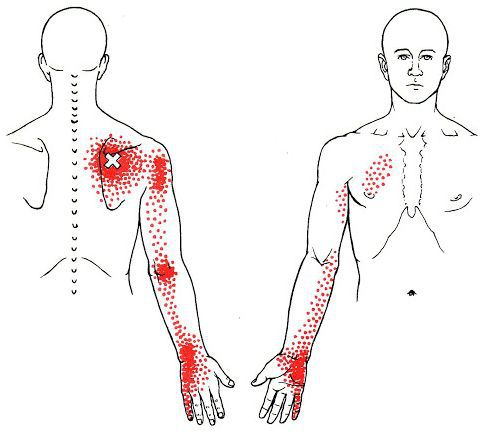
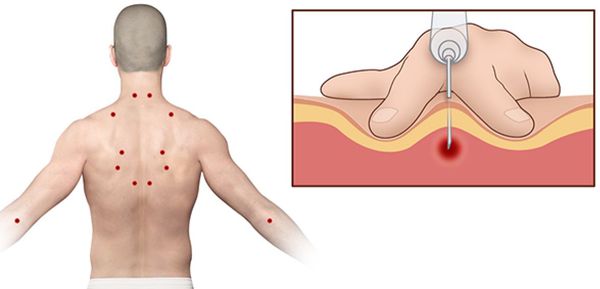
Каждой точке характерны свои зоны иррадиации. Например:
Активные триггерные точки являются непосредственным источником боли. После их стимуляции боль распространяется в отдалённые, но строго определённые зоны, как на картинках выше.
Уплотнение участка мышцы может предшествовать формированию триггерной точки, поэтому его появление не всегда сопровождается болью.
Патогенез миофасциального синдрома
Патофизиология миофасциальной боли не совсем понятна. Считается, что в основе этой патологии лежит нарушение сократимости мышц и уменьшение их способности к расслаблению.
Длительный спазм приводит к рубцеванию мышцы и формированию триггерных точек. Мышца становиться менее растяжимой, что ведёт к ограничению движений.
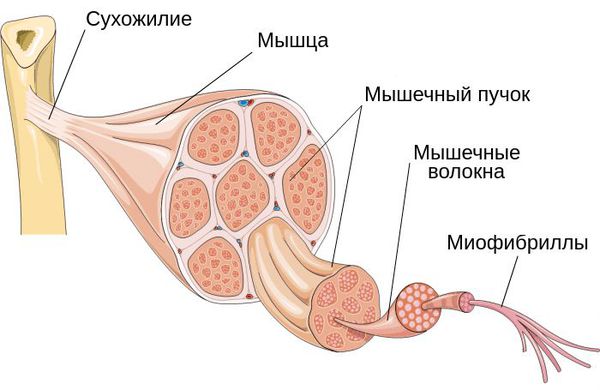
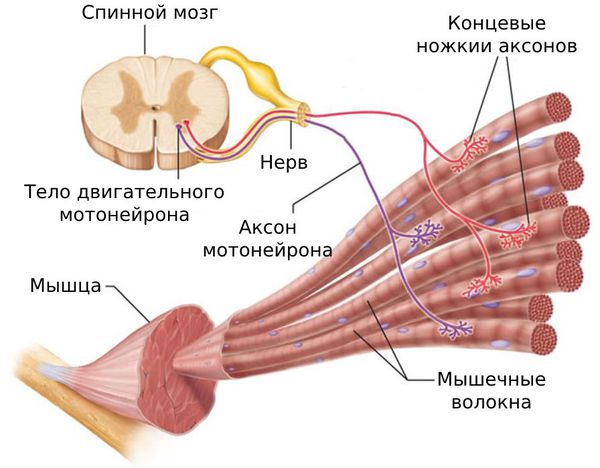
Поражение может локализоваться как в пределах нескольких миофибрилл — микроструктурной части мышцы, так и в мышечных группах.
Один из показателей изменения тонуса мышц — наличие локальных уплотнений. Они могут образоваться в вялой (гипотоничной) мышце в виде малоактивных образований или как триггерный феномен в виде уплотнённого участка мышцы с выраженной местной и отражённой болью и локальным судорожным ответом.
Классификация и стадии развития миофасциального синдрома
В Международной классификации болезней (МКБ-10) нет отдельного кода для миофасциального синдрома. Он относится сразу к нескольким рубрикам:
Первичный синдром связан с первоначальной дисфункцией мышцы, например перерастяжением, повторной микротравмой, переохлаждением мышцы и работой за компьютером в неправильной позе.
Течение миофасциальной боли разделяют на три фазы:
Осложнения миофасциального синдрома
Лечение триггерных точек временно облегчает боль, иррадиирующую из внутренних органов. Б ез лечения миофасциальный синдром может усугубить симптомы остеохондроза, сколиоза или другого основного заболевания, тем самым формируя порочный круг.
В качестве осложнений также можно отметить сдавление сосудов и нервов спазмированной мышцей. Это состояние приводит к радикулиту и вазомоторным нарушениям: приливам, повышенной потливости и побледнению кожи.
Диагностика миофасциального синдрома
Чтобы поставить диагноз «миофасциальный синдром», необходимо выявить у пациента пять больших критериев и один из трёх малых.
Физикальное обследование
Поиск триггерных точек — наиболее важная часть осмотра при подозрении на миофасциальный синдром. Как правило, они находятся в определённых участках мышц. При давлении на такие точки пациент подпрыгивает или вздрагивает от боли и дискомфорта. Причём боль возникает в характерной для каждой мышцы области.
Пальпируя мышцу перпендикулярно мышечным волокнам, можно обнаружить узел или тугой тяж — веревкообразное утолщение. Это и есть триггерная точка. Пальпация данной зоны очень болезненна.
В области активных и латентных триггерных точек пальпируемой мышцы могут отмечаться подёргивания, местные вегетативные реакции и сенсорные нарушения, такие как парестезии и дизестезии.
Парестезии — это ощущения, которые возникают без каких-либо раздражителей, например ползание мурашек.
Дизестезии — это ощущения, которые не соответствуют силе раздражителя. В таких случаях лёгкое прикосновение к коже может вызывать неприятные ощущения или даже сильную боль.
Часто сенсорные нарушения соответствуют зоне распространения боли.
Лабораторные исследования
Лабораторных тестов, выявляющих миофасциальный синдром, не существует. Однако они полезны в поиске предрасполагающих факторов, таких как гипотиреоз, гипогликемия и дефицит витаминов.
Перечень анализов включает общий анализ крови, скорость оседания эритроцитов (СОЭ), биохимический профиль и определение уровня витаминов C, B1, B6, B12 и фолиевой кислоты. На причину миофасциальной боли могут указать любые отклонения в результатах данных тестов.
Анализ на тиреотропин, или тиреотропный гормон (ТТГ), может быть полезным при наличии клинических признаков заболевания щитовидной железы. Допустимые значения тиреотропина для взрослых составляют 0,3-4,2 мкме/мл.
Дополнительные методы исследования
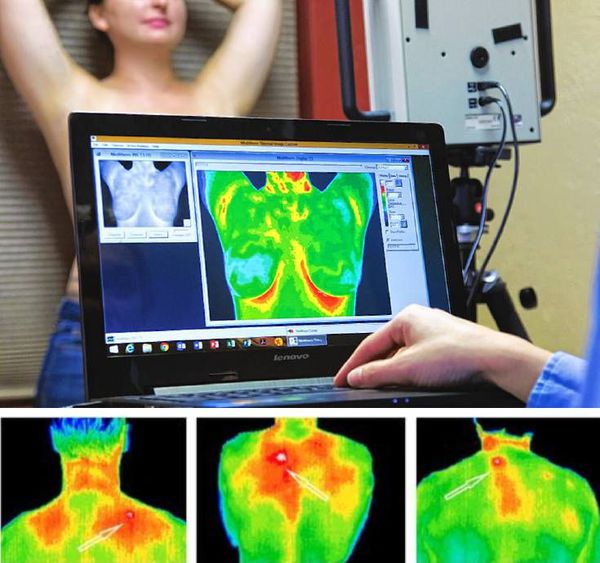
Инфракрасная или жидкокристаллическая термография позволяют визуализировать усиление кровотока, которое иногда отмечается в триггерных точках. Но данные методики применяются редко, так как они не являются стандартизированными.
Дифференциальная диагностика
В ходе обследования важно исключить другие причины боли: фибромиалгию, радикулопатию, дискогенную боль, спондилогенную боль, заболевания суставов (артрозы, артриты ) и болезни внутренних органов.
Лечение миофасциального синдрома
В лечении миофасциальной боли применяют комплексный подход. Он предполагает устранение патологического мышечного напряжения и триггерных точек.
При первичном синдроме проводится местное воздействие на поражённые структуры:
При вторичном синдроме на первый план выходит лечение основного заболевания.
К медикаментозным методам лечения миофасциальной боли относят:
НПВП снимают боль, воспаление и понижают температуру тела. Механизм их действия основан на подавлении активности веществ, которые участвуют в каскаде воспалительных реакций.
При выраженном болевом синдроме назначают низкие дозы трициклических антидепрессантов. Они уменьшают мышечную боль и обладают седативным эффектом.
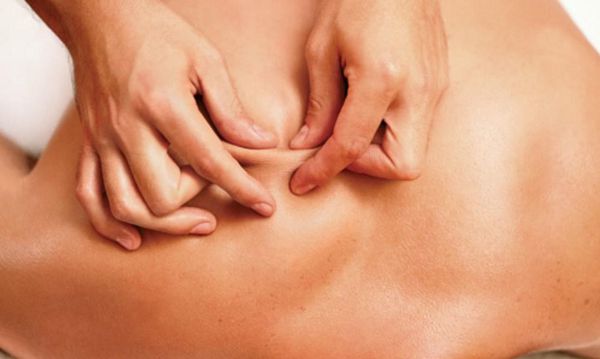
Ишемическая компрессия триггерных точек направлена на прекращение или значительное снижение мышечного напряжения и уменьшение боли. Триггерная точка сдавливается кончиками пальцев и удерживается 60-90 секунд с постепенным увеличением силы давления.
Одновременно со сдавливанием триггерной точки производится растяжение поражённой мышцы. Это позволяет сократить время процедуры: чем больше мышца растягивается, тем сильнее она расслабляется, снимается гипертонус, быстрее происходит обезболивание.
Пациенты, принимавшие участие в эксперименте, были разделены на три группы по 20 человек: первую группу лечили в течение 4-х дней с помощью лидокаинового пластыря, приклеенного на триггерную точку; второй группе назначался пластырь с плацебо; а третья группа получала инъекции 0,5 % гидрохлорида бупивакаина.
Исследователи обнаружили, что в первой и третьей группах значительно уменьшились субъективные симптомы и увеличился порог болевой чувствительности. Причём эффективность терапии оказалась выше у пациентов третьей группы, которая получала инъекции анестетика, но они испытывали больший дискомфорт от проводимого лечения, чем пациенты из первой группы.
Пластырь используют только один раз в сутки. Его приклеивают на сухую неповреждённую кожу в области боли не больше чем на полдня, после чего делают перерыв не менее 12 часов. Перед приклеиванием пластыря волосы на коже нужно состричь ножницами, не сбривать.
Одновременно можно использовать не больше трёх пластырей. Если потребуется, пластырь можно разрезать на части, но только перед удалением защитной плёнки. Повторно использовать снятый пластырь не следует.
Важно регулярно оценивать эффективность такой местной терапии. Это позволит определить оптимальное количество пластырей, которые можно использовать одновременно, чтобы покрыть область боли или увеличить время между аппликациями.
Через 2-4 недели от начала лечения эффективность аппликаций нужно оценить повторно. Если за это время ответ на терапию был недостаточным или терапевтический эффект определяется только защитными свойствами пластыря, лечение следует прекратить.
В лечебный комплекс должны быть включены упражнения по перестройке неоптимального двигательного стереотипа. Они корректируют позы и движения, выполняемые в быту и во время работы.
В университете штата Мичиган проводилось изучение различных методик массажа и мануальной терапии, в результате которого был разработан специальный метод воздействия на миофасциальные структуры — » миофасциальный релиз «. Данная техника предполагает самостоятельное выполнение упражнений, без помощи врача или массажиста, что даёт возможность регулировать степень нажатия на мышцы и их растяжение, руководствуясь своими ощущениями.
Миофасциальный релиз можно выполнять с помощью различных инструментов: пенопластовых и ручных роликов, латексных шариков или других вспомогательных устройств. Они позволяют снять излишнее напряжение в триггерных точках, расслабить мышцы и связочный аппарат путём воздействия на фасцию. В результате наступает полное расслабление одной или группы мышц.
Механизмы, лежащие в основе миофасциального релиза, изучены недостаточно. Исследования, пытающиеся проиллюстрировать эффективность данной техники, часто плохо спланированы и не дают ответа на вопросы о том, как долго должна проводиться эта процедура, какой должна быть сила давления на поражённую мышцу и какое приспособление лучше подходит для упражнений.
Программа реабилитации предполагает использование ортезов: корсетов, бандажей, специальной обуви, стелек и пр. Ортопедические стельки, специальная ортопедическая обувь и подпяточники, к примеру, могут быть полезны для коррекции длины ног.
Прогноз. Профилактика
Миофасциальный синдром — не опасное для жизни состояние, но оно может значительно снизить качество жизни и стать основной при чиной временной нетрудоспособности.
Всем людям, старше 18 лет, Всемирная организация здравоохранения рекомендует:
Если мышцы будут крепкими, упругими, эластичными, с хорошим кровоснабжением, то в условиях перегрузок они либо не пострадают, либо пострадают минимально и быстро восстановятся.
Помимо ведения активного образа жизни важно избегать провоцирующих факторов и не заниматься самолечением при появлении боли, независимо от её локализации.
Миофиброз что это такое
Миофиброз в правом желудочке при тетраде Фалло и в левом желудочке при врожденном сужении устья аорты в ряде случаев является диффузным, поскольку подвергшиеся коллагенизации решетчатые волокна пронизывают всю толщу стенки наиболее гипертрофированного желудочка. Тем не менее самой большой степени процесс коллагенизации решетчатых волокон достигает во внутренних слоях миокарда, в трабекулярных и папиллярных мышцах.
Таким образом, аргирофильная строма гипертрофированного сердца при врожденных пороках изменяется по тем же законам, что и при гипертрофии сердца другой этиологии.
Паренхима и строма сердца представляют собой неразрывное целое. Понятие «компенсаторная гипертрофия миокарда» включает в себя и понятие «гиперплазия стромы», так как гипертрофия миокарда при различных видах врожденных пороков, а также при гипертрофии сердца другой этиологии сопровождается разрастанием сети продольных и поперечных интрамуральных решетчатых волокон.
О значении соединительнотканной основы мышечной ткани свидетельствует работа В. А. Энгельгардта (1948), в которой автор указывает, что движущей силой сокращения служит эластическое натяжение растянутой соединительнотканной основы, поэтому активной фазой мышечной деятельности является фаза расслабления. Миозиновая структура в мышечном волокне обусловливает сопротивление тянущей силе соединительнотканной основы.
Автор считает, что эластичность сокращенного и растянутого мышечного волокна зависит исключительно от оплетающей это волокно соединительнотканной стромы.
Мы не будем подробно разбирать очень важные и интересные вопросы фибриллогенеза в гипертрофированном миокарде, поскольку они специально обсуждены нами ранее (1949).
Следует отметить, что вопросы фибриллогенеза все еще далеки от решения, поскольку даже электронная микроскопия не дала этой возможности (В. П. Гилев, 1959). Укажем лишь, что нами особенно замечены высказывания некоторых гистологов о том, что волокна соединительной ткани могут быть образованы не только соединительнотканными клетками, но и всеми структурами мезодермального происхождения, в том числе гладкомышечными и поперечнополосатыми волокнами [Даблин (Dablin, 1946)]. М. Ф. Глазунов (1933, 1934) доказал образование аргирофильных волокон в виде тончайшей войлокообразной сети на поверхности протоплазмы клеток в опухоли из поперечнополосатой мускулатуры и в новообразовании из гладкомышечных элементов.
Мы, так же как М. Ф. Глазунов (1947), допускаем, что мышечные волокна обладают фибриллогенетической способностью, что связано с генетическим родством соединительнотканных и мышечных волокон в смысле их единой мезенхимальной природы.
Даже сторонники эктоплазматической теории образования волокнистых структур соединительной ткани принимают положение о фибриллогенетической способности мышечных элементов (Г. В. Ясвоин, 1935).
А. А. Заварзин (1947) указывает, что «образование опорных структур является элементарным свойством животной клетки, и притом не только соединительнотканной, но и эпителиальной». Н. Г. Хлопин (1946) считает «способность к образованию межклеточных веществ — одним из элементарных свойств живой протоплазмы, быть может, одной из форм ее взаимодействия с окружающей средой». Он указывает, что «аргирофильные волокна могут быть образованы клетками различного происхождения, а не только производными мезенхимы».
Особенно интересно то, что в эксплантате из мускулатуры сердца отмечается новообразование решетчатых волокон (В. Цымбал, 1938).
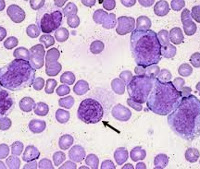
Миелофиброз – это хроническое гематологическое заболевание, характеризующееся опухолевой пролиферацией гемопоэтических стволовых клеток и фиброзом костного мозга. Основные клинические проявления включают симптомы опухолевой интоксикации и анемического синдрома (прогрессирующую слабость, бледность кожи и слизистых оболочек, потерю веса), а также увеличение селезенки (спленомегалию). Диагноз устанавливается на основании молекулярно-генетических исследований, изучения гистологической картины костного мозга. Лечение проводится с помощью химиотерапевтических препаратов. Хирургические методы лечения подразумевают трансплантацию костного мозга и удаление селезенки.
МКБ-10
Общие сведения
Миелофиброз (агногенная миелоидная метаплазия, сублейкемический миелоз) – злокачественное заболевание, при котором происходит постепенное замещение костного мозга опухолевыми стволовыми клетками и разрастающейся соединительной тканью. Впервые эту патологию описал немецкий врач Г. Хойк в 1879 году. А в 1951 году американским гематологом Уильямом Дамешеком миелофиброз был выделен в самостоятельную нозологическую единицу. При неблагоприятном течении миелофиброз способен трансформироваться в более тяжелую болезнь ‒ острый лейкоз. Распространенность миелофиброза составляет от 0,3 до 0,7 случаев на 100 тыс. населения. Пик заболеваемости приходится на возраст от 50 до 70 лет, но встречаются и молодые пациенты. Чаще страдают мужчины.
Причины миелофиброза
Существует первичный и вторичный сублейкемический миелоз. Точная причина первичного миелофиброза до сих пор не установлена. Наибольшей популярностью среди специалистов в области гематологии пользуется теория влияния генетической мутации. У большинства пациентов выявляются мутации гена тирозинкиназы (JAK2V617F), кальретикулина (CALR), тромбопоэтина (MPL), регулирующих экспрессию белков JAK-STAT сигнального пути. Гены локализуются в локусе хромосомы del3p24.
В качестве этиологического фактора изучается действие большой дозы радиоактивного излучения. Также рассматривается роль персистирующих вирусных инфекций (вируса простого герпеса, Эпштейна-Барра, цитомегаловируса), длительного приема оральных контрацептивов, миелосупрессивных лекарственных препаратов, контакта с различными органическими и неорганическими соединениями (бензолом, мышьяком). Вторичный миелофиброз развивается как исход других хронических миелопролиферативных заболеваний – истинной полицитемии, эссенциальной тромбоцитемии, хронического миелолейкоза.
Патогенез
В результате повышенной экспрессии сигнальных белков в одной из стволовых костномозговых клеток запускается активная пролиферация (опухолевая трансформация). Этот процесс сопровождается вторичным воспалением с выделением цитокинов и факторов роста. Факторы роста фибробластов и эндотелия сосудов индуцируют выработку стромальными клетками костного мозга большого количества коллагена и разрастание соединительной ткани (собственно фиброз). Постепенно нормальная ткань костного мозга замещается опухолью и соединительной тканью.
При массивном поражении опухолью костного мозга клетки крови, не достигнув стадии полного созревания, попадают в системный кровоток. Это приводит к образованию очагов экстрамедуллярного (внекостномозгового) кроветворения, главным образом в печени и селезенке. Распад опухоли ведет к высвобождению мочевой кислоты, которая откладывается в тканях суставов и почечных канальцах.
Симптомы миелофиброза
Длительное время пациент чувствует себя удовлетворительно. Через несколько лет от начала заболевания постепенно появляется опухолевая интоксикация в виде общей слабости, повышения температуры до субфебрильных цифр, потливости, усиливающейся по ночам. У больного снижается аппетит, он стремительно теряет в весе. Присоединяется анемический синдром (бледность кожных покровов, головокружение, учащение сердцебиения). Характерны носовые, десневые кровотечения, геморрагические высыпания на коже. Возникают боли в суставах, кожный зуд, боли в костях.
Пациент ощущает тяжесть и боли в левом подреберье вследствие выраженного увеличения селезенки. На фоне спленомегалии развивается синдром гиперспленизма, который заключается в массивном разрушении клеток крови (в основном эритроцитов) в синусоидах селезенки. В этом случае встречаются признаки гемолиза (желтушность кожи, слизистых оболочек, потемнение мочи).
Редкие симптомы связаны с необычной локализацией очагов экстрамедуллярного кроветворения – в легких (кашель, затруднение дыхания, кровохарканье), желудочно-кишечном тракте (боли в животе, кровавая диарея). При расположении очагов в центральной и периферической нервной системе наблюдаются эпилептические судороги, нарушения чувствительности, слабость движений в конечностях, вплоть до полного паралича.
Осложнения
При миелофиброзе часто образуются тромбы, которые приводят к острому нарушению мозгового кровообращения, инфаркту миокарда, тромбоэмболии легочной артерии. Стойкое снижение уровня лейкоцитов нередко сопряжено с различными инфекциями, приобретающими тяжелое течение. Наиболее неблагоприятным осложнением считается трансформация миелофиброза в миелолейкоз (бластный криз), трудно поддающийся терапии. К нетипичным осложнениям следует отнести патологические переломы из-за деструкции трубчатых костей и портальную гипертензию, причиной которой служит длительная обструкция микротромбами внутрипеченочных вен.
Диагностика
Курацией пациентов с миелофиброзом занимаются врачи-гематологи. При общем осмотре обращает на себя внимание изменение цвета кожных покровов, слизистых (бледность или желтушность), спленомегалия при пальпации и перкуссии селезенки, иногда достигающей гигантских размеров (до лобкового симфиза). Дополнительные методы диагностики включают:
Для достоверной постановки диагноза гематологическим сообществом разработаны специальные критерии. Большие критерии включают повышенную клеточность костного мозга с ретикулярным и коллагеновым фиброзом, наличие мутаций генов JAK2V617F, MPL, CALR. К малым критериям относятся анемия, спленомегалия, лейкоэритробластоз (присутствие в крови незрелых форм лейкоцитов, эритроцитов), а также повышение лактатдегидрогеназы. Диагноз считается подтвержденным, если имеются 2 больших критерия или 1 большой и 3 малых критерия.
Миелофиброз следует дифференцировать в первую очередь с гематологическими заболеваниями, такими как аутоиммунные гемолитические анемии, гемобластозы (лейкозы, лимфомы). Сочетание спленомегалии с симптомами интоксикации (слабостью, субфебрилитетом, ночной потливостью) требует исключения туберкулеза, подострого инфекционного эндокардита.