микроценоз у женщин это что
Состояние микробиоценоза влагалища, бактериальный вагиноз и возможности его лечения
Опубликовано в журнале:
«CONSILIUM MEDICUM», 2013, ТОМ 15, № 10, с. 22-24
А.В.Ледина, В.Н.Прилепская
ФГБУ Научный центр акушерства, гинекологии и перинатологии им. В.И.Кулакова Минздрава РФ
Бактериальный вагиноз (БВ) – широко распространенное патологическое состояние, встречающееся у женщин детородного возраста, которое включает комплекс изменений вагинального биотопа, характеризующегося снижением количества нормальной кислородпродуцирующей лактофлоры и повышением концентрации других микроорганизмов, особенно грамотрицательных анаэробов типа Prevotella Porphyromonas spp., Peptostreptococcus spp., Fusobacterium spp., Mobiluncus spp. и GV [5, 18].
Известно, что микрофлора влагалища здоровых женщин репродуктивного возраста представлена широким спектром микроаэрофилов, а также факультативных и облигатных анаэробов [4], присутствие которых не нарушает нормального состояния, не вызывает развития воспалительной реакции и патологических симптомов, характерных для вульвовагинита или БВ. В основном нормальная микрофлора представлена микроорганизмами рода Lactobacillus spp. – микроаэрофильными, продуцирующими перекись водорода палочками (71–100%), реже – анаэробными грамположительными палочками (5–30%).
Кроме лактобактерий, микроаэрофильная флора влагалища здоровых женщин представлена Gardnerella vaginalis (по данным разных авторов, в 6–60% случаев), а также включает облигатные анаэробы Peptostreptococcus spp. (30–90%), грамположительные анаэробные кокки, грамположительные палочки – строгие анаэробы Bifidobacterium spp. (у здоровых женщин примерно в 12% случаев), Clostridium spp. (10–25%), Propionibacterium spp. – P. acnes (до 25%), значительно реже выявляются Mobiluncus spp. (0–5%). Все эти микроорганизмы являются типичными представителями нормальной микрофлоры генитального тракта.
В нормальном биотопе также могут обнаруживаться грамотрицательные строго анаэробные палочковидные бактерии бактероиды Bacteroides spp.: B. urealyticum, B. fragilis, B. vulgatus, B. ovatus, B. distasonis, B. uniformis, B. coccae, B. multiacidus (9–13%), Fusobacterium spp. (14–40%), Porphyromonas spp. (31%), Prevotella spp. (60%) и генитальные микоплазмы M. hominis, U. urealyticum (у 2–15% сексуально активных женщин).
Из представителей факультативных анаэробных микроорганизмов часто выделяют каталазопозитивные, коагулазонегативные Staphylococcus epidermidis, новобиоцинрезистентные Staphylococcus saprophyticus, Streptococcus spp. Это стрептококки группы viridans – «зеленящие» (а или g), гемолитические, стрептококки серологической группы В (Streptococcus agalactie), стрептококки серологической группы D (энтерококки); непатогенные коринебактерии – Corynebacterium minutissimum, C. equi (новое название – Rhodococcus equi), C. aquaticum, C. xerosis; Escherichia coli.
Микробиоценоз влагалища при БВ характеризуется резким снижением уровня перекись продуцирующих лактобактерий, вплоть до их полного исчезновения, и замещением их гарднереллами, которые способствуют росту колоний аэробных и анаэробных микроорганизмов. Кроме G. vaginalis, характерными представителями микрофлоры при БВ являются Prevotella spp., Porphyromonas spp., Bacteroides spp., Peptostreptococcus spp., Mycoplasma hominis, Ureaplasma urealyticum, Mobiluncus spp., а также Fusobacterium spp. и Atopobium vaginae.
Концентрация микроаэрофильных бактерий (G. vaginalis) при БВ может повышаться в сотни раз, а анаэробных микроорганизмов Bacteroides spp., Peptococcus spp. – в тысячи раз и более [1, 9]. В некоторых случаях на фоне абсолютного преобладания микроорганизмов, ассоциированных с БВ, могут присутствовать и лактобактерии в низком титре, но, как правило, это анаэробные лактобактерии, неспособные продуцировать перекись водорода.
В сложной цепи патогенеза различных заболеваний женских половых органов существенная роль отводится иммунным реакциям организма. Снижение неспецифической резистентности у пациенток с БВ [2], а также то, что до 90% G. vaginalis находятся на поверхности вагинального эпителия в виде биопленок [21], способствует росту резистентности анаэробной вагинальной флоры [13] к современным лекарственным препаратам и длительному рецидивирующему течению патологического процесса.
Клиника
Основными клиническими проявлениями БВ являются гомогенные выделения из влагалища, пенистые, слегка тягучие, белого или серого цвета со специфическим «рыбным» запахом. Другие жалобы, такие как зуд, дизурические расстройства, диспареуния, встречаются реже, могут совсем отсутствовать или появляться периодически. Бессимптомное течение инфекционного процесса наблюдается более чем у 1/2 всех женщин с БВ, и у них какие-либо субъективные жалобы могут вообще отсутствовать [16]. При длительно текущем процессе выделения приобретают желтовато-зеленоватую окраску, становятся более густыми, нередко напоминают творожистую массу, равномерно распределяются по стенкам влагалища без выраженного его воспаления [8].
Наиболее опасны осложнения БВ, которые возникают при беременности, во время родоразрешения (преждевременный разрыв плодных оболочек, хориоамнионит, аномалии родовой деятельности), в послеродовом или послеоперационном периоде в случае оперативного родоразрешения (послеродовый эндометрит). БВ может оказывать неблагоприятное влияние на развитие плода (гипотрофия) или новорожденного (пневмония), поэтому чрезвычайно важным является лечение этого заболевания в период планирования и во время беременности [1].
Диагностика
С 1983 г. и по настоящее время для постановки диагноза БВ применяются критерии, предложенные R.Am-sel и соавт. (1983 г.), которые включают наличие обильных выделений из влагалища с неприятным запахом; появление запаха «гнилой рыбы» при проведении аминного теста; повышение значения pH вагинального содержимого до 4,5; присутствие «ключевых клеток» в мазках, окрашенных по Граму. Диагноз БВ можно поставить в случае выявления 3 из 4 указанных критериев.
Микроскопия вагинального мазка, окрашенного по Граму, – наиболее информативный, достоверный и доступный метод диагностики БВ, который дает возможность объективно оценить состояние вагинальной микроэкологии, причем позволяет оценить не только морфологические особенности и соотношение отдельных компонентов вагинальной микрофлоры, но и получить информацию о состоянии слизистой влагалища и наличии лейкоцитарной реакции [5]. Полимеразная цепная реакция позволяет провести не только типирование, но и количественное определение микроорганизмов в режиме реального времени и в последние годы широко применяется в клинической практике.
Лечение
Успешное лечение БВ, как и любого заболевания, зависит от правильной и своевременной постановки диагноза и проведения патогенетически обоснованной эффективной терапии.
Цель лечения БВ – восстановить нормальную микрофлору влагалища, задержать рост микроорганизмов, не свойственных этому микроценозу. Как правило, на первом этапе лечения для пациентки подбирается терапия, которая обеспечивает высокую концентрацию лекарственного вещества во влагалище, что обусловливает эффективность использования малых доз антимикробного препарата и быстрое купирование симптомов заболевания. Второй этап лечения включает стимуляцию нормальной лактофлоры влагалища за счет применения биологических бактерийных препаратов – эубиотиков и пробиотиков [6].
Основными препаратами для лечения БВ являются метронидазол, клиндамицин и тинидазол. Эти препараты могут применяться как в таблетированной форме для приема внутрь, так и в виде вагинальных таблеток, гелей, свечей. Хотя пероральный путь приема ассоциируется с большей частотой побочных эффектов, он является более приемлемым для большинства пациенток.
Метронидазол рекомендуется назначать в дозе 500 мг 2 раза в день в течение 7 дней или 1-кратно в дозе 2 г, но такой режим считается менее эффективным. При приеме метронидазола могут возникать побочные эффекты со стороны желудочно-кишечного тракта в виде металлического вкуса во рту и тошноты (до 10%), а также транзиторная нейтропения (7,5%), периферическая нейропатия. Тошнота, другие гастроинтестинальные эффекты менее выражены при интравагинальном пути введения метронидазола. Вагинальный гель в дозе 5 г, вводимый ежедневно в течение 5 дней, не уступает по эффективности пероральному пути введения и с успехом может применяться для лечения БВ [17].
Тинидазол – препарат нитроимидазольного ряда, применяется в таблетках по 1 г 1 раз в день в течение 5 дней или по 2 г в течение 2 дней.
Сравнимым по эффективности с метронидазолом, но имеющим меньшее количество побочных эффектов является клиндамицин (Клиндацин ® ) – антибиотик группы линкозамидов, обладающий широким спектром действия, оказывающим в основном бактериостатический эффект. Клиндамицин активен в отношении Staphylococcus spp. (в том числе Staphylococcus epidermidis, продуцирующих пенициллиназу), Streptococcus spp. (исключая Enterococcus spp.), Streptococcus pneu-moniae, Corynebacterium diphtheriae, в отношении споро- и неспорообразующих анаэробов и микроаэрофильных грамположительных кокков (включая Peptococcus spp. и Peptostreptococcus spp.), Clostridium perfringens, Clostridium tetani, Mycoplasma spp., Bacteroides spp. (включая Bacteroides fragilis и Prevotella melaninogenica), Fusobacterium spp., Propionibacterium spp., Eubacter spp., Actinomyces spp., т.е. против большинства микроорганизмов, вызывающих дисбиоз влагалища и БВ.
Предпочтительным режимом является местное применение препарата в течение 3–7 дней. При этом вагинальные суппозитории вводятся по 1 на ночь или 2% вагинальный крем при помощи аппликатора (5 г) на ночь 3–7 дней. Перорально клиндамицин назначается 2 раза в день по 300 мг в течение 7 дней.
Местный клиндамицин является наиболее эффективным по сравнению с метронидазолом препаратом при лечении рецидивирующего БВ, особенно ассоциированного с A. vaginae; клиническое излечение при его применении наступает в 83,3% случаев (рПобочные эффекты (псевдомембранозный колит, тошнота) при приеме клиндамицина встречаются редко, что значительно повышает комплаентность терапии.
Применение клиндамицина (Клиндацин ® ), что очень важно, возможно при беременности или в подготовительном к родам периоде (только местно) в обычных терапевтических дозировках.
Эффективность, быстрое достижение положительного результата лечения, хорошая переносимость клиндамицина при лечении, в том числе беременных женщин, доказана при проведении многочисленных рандомизированных плацебоконтролируемых сравнительных клинических исследований [1, 7, 14].
Вторым этапом лечения, а также с целью профилактики рецидивов БВ назначаются эубиотики, пробиотики, которые могут применяться в комплексе с антибактериальными препаратами или как основное средство лечения. В первом случае назначение пробиотиков целесообразно проводить не ранее чем через 3 дня после окончания антибактериальной терапии БВ в виде интравагинальных суппозиториев; длительность лечения должна составлять менее 7–10 дней [6, 12].
После проведенного лечения примерно у 1/3 пациенток возникает рецидив заболевания в течение первых 3 мес, а более чем у 1/2 симптоматика возобновляется в течение 12 мес [19, 20]. Это вероятнее всего происходит в связи с неэффективностью проведенного лечения, так как от 65 до 80% [15] патогенов находится в составе биопленок, матрикс которых может связывать или не пропускать, и/или инактивировать антибиотики [3, 10, 11] и приводить к снижению эффективности лечения. Другой возможной причиной частых рецидивов является то, что не происходит достаточно полного восстановления нормальной микрофлоры влагалища и на этом фоне вновь активизируется патогенная микрофлора [12, 23].
Вопрос о целесообразности назначения лечения партнерам женщин, получающих лечение по поводу БВ, не решен. Ряд исследователей считают, что лечение половых партнеров не влияет на успешность терапии, хотя доказана роль половых контактов в возникновении и рецидивировании БВ. Кроме того, показана эффективность использования презервативов в снижении частоты рецидивов БВ [22]. Но поскольку доказательная база для окончательных выводов остается недостаточной, для решения этой задачи необходимы новые исследования.
Таким образом, БВ, представляющий дисбиотическое состояние экосистемы влагалища, является достаточно распространенной в современной популяции патологией, требующей своевременной диагностики, комплексной адекватной терапии и профилактики. Препаратом, оказывающим быстрое положительное действие и обладающим хорошей переносимостью, а также разрешенным к применению во время беременности, является клиндамицин (Клиндацин ® ). Высокая эффективность, доказанная клиническими исследованиями, позволяет использовать Клиндацин ® в клинической практике как один из основных препаратов для лечения БВ.
Индекс лекарственного препарата: Клиндамицин: Клиндацин ® (Акрихин ОАО)
Диагностика и варианты комплексного лечения нарушений микроценоза влагалища: клинические и микроэкологические направления
Опубликовано в журнале:
«ЗДОРОВЬЕ ЖЕНЩИНЫ», 2009, №5 (41) с. 90-93
П.В.Буданов
Московская медицинская академия имени И.М. Сеченова
В статье приведены современные критерии диагностики нарушений микроценоза влагалища и трихомониаза. Обследованы 214 больных с нарушениями микроценоза влагалища, получавших комплексное лечение с применением комбинированного препарата Полижинакс. В результате исследования показано, что эффективность комплексного лечения нарушений микроценоза влагалища с использованием данного препарата составила 92,52%. Полижинакс не влияет на количество лактобацилл, обладает хорошей переносимостью. Применение на втором этапе лечения дисмикробиоценоза влагалища препаратов про- и эубиотиков приводит к повышению эффективности терапии и снижению частоты рецидивов. Для лечения 76 больных с трихомонадным кольпитом использовали селективный трихомонацидный препарат тенонитрозол (Атрикан 250), который позволяет добиться клинического и микробиологического выздоровления при лечении неосложненных форм урогенитального трихомониаза у 96,05% пациенток.
Ключевые слова: трихомониаз, бактериальный вагиноз, кандидоз.
В настоящее время для инфекционных заболеваний женских половых органов характерна смешанная этиология, стертая или бессимптомная клиническая картина, высокая частота микст-инфекций и склонность к рецидивированию.
Нарушения микроценоза влагалища встречаются у 45–86% больных гинекологических стационаров. Они являются причиной инфекционных осложнений после хирургических вмешательств на органах малого таза, способствуют возникновению воспалительных заболеваний внутренних половых органов. Повреждая биологический барьер, они увеличивают в несколько раз вероятность инфицирования возбудителями, передаваемыми половым путем [8].
Подавляющее большинство инфекционных заболеваний влагалища и шейки матки являются вариантами нарушения микроценоза. Так, бактериальный вагиноз (БВ), генитальный кандидоз (ГК) и трихомонадный вагинит составляют более 90% всех вагинальных инфекций [3].
В настоящее время подробное изучение культуральных и биохимических свойств представителей влагалищного биотопа привело к трансформации знаний о вариантах нарушений нормоценоза влагалища и его инфекционной патологии [3, 7].
Термин «нормоценоз» отражает типичное состояние нормального биотопа влагалища (преобладание лактобактерий, отсутствие грамотрицательной микрофлоры, спор, мицелия, псевдогифов, лейкоцитов, неизмененные эпителиальные клетки). «Промежуточный тип» биоценоза влагалища является пограничным типом, редко сопровождается субъективными симптомами и клиническими проявлениями (сниженное количество лактобактерий, наличие грамположительных кокков, грамотрицательных палочек). «Дисбиоз» влагалища соответствует микробиологической картине бактериального вагиноза (минимальное количество или полное отсутствие лактобактерий, полиморфная грамотрицательная и грамположительная палочковая и кокковая микрофлора, наличие ключевых клеток). «Вагинит» соответствует неспецифическому вагиниту (преобладание лейкоцитов над эпителиоцитами; повышенная эксфолиация эпителиоцитов; обнаружение трихомонад, псевдомицелия, спор грибов). При обнаружении трихомонад, мицелия, псевдогифов, спор определяется соответствующий этиологический диагноз.
Наряду с этим сопоставление бактериального вагиноза с неспецифическим кольпитом или промежуточным типом микроценоза влагалища и назначение антибактериальной терапии без учета патогенеза заболевания в большинстве наблюдений не обеспечивает положительного эффекта, а приводит к потенцированию патологического процесса.
Существование экосистемы влагалища предполагает наличие как в норме, так и при патологии нескольких видов микроорганизмов, представляющих его биотоп. Таким образом, классический постулат «один микроб – одно заболевание» не находит подтверждения даже при специфических инфекциях. При бактериологическом исследовании выявляются полимикробные ассоциации, включающие как бактерии, так и простейшие, вирусы, меняющиеся при инфекционных заболеваниях (вторичная экологическая сукцессия), а также на протяжении всей жизни женщины. В понимании механизмов естественного барьера для инфекционных осложнений наиболее важен термин «колонизационная резистентность влагалищного биотопа». Это своего рода совокупность механизмов, поддерживающих стабильность популяционного и количественного состава компонентов нормального микроценоза.
Собственный опыт диагностики, лечения, оценки эффективности и наблюдения отсроченных результатов различной терапии более 300 случаев бактериального вагиноза, генитального кандидоза, трихомониаза, уреаплазмоза и микоплазмоза в различных возрастных группах женщин, в том числе у беременных, показал, что частота положительных результатов лечения зависит не только от качества проведения этиотропной терапии и элиминации возбудителя, а главным образом от восстановления нормальной микрофлоры влагалища.
Доказано, что на фоне промежуточного типа микроценоза влагалища в среднем в течение 1–2 мес развивается та или иная форма вагинальной инфекции. Следовательно, промежуточный тип микроценоза следует рассматривать как патологическое состояние биотопа влагалища. В этом случае нарушение колонизационной резистентности влагалища является значимым фактором риска развития инфекций, передаваемых половым путем (ИППП), и ассоциированных с ними осложнений. Проведение коррекции промежуточного типа влагалищного микроценоза с помощью комбинированных антибактериальных/антимикотических препаратов в сочетании с препаратами про- и эубиотиков позволяет снизить частоту возникновения нарушений микроценоза влагалища, ИППП и связанных с ними осложнений.
В лечении неспецифического кольпита главное место занимают местные комбинированные средства с противопротозойным, противомикробным и противогрибковым действием. Следует отметить, что некоторые авторы предлагают после комплексного бактериологического исследования выделять ведущего возбудителя и воздействовать на него с помощью специфических антибактериальных препаратов [7].
Также имеются данные об эффективности комбинированных местных препаратов в лечении бактериального ваги-ноза [2, 5]. Кроме того, многие авторы отдают предпочтение комбинированным препаратам, включающим антимикотики [4–6].
Таким образом, высокий риск возникновения генитальных инфекций на фоне промежуточного типа микроценоза влагалища и патогенетическая обоснованность проведения комплексной терапии неспецифического кольпита приводят к необходимости выбора комбинированного антибактериального и фунгицидного препарата для местного применения с минимальным резорбтивным действием. В то же время такой препарат не должен обладать выраженной антибактериальной активностью, сопоставимой с метронидазолом и клиндамицином. Назначение подобных антибиотиков при рассматриваемых вариантах нарушений микроценоза влагалища приводит к образованию порочного круга «антибиотик – кандидоз – антимикотик – рецидив – нарушения микроценоза влагалища – системная терапия – изменение микроэкологии влагалища».
В связи с этим целью настоящей работы явилось изучение эффективности комбинированного препарата Полижи-накс в комплексной терапии неспецифического кольпита и промежуточного типа микроценоза влагалища.
Препарат Полижинакс состоит из трех компонентов: двух бактерицидных антибиотиков (неомицина и полимиксина В), и полиенового антигрибкового препарата – нистатина. Неомицин – аминогликозид широкого спектра действия, оказывающий бактерицидное действие, он активен в отношении многих грамотрицательных и грамположительных микроорганизмов, в том числе E. Coli, Shigella spp., Proteus spp., S.aureus, Enterobacter spp., Haemophilus influencae, Klebsiella pneumoniae. Полимиксин В – это антибиотик полипептидной структуры, активный в отношении большинства грамотрицательных бактерий.
Обследованы 214 женщин в возрасте от 17 до 54 лет. На основании клинических данных, расширенных критериев микроскопии, выявления возбудителей группы ИППП у всех пациенток были обнаружены изолированные или сочетанные нарушения микроценоза влагалища. В комплексе проводимого лечения Полижинакс использовался интравагинально 2 раза в сутки в течение 10 дней с последующим назначением пробиотиков (живые лиофилизированные лактобациллы и вагинальные штаммы живых лактобацилл). При обнаружении ИППП осуществляли специфическую антибактериальную терапию.
Учитывая высокую частоту бессимптомных форм дисмикробиоценоза влагалища, полученные результаты оценивали на основании данных динамического микробиологического исследования.
После проведенного лечения контролировали скорость элиминации возбудителя, наличие рецидивирования и суперинфекции. Так, при наличии бактериального вагиноза через день после окончания курса лечения проводился микробиологический контроль для оценки эффективности и определения условий для назначения второго этапа терапии. Контроль повторяли через семь дней после второго этапа терапии, а в последующем – каждые два месяца при отсутствии жалоб и клинических проявлений заболевания.
Пациенткам с БВ, ГК, неспецифическим кольпитом и промежуточным типом микроценоза влагалища выполняли контрольные микробиологические исследования: на первый, третий, пятый день курса лечения и через неделю после его окончания.
Отмечено, что к пятым суткам лечения у 65% пациенток в мазках отсутствовали «ключевые клетки». При этом полная элиминация ассоциированных с БВ микробных агентов достигалась только к концу второго этапа терапии.
Следует подчеркнуть, что даже при снижении исходного уровня Lactobacillus spp. (до начала лечения) на фоне терапии Полижинаксом их количество не уменьшалось. Это выгодно отличает данный препарат от других антибактериальных агентов, используемых для лечения нарушений микроценоза влагалища.
При генитальном кандидозе оценка эффективности проводимой терапии включала определение срока исчезновения жалоб, нормализации клинической картины, микробиологического выздоровления, частоты и времени возникновения рецидивов (табл. 1).
Таблица 1. Клиническая эффективность Полижинакса для местного лечения вагинального кандидоза
| Срок, сутки | Отсутствие клиники воспаления, суток | Частота рецидивов, % (n) | |
| Исчезновение жалоб | Исчезновение белей | ||
| 4 | 9 | 8 | 13,08 (28) |
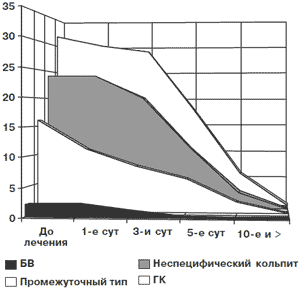
При использовании Полижинакса в составе комплексного лечения нарушений микроценоза влагалища уже к середине курса наступает клиническое улучшение. Уменьшение количества лейкоцитов в вагинальном мазке начинается с первых суток лечения и достигает нормальных значений после шести дней лечения (рис. 1). Однако процесс уменьшения и полного исчезновения патологических выделений происходит медленнее. Другими словами, при БВ клинический эффект от лечения достигается раньше, чем микробиологическое выздоровление, а при ГК – наоборот.
Рис. 1. Динамика лейкоцитарной реакции вагинального мазка
| До лечения | 1-е сутки | 3-и сутки | 5-е сутки | 10-е сутки и далее | |
| БВ | 2 | 2 | 1 | 0 | 0 |
| Промежуточный тип | 16 | 11 | 8 | 6 | 2 |
| Неспецифический кольпит | 24 | 24 | 20 | 11 | 3 |
| ГК | 32 | 30 | 29 | 18 | 6 |
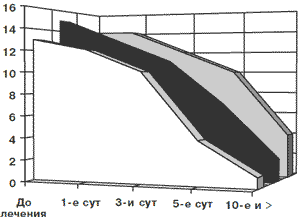
Активность элиминации патогенных грибов прогрессивно увеличивается (рис. 2), а снижение общей бактериальной обсемененности выражено в середине курса лечения этим препаратом (рис. 3).
Рис. 2. Частота обнаружения спор/псевдомицелия грибов Candida spp. на фоне лечения Полижинаксом
| До лечения | 1-е сутки | 3-и сутки | 5-е сутки | 10-е сутки и > | |
| БВ | 14 | 6 | 1 | 0 | 0 |
| ГК | 13 | 12 | 10 | 4 | 1 |
| Промежуточный тип | 15 | 13 | 11 | 7 | 2 |
| Неспецифический кольпит | 14 | 14 | 12 | 10 | 4 |
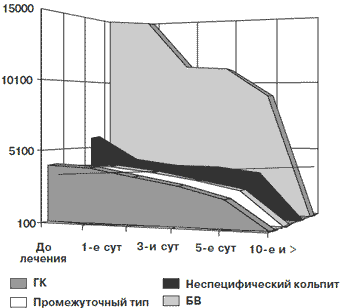
Рис. 3. Изменение общей бактериальной обсемененности вагинального мазка на фоне использования Полижинакса
| До лечения | 1-е сутки | 3-и сутки | 5-е сутки | 10-е сутки и > | |
| ГК | 4100 | 3960 | 3410 | 2809 | 2050 |
| Промежуточный тип | 3890 | 3890 | 3505 | 3010 | 2400 |
| Неспецифический кольпит | 5860 | 4160 | 3830 | 3710 | 3440 |
| БВ | 14980 | 14800 | 11300 | 11050 | 9000 |
В качестве монотерапии Полижинакс был использован при умеренном дефиците или нормальном количестве лактобацилл в составе вагинального отделяемого. При этом эффективность его применения достигала 87,85%.
В составе комбинированной терапии нарушений микроценоза влагалища эффективность назначения Полижинакса достигала 92,52%. Нами не отмечено побочных проявлений препарата, но подтверждена его хорошая переносимость.
Одним из широко распространенных заболеваний мочеполового тракта является трихомониаз. Очень часто трихомонадная инфекция сочетается с бактериальной или вирусной патологией половых путей женщины [1]: с БВ достигает 32%, с ГК – 17%. По нашим данным, трихомонадный вагинит в виде моноинфекции встречается у 12–28% больных.
При отсутствии микст-инфекции назначение препаратов с выраженной анаэробной активностью (тинидазол и орни-дазол) приводит к подавлению лактобациллярной флоры и, несмотря на элиминацию возбудителя, способствует повреждению биологического барьера – нормального микроценоза влагалища. То же относится к препаратам с трихомонацидным действием для местного применения, так как они содержат метронидазол или тернидазол. Кроме того, местное лечение урогенитального трихомониаза в виде монотерапии достигает клинического и микробиологического эффекта всего в 40–73% наблюдений.
В связи с этим наиболее актуальным представляются поиск и применение антипротозойного препарата с высокой избирательностью воздействия на урогенитальные трихомонады. Эти простейшие являются самостоятельным видом, морфологически и культурально отличающимся от ротовых и кишечных трихомонад.
Для выяснения эффективности лечения моноинфекции, вызванной Trichomonas vaginalis, и влияния трихомонацидного препарата на состояние молочнокислого ростка влагалищного биотопа проведено обследование 76 больных женщин детородного возраста.
У всех пациенток первичная диагностика трихомониаза осуществлена на основании данных микроскопии нативного мазка и мазка, окрашенного по Граму. Причем микроскопию нативного мазка проводили в течение 1–3,5 мин после взятия материала. Наибольшая частота обнаружения влагалищной трихомонады отмечена при проведении нативной микроскопии, когда возбудитель определялся по его характерным толчкообразным движениям среди клеточных элементов и микроорганизмов. При микроскопии окрашенных препаратов тех же больных обнаруживали трихомонады, имеющие грушевидную, овальную, круглую форму с четкими контурами и асимметрично расположенным ядром.
До начала лечения исключали нарушения микроценоза влагалища и ИППП.
Все больные получали курс лечения тенонитрозолом по 250 мг 2 раза в сутки перорально во время еды в течение четырех дней (препарат Атрикан 250). Также обследование и лечение проводили половым партнерам. Для контроля эффективности лечения использовали данные бактериоскопического и культурального методов.
В качестве критериев излеченности рассматривали отсутствие клинических проявлений, элиминацию возбудителя по данным микроскопии и культурального метода из влагалища, мочеиспускательного канала, прямой кишки, нормальные показатели клинического и лабораторного обследования через 3 мес после проведенного лечения.
Клиническая и микробиологическая эффективность при лечении неосложненных форм урогенитального трихомониа-за с помощью тенонитрозола (Атрикан 250) достигла 96,05%.
На фоне применения избирательного антипротозойного препарата тенонитрозола не отмечено снижения количества лактобацилл по сравнению с исходным уровнем. Кроме того, общее количество Lactobacillus spp. достигало титра 105–107 КОЕ•мл-1 в среднем через (12,41±4,4) дня после окончания лечения без применения препаратов эубиотиков.
Таким образом, полученные данные свидетельствуют о высокой эффективности использования комбинированных антимикробных препаратов (Полижинакс) на начальных этапах развития инфекционного процесса и формирования патогенных микробных ассоциаций. Включение в состав комплексной терапии нарушения микроценоза влагалища препаратов пробиотиков (эубиотиков), обеспечивающих повышение колонизационной резистентности влагалищного биотопа, позволяет повысить эффективность лечения и увеличить продолжительность безрецидивного промежутка.
При урогенитальном трихомониазе, проявляющемся в виде моноинфекции, высокой эффективностью обладает тенонитрозол (Атрикан 250). Применение данного антипротозойного препарата позволяет добиться полного клинического и микробиологического выздоровления. Кроме того, он не оказывает отрицательного влияния на состав нормальной микрофлоры влагалища, что является положительным результатом.