мифепристон чем опасен для ребенка
Мифепристон в родах
Дорогие мамы, недавно мне задали вопрос о применении Мифепристона в родах. Хочу сегодня обсудить с вами эту тему, так как считаю, что для мамы очень важно быть осведомленной касательно разных препаратов, применяемых врачами во время родов, ведь от этого зависит течение родов и рождение вашего малыша! Никогда не забывайте, что даже в роддоме у вас есть право просить то, что вы считаете нужным и отказываться от того, что, по вашему мнению, может навредить. Мы уважаем врачей и доверяем им свою жизнь и жизнь малыша. Но, давайте будем помнить о том, что мы должны слушать свое тело и доверять интуиции. А также, очень полезным будет изучить тему самых распростаненных манипуляций и препаратов во время родов. Чем мы сегодня и займемся.
МИФЕПРИСТОН И ПОДГОТОВКА ШЕЙКИ К РОДАМ.
Мифепристон – один из препаратов, который применяется в нашей стране для вызывания родов. Это 2 таблетки, которые даются маме с определенным интервалом. Обязательно с назначением врача и КТГ-мониторингом сердцебиения ребенка. Это называется преиндукция родов (подготовка шейки матки) и проводится только в медицинских учреждениях.
⠀
В нашей стране – средство выбора при недостаточно зрелой шейке матки, включен в протокол. По мнению авторов русскоязычных исследований: по сочетанию эффективность/побочные эффекты мифепристон оптимален.
⠀
В некоторых западных стран мифепристон не используется для индукции на живых младенцах из-за возможных последствий, только для медикаметозных абортов и в случае гибели ребенка.
⠀
В России есть врачи, которые не применяют мифепристон для преиндукции родов, как раз из-за высоких рисков для ребенка. Есть мнение, что мифепристон дает плацентарные нарушения, вызывает периферический спазм сосудов, и это приводит к гипоксии. Достаточно часто при его применении встречается излитие мекониальных вод. Про последствия для матери подробно в Википедии, здесь цитировать не буду.
Я попросила уважаемого мной доктора, Галину Клименко, прокомментировать применение мифепристона (она использует его в своей практике), ниже весь текст от нее, дочитайте до конца. Мне очень близок вывод.
МНЕНИЕ ДОКТОРА
Мифепристон – антипрогестогенный препарат, который блокирует чувствительные к прогестерону рецепторы и приводящий к прекращению беременности.
⠀
Несмотря на множество печатных работ о минимальных рисках развития дискоординации, рисков кесарева сечения и осложнений в виде гипоксии плода, в применении метода есть множество ограничений – они же противопоказания:
⁃ Почечная и печеночная недостаточность
⁃ Несоответствие размеров таза матери и головки плода: здесь следует остановится подробнее, т.к. этот диагноз ставится только в родах, но заподозрить можно и ранее: либо по данным МР пельвиометрии, либо по наличию анатомически узкого таза и крупного плода и высоко стоящей головке!
⁃ Неправильные положения и предлежания плода: поперечное, косое, тазовое и др.
– Аномалии расположения плаценты
– Рубец на матке
– Опухоли матки, препятствубщие рождению плода
– Тяжелая преэклампсия
– Нарушения состояния малыша по ктг
– Кровяные выделения из половых путей неясного генеза
– Хориоамниотит
На использование мифепристона необходимо получить информированное согласие пациентки!
Из возможных осложнений: тошнота, рвота, диарея, головная боль, крапивница, слабость, гипертермия. По сравнению с другими методами несколько чаще отмечается преждевременное излитие околоплодных вод!
Теперь хотелось бы обсудить, почему у метода подготовки к родам и индукции родов так много противников? Все очень просто: роды – это сложный естественный процесс, любое вмешательство в который может привести к целому каскаду последующих действий и увести нас очень и очень далеко от физиологии. Поэтому, дорогие мои, не забываем, что беременность – процесс физиологический, длиться он может в норме до 42 недель. Поэтому при хорошем самочувствии мамы и малыша (узи, допплерометрия, оценка количества околоплодных вод, КТГ до нескольких раз в день на 42 неделе) – чаще всего лучше просто подождать, применяя так называемое активное наблюдение, т.е. постоянно контролируя маму и малыша.
Сложно ли это для врача?
Очень сложно и очень ответственно. Иногда ожидание родов затягивается на 1-2 недели и это каждый раз очень беспокоит вашего акушера-гинеколога. Но, иногда роды необходимо все же приблизить по показаниям со стороны мамы или малыша.
Итак, кому показана индукция, или “вызов” родовой деятельности до срока ее самостоятельного начала?
ЕСТЬ ДВЕ ГРУППЫ ПОКАЗАНИЙ
Со стороны матери:
– Переношенная беременность. Чаще всего говорим о сроке 41-42 недели, но все очень индивидуально!
– Преэклампсия. Важна тяжесть/длительность течения и эффект от проводимой терапии;
– Сахарный диабет, в т.ч. и ГСД;
– Холестатический гепатоз: проблемы характеризующиеся повышением печеночных ферментов, зудом и нарушением свертываемости крови.
Со стороны ребенка:
– Резус-конфликт. Выраженное маловодие в доношенном сроке беременности;
– Тенденция к перенашиванию и признаки нарушения состояния плода (по КТГ и допплерометрии), причем стоит сказать, что признаки должны быть начальными. Потому что если в состоянии ребенка выявлены серьезные отклонения, то лучше всего не проводить индукцию, а ставить вопрос о кесаревом сечении.
Поверьте, друзья мои, вашему врачу гораздо проще и спокойнее приехать ночью на роды, начавшиеся с прекрасных схваток, чем ломать себе голову какой метод преиндукции и индукции родов вам подойдет и какие у этого всего будут последствия.
На мой взгляд это мнение компетентного доктора, согласны вы с ним?
По поводу индукции родов, я, точно, будучи психологом, ничего не советую мамам. Мне важно было дать вам информацию с обеих сторон. Любое вмешательство в умный родовой процесс – это не просто таблеточка, не просто капельница, не просто какй-то укольчик. У всего есть свои побочные эффекты. Любой вид так называемой помощи телу родить, может привести к эффекту домино (шквалу медицинских вмешательств) и неприятным последствиям. Принимайте взвешанное обдуманное решение, учитывая риски и последствия обоих вариантов. Иногда вмешательство спасает жизни, а иногда рушит. И только вам РАЗУМ может отличить одно от другого.
Как научиться слушать свое тело? Как чувствовать себя уверенной в родах, в любой ситуации быть спокойной и принимать решения, которые будут во благо и вам, и малышу?
На курсе по гипнородам у нас есть целый урок, который посвящен ситуациям, когда роды идут не по плану. Помимо этого вы найдете на курсе еще очень много всего полезного и интересного, например техники снижения уровня ощущений в родах и способы натуральной и безопасной стимуляции начала родов, если они не начинаются в срок.
Мифепристон чем опасен для ребенка
В системе Российского здравоохранения важная роль принадлежит охране материнства и детства, созданию наилучших условий для рождения здорового ребенка при сохранении здоровья матери [6, 7]. За последние годы прослеживается тенденция роста возрастных первородящих, частоты акушерских и экстрагенитальных заболеваний, что порой диктует необходимость более ранней медикаментозной подготовки родовых путей к родам [4, 12, 14]. В настоящее время существует достаточно публикаций, свидетельствующих об эффективном применении мифепристона при подготовке родовых путей при доношенном сроке гестации [1, 2]. Кроме того, имеется достаточный опыт применения антигестагенов при переношенной беременности с целью недопущения осложнений как для матери, так и для плода [9].
Однако, несмотря на широкое внедрение клинических рекомендаций и протоколов [1], эффективность применения антигестагенов при целом плодном пузыре и преждевременном разрыве плодных оболочек (ПРПО), по данным литературы, значительно варьирует [3, 5, 8, 11, 13].
В связи с этим целью настоящей работы явилась клиническая оценка эффективности применения мифепристона при подготовке шейки матки к родам при доношенном сроке беременности и различных акушерских ситуациях.
Материал и методы исследования. Работа выполнена на базе перинатального центра ГУЗ «Саратовская городская клиническая больница № 8». Проведен ретроспективный анализ историй родов 250 женщин при сроках гестации 37,2–40,5 недель, у которых исходно имела место «незрелая» шейка матки (3–5 баллов по шкале Bishop). В основной группе подготовка шейки матки к родам проводилась при условии целого плодного пузыря (n=190). В группе сравнения терапия антигестагенами назначалась в связи с преждевременным отхождением околоплодных вод при «незрелой» шейке матки (n=30). Группа контроля представлена беременными, которые не дали согласие на проведение прединдукционной подготовки.
Критерии включения: одноплодная доношенная беременность, головное предлежание плода, удовлетворительное состояние плода по данным КТГ (8–10 баллов).
Критерии исключения: преэклампсия тяжелой степени, наличие рубца на матке, суб- и декомпенсированная плацентарная недостаточность, крупный плод (более 4500 гр.), неправильное положение плода, соматические заболевания матери в стадии декомпенсации, индивидуальная непереносимость препарата.
Оценку состояния родовых путей мы проводили по шкале Е. Bishop (1964) в модификации J. Burnett (1966). Подготовку шейки матки при помощи мифепристона начинали после получения информированного согласия пациентки. В основной группе мифепристон применяли по следующей схеме: первый прием 200 мг per os, повторный прием 200 мг при отсутствии регулярной родовой деятельности через 24 часа. Оценку эффективности проводили через 48–72 часа. При отсутствии спонтанной родовой деятельности после первого этапа подготовки применяли простагландин, содержащий гель или амниотомию в зависимости от степени зрелости шейки матки. Простагландин Е2 (динопростон 0,5 мг) в виде геля в одноразовом шприце в объеме 2,5 мл вводили интрацервикально каждые 6 часов не более 3 доз. В группе сравнения мифепристон назначался при поступлении в родильный блок, повторная доза использовалась при отсутствии эффекта через 6 часов. Оценку эффективности в группе сравнения проводили через 12 часов после первого приема препарата. Обследование беременных проводилось согласно приказу № 572н. Для оценки функционального состояния плода проводили УЗИ с допплерометрией, а также наружное кардиотокографическое исследование перед началом преиндукции родов и в динамике, перед каждым последующим этапом подготовки шейки матки. Статистическая обработка данных проведена с использованием пакета прикладных программ (ППП) Statgraphics (Statistical Graphics System), разработанного фирмой «STSC Inc.».
Результаты исследования. Беременные всех трех групп были сопоставимы по срокам гестации, особенностям акушерско-гинекологического анамнеза, наличию экстрагенитальных заболеваний. Все обследованные женщины находились в активном чадородном возрасте. Средний возраст пациенток основной группы составил 28,2±9,5 лет, в группе сравнения 27,6±10,7 лет и в контрольной группе 25,8±12,6 лет. Доля первородящих женщин в основной группе составила 52,6 %, в группе сравнения – 53,3 % и в контрольной группе – 56,6 %.
Показаниями к назначению мифепристона в основной группе беременных явились: незрелость родовых путей при доношенном сроке беременности, выраженные отеки беременных, изосенсибилизация по резус-фактору, гепатоз с синдромом холестаза и цитолиза, гестационная артериальная гипертензия. В группе сравнения всем пациенткам был назначен мифепристон, учитывая преждевременный разрыв плодных оболочек при доношенном сроке беременности и «незрелой» шейке матки.
В основной группе у 83,2 % женщин (n=158) развилась спонтанная родовая деятельность через 24,2±3,5 часа. В 6,8 % случаях (n=13) была достигнута оптимальная биологическая готовность родовых путей и проведена амниотомия при «зрелой» шейке матки, после чего через 2,5±0,5 часа констатирован I период родов. У 8,9 % пациенток (n=17) отмечался недостаточный эффект от приема антигестагенов, что явилось показанием для проведения 2 этапа подготовки шейки матки простагландин содержащим гелем и, спустя 5,2±0,5 часов, в этой группе женщин зафиксировано начало родового акта. В 2 случаях (1,1 %), в связи с отсутствием эффекта от мифепристона, наличием противопоказаний для назначения динопростона (дисбиоз влагалища) было проведено кесарево сечение в плановом порядке.
В группе сравнения регулярная родовая деятельность развилась у 93,3 % пациенток (n=28) через 6,3±0,7 часов от первого приема мифепристона. В 2 случаях (6,7 %) проведено кесарево сечение, показанием к которому явилось отсутствие эффекта от родовозбуждения при безводном промежутке более 12 часов.
В группе контроля в 70 % наблюдений (n=21) через 5–7 дней развилась спонтанная родовая деятельность, а в 10 % случаев (n=3) была достаточная биологическая готовность родовых путей для проведения амниотомии при сроке 41–41,1 недель, которая оказалось эффективной. У 6 пациенток (20 %) этой группы отсутствовали условия для проведения амниотомии, в результате чего при сроке гестации 41–41,5 недель были родоразрешены путем операции кесарева сечения по неготовности родовых путей к родам.
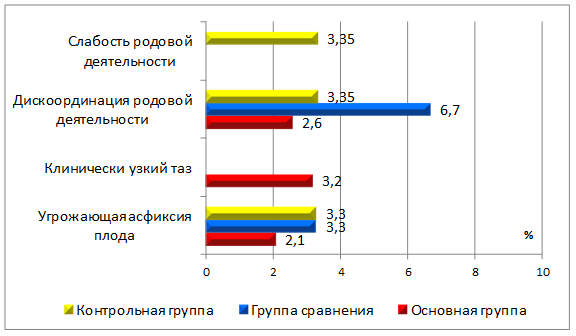
Анализ течения родового акта показал более высокую частоту нарушений сократительной деятельности матки, без отсутствия эффекта консервативной терапии, в контрольной группе и в группе сравнения (рис. 1).
Рис.1. Сравнительный анализ показаний к проведению экстренного кесарева сечения в группах женщин
При этом при ПРПО (группа сравнения) в 2 раза чаще диагностировалась дискоординация маточных сокращений, а упорная слабость родовой деятельности развивалась только при отсутствии подготовки мифепристоном (контрольная группа). В основной группе дискоординированная родовая деятельность, без эффекта от лечения, констатирована только в 5 наблюдениях (2,6 %). Согласно данным литературы, частота аномалий родовой деятельности в группе женщин, которым проводилась подготовка к родам мифепристоном, варьирует от 14 % до 29 % [2, 5].
Среди других осложнений родового акта, которые явились показанием для завершения родов путем операции кесарева сечения в экстренном порядке, следует отметить угрожающую асфиксию плода и клинически узкий таз (рис. 1). Удельный вес острой асфиксии плода в группах достоверно не отличался друг от друга. В то же время признаки клинического несоответствия размеров головки плода и таза матери были установлены лишь в основной группе (n=6).
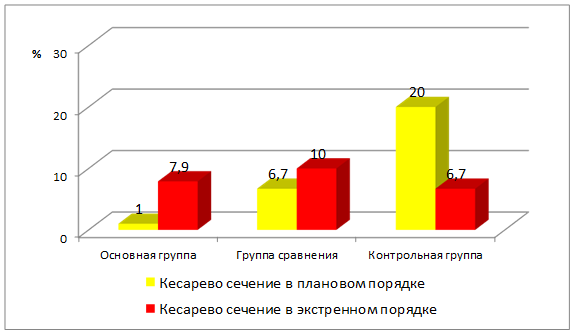
Сравнительный анализ частоты оперативного родоразрешения в экстренном и плановом порядке в зависимости от акушерской ситуации представлен на рис. 2. Суммарно частота операции кесарева сечения в основной группе составила 8,9 %, в группе сравнения – 16,7 %, а в контрольной группе – 26,7 %. О снижении частоты оперативного родоразрешения при использовании мифепристона свидетельствуют многие исследования [2, 5, 10].
Рис. 2. Удельный вес женщин, родоразрешенных оперативным путем
При анализе исходов родового акта в группах обследуемых женщин выявлена более высокая частота акушерского травматизма в контрольной группе: разрывы шейки матки 1 степени встречались в 23,3 % случаев, разрывы промежности 1–2 ст. – в 10 % наблюдений. В то же время в основной группе и группе сравнения частота разрывов шейки матки 1 степени составила, соответственно, 15,8 % и 13,3 %; а разрывов промежности 1–2 степени – 3,2 % и 6,7 %, что, несомненно, меньше аналогичных показателей контрольной группы. При этом средняя масса новорожденных детей в группах достоверно не отличалась друг от друга и составила в основной группе 3525,68±224,35 гр., в группе сравнения – 3462,81±177,39 гр. и в группе контроля 3449,47±231,12 гр.
Из осложнений послеродового периода в основной группе диагностированы: субинволюция матки и лохиометра (3,7 %; n=7), анемия, сохраняющаяся в послеродовом периоде (41,1 %; n=78); в группе сравнения данные осложнения встречались, соответственно, в 3,3 % ( n=1) и 50,0 % ( n=15) наблюдений. По данным В.А. Петрухина и соавт. (2013), из послеродовых осложнений лохиометра имела место лишь у 4,9 % родильниц после применения мифепристона [5]. По мнению авторов, благоприятное течение послеродового периода и низкий процент послеродовых осложнений позволяют судить об отсутствии отрицательного влияния мифепристона на инволютивные процессы в миометрии.
В контрольной группе удельный вес анемии достоверно не отличался от показателей родильниц, которым применялись антигестагены, а субинволюции матки выявлены у 13,3 % женщин (n=4), что в 2,5 раза превышало частоту послеродовых осложнений в основной группе и группе сравнения. Кроме того, в группе контроля имели место 2 случая (6,7 %) позднего послеродового кровотечения, обусловленного гипотонией матки (кровопотеря до 1000 мл).
Сравнительный анализ перинатальных исходов в группах показал следующее: в основной группе в удовлетворительном состоянии (8–10 баллов по шкале Апгар) родилось 81,1 % новорожденных (n=154), в состоянии умеренной асфиксии (5–7 баллов по шкале Апгар) – 18,9 % (n=36). В группе сравнения высокую оценку по шкале Апгар (8–10 баллов) получили 80 % детей (n=24), в состоянии умеренной асфиксии – 20 % ( n=6). В контрольной группе умеренная асфиксия новорожденных диагностировалась в 1,6 раза чаще, чем в основной группе. Интранатальных, ранних неонатальных потерь, тяжелого травматизма новорожденных при этом ни в одном случае не зарегистрировано.
Заключение. Результаты проведенного анализа доказывают высокую эффективность применения мифепристона при срочных родах и различных акушерских ситуациях. Установлено, что применения мифепристона при целом плодном пузыре способствовало развитию спонтанной родовой деятельности через 24,2±3,5 часов у 83,2 % женщин, 15,7 % пациенток вступили в роды после проведения второго этапа подготовки (динопростон или амниотомия). При преждевременном разрыве плодных оболочек регулярная родовая деятельность развилась у 93,3 % пациенток через 6,3±0,7 часов после первого приема мифепристона. Частота операции кесарева сечения в основной группе составила 8,9 %, в группе сравнения – 16,7 %. Клиническая эффективность мифепристона с последующим этапом родовозбуждения амниотомией или динопростоном при целом плодном пузыре составила 91,1 %, а при преждевременном разрыве плодных оболочек – 83,3 %. Следует отметить, что отсутствие своевременной и адекватной медикаментозной подготовки родовых путей при доношенном сроке гестации и «незрелой» шейке матки приводит к увеличению удельного веса оперативного родоразрешения (до 26,7 %), а также родового травматизма, и рождению детей в состоянии умеренной асфиксии (до 30 %).
Исследование о влиянии мифепристона на плод при остановленном аборте
Авторы:
Джордж Делгадо (George Delgado) * врач,
Стивен Дж. Кондли (Steven J. Condly) ** доктор философии,
Мэри Дэвенпорт (Mary Davenport) *** врач, магистр естественых наук,
Тхидарат Тиннакорнсрисуфап (Thidarat Tinnakornsrisuphap) **** доктор философии,
Джонатан Мэк (Jonathan Mack) ***** доктор философии,
Вероника Хаув (Veronica Khauv), бакалавр естественых наук,
Пол С. Жу (Paul S. Zhou)
АННОТАЦИЯ:
Предпосылки исследования: некоторые женщины, уже принявшие мифепристон для прерывания беременности, антагонист прогестероновых рецепторов, передумывают делать аборт и желают остановить процесс медикаментозного аборта. В медицинской литературе представлены всего две статьи, документирующие отмену действия мифепристона.
Цели исследования: мы представляем и анализируем серию случаев, в которых женщины пытались остановить действие мифепристона с помощью прогестерона для того, чтобы установить возможность и безопасность остановки действия мифепристона при применении прогестерона. Кроме того, мы сравниваем различные схемы назначения прогестерона, чтобы определить их относительную эффективность.
Методы исследования: ретроспективный анализ клинических данных 754 пациенток, которые решили попытаться остановить процесс медикаментозного аборта после принятия мифепристона, но до приема второго препарата согласно инструкции, мизопростола. Мы изучали пациенток, получивших прогестерон с целью остановки действия мифепристона, и провели статистический анализ для определения эффективности различных процедур по сравнению с контрольным уровнем выживаемости эмбрионов после применения мифепристона, описанного в специальной литературе.
Результаты исследования: внутримышечное введение прогестерона и высокие дозы при оральном применении прогестерона показали наибольшую эффективность с показателями отмены в 64% (P-уровень
Капиллярная дисплазия кожи
Билатеральное отсутствие пальца стопы
Одностороннее отсутствие двух пальцев руки
Киста сосудистых сплетений
Поскольку предыдущие исследования на людях немногочисленны, доступные сведения предполагают, что мифепристон не является тератогенным (4, 40, 41). Практический бюллетень Американского колледжа акушеров и гинекологов за март 2014 года заявляет об отсутствии доказательств о связи мифепристона с тератогенностью (42). Наши данные, отражающие самое большое количество младенцев, подвергшихся воздействию мифепристона при внутриутробном развитии, также свидетельствуют о том, что риск возникновения врождённых пороков развития среди женщин, купировавших абортивное действие мифепристона, не выше, чем в целом среди населения.
Ограничения в исследовании
Настоящее исследование ограничено тем, что не является рандомизированным плацебо-контролируемым исследованием. Однако, плацебо-контролируемое исследование группы женщин, сожалеющих об аборте и желающих сохранить беременность, являлось бы неэтичным. Кроме того, хотя число вышедших из-под наблюдения женщин и небольшое, это могло повлиять на результаты. Также сбор некоторых данных был неполным.
Одним потенциально искажающим фактором является отбор живых эмбрионов с помощью УЗИ до применения первой дозы прогестерона. Возможно, что эмбрионы, живые на момент УЗИ, смогли бы выжить и без прогестероновой терапии. Однако, в наше исследование были включены также несколько женщин, начавших прогестероновую терапию до документального подтверждения жизни эмбриона на УЗИ. Несомненно, в данную группу попадали и те женщины, эмбрионы которых умерли до начала прогестероновой терапии. Включение таких женщин в исследование искусственно занижало бы уровень успешности прогестероновой терапии. Точное число женщин, прошедших или не прошедших ультразвуковое обследование до начала терапии, оказалось неизвестным для наших исследователей. Если бы ультразвуковое обследование было легкодоступным, было бы разумно сначала обязательно подтвердить или хотя бы проверить жизнеспособность эмбриона или плода до начала лечения во избежание приема прогестерона без надобности и для исключения внематочной беременности до начала прогестероновой терапии.
Выводы
Применение прогестерона для купирования действия мифепристона, являющегося конкурентным блокатором прогестероновых рецепторов, оказалось и безопасным, и эффективным. Прогестероновая терапия является биологически целесообразной, показавшей ранее свою эффективность на животных и подтвержденной данным исследованием серии случаев, продемонстрировавшим статистически значимую разницу в выживании между группами, прошедшими лечение, и историческими контрольными данными. Мифепристон оказывает эмбриоцидный и абортивный эффект, но не является тератогенным; прогестерон не вызывает врождённые пороки развития.
Основываясь на указанных новых данных, женщинам, желающим купировать действие мифепристона, могут быть предложены две целесообразные схемы лечения:
1. Микронизированный прогестерон (200 мг) по две капсулы перорально в возможно короткие сроки, затем по 2 капсулы 200 мг орально два раза в день в течение трёх дней, далее по 2 капсулы 200 мг ежедневно перед сном до конца первого триместра;
2. Прогестерон 200 мг внутримышечно в возможно короткие сроки, затем 200 мг внутримышечно один раз в день на второй и третий день, затем через день − всего семь инъекций. Некоторые лечащие врачи могут порекомендовать продолжить курс внутримышечных инъекций, поскольку данная рекомендация основывается на сравнительно небольшом количестве случаев.
Рекомендации для дальнейших исследований
Мы предлагаем включить в дальнейшие исследования рандомизированные контролируемые исследования, сравнивающие дозы прогестерона и способы его применения, которые определят, какие способы применения, дозы и продолжительность прогестероновой терапии являются наиболее эффективными и оказывают наименьшую нагрузку на пациента.
Авторы выражают признательность Саре Литтлфилд за усердие в сборе и подготовке данных и помощь с организационными задачами.
1. Jones RK and Jerman J. Abortion incidence and service availability in the United States, 2014. Perspectives on Sexual and Reproductive Health, 2017, 49(1), DOI: 10.1363/psrh.12015.
2. Delgado G, Davenport M. Progesterone Use to Reverse the Effects of Mifepristone. Ann Pharmacother 2012;46. Published Online, 27 Nov 2012, theannals.com, DOI: 10.1345/aph.1R252.
3. Medication Guide, Mifeprix. www.fda.gov/downloads/drugs/drugsafety/ucm088643.pdf (accessed November 19, 2016).
4. Creinin, M, Gemzell Danielsson, K. Chapter 9, Medical abortion in early pregnancy, in Management of Unintended and Abnormal Pregnancy: Comprehensive Abortion Care. Published Online: 22 May 2009 DOI:10.1002/9781444313031.ch9.
5. Heikinheimo O, Kekkonen R, Lahteenmaki P. The pharmacokinetics of mifepristone in humans reveal insights into differential mechanisms of antiprogestins action. Contraception 2003;68:421–6.
6. Sarkar NN. Mifepristone: bioavailability, pharmacokinetics and use-effectiveness. Eur J Obstet Gynaecol Reprod Bio; 2002;101:113–20.
7. Drug Bank Progesterone. http://www.drugbank.ca/drugs/DB00396 (accessed 2011 Oct 8).
8. Johannisson E, Oberholzer M, Swahn ML, Bygdeman M. Vascular changes in the human endometrium following the administration of the progesterone antagonist RU 486. Contraception 1989; 39: 103–107.
9. Schindler AM, Zanon P, Obradovic D, Wyss R, Graff P, Hermann WL. Early ultrastructural changes in RU-486-exposed decidua. Gynecol Obstet Invest 1985; 20: 62–67.
10. Swahn ML, Bygdeman M. The effect of the antiprogestin RU 486 on uterine contractility and sensitivity to prostaglandin and oxytocin. Br J Obstet Gynaecol 1988; 95: 126–134.
11. Herrmann WL, Schindler AM, Wyss R, Bishof P. Effects of the antiprogesterone RU 486 in early pregnancy and during the menstrual cycle. In: Beaulieu EE, Siegel S, eds. The Antiprogestin Steroid RU 486 and Human Fertility Control. Plenum, New York, 1985: 259–262.
12. Ottander U, et al. A Putative Stimulatory Role of Progesterone Acting via Progesterone Receptors in the Steroidogenic Cells of the Human Corpus Luteum. Biology of Reproduction March 1, 2000 vol. 62 no. 3 655–663.
13. Yamabe, S; Katayana, K; Mochuzuki, M Folio endocrine. 65, 497–511, 1989. The Effects of RU486 and Progesterone on Luteal Function During Pregnancy.
15. Beaulieu EE. RU-486: An antiprogestin steroid with contragestive effect in women. In Baulieu EE,
Siegel S (eds): The Antiprogestin Steroid RU 486 and Human Fertility Control. New York, Plenum, 1985. pp. 2–6.
16. Grossman D et al. Continuing pregnancy after mifepristone and “reversal” of first-trimester medical abortion: A systematic review, Contraception (2015) September 2015 Volume 92, Issue 3, pp. 206–211, DOI: 10.1016/j.contraception.2015.06.001).
17. Davenport M, Delgado G, Khauv V. Embryo survival after mifepristone: review of the literature. Issues in Law and Medicine 2017, 32 (1): 3–18.
18. Ylikorkala O, Alfthan H, Kääriäinen M, Rapeli T, Lähteenmäki P. Outpatient therapeutic abortion with mifepristone. Obstet Gynecol 1989;74:653–7.
19. Maria B, Chaneac M, Stampf F, Ulmann A. [Early pregnancy interruption using anantiprogesterone steroid: Mifepristone (RU 486)]. J Gynecol Obstet Biol Reprod (Paris) 1988;17:1089–94.
20. Carol W, Klinger G. [Experiences with the antigestagen mifepristone (RU 486) in the interruption of early pregnancy]. Zentralbl Gynakol 1989;111:1325–8.
21. Somell C, Olund A. Induction of abortion in early pregnancy with mifepristone. Gynecol Obstet Invest 1990;29:13–5.
22. Kovacs L, Sas M, Resch BA, Ugocsai G, Swahn ML, Bygdeman M, Rowe PJ. Termination of very early pregnancy by RU 486–an antiprogestational compound. Contraception 1984;29:399–410.
23. Kovacs L, Termination of Very Early Pregnancy with Different Doses of RU-486: A Phase I Controlled Clinical Trial. In Beaulieu EE, Siegel S (eds): The Antiprogestin Steroid RU 486 and Human Fertility Control. pp. 179–198. New York, Plenum, 1985.
24. Swahn ML. S. Cekan, G. Wang, V. Lundstom, and M. Bygdeman. In Beaulieu EE, Siegel S (eds): The Antiprogestin Steroid RU 486 and Human Fertility Control. pp. 249–258. New York, Plenum, 1985.
25. Herrmann WL, Schindler AM, Wyss R, et al: Effects of the antiprogesterone RU 486 in early pregnancy and during the menstrual cycle. In Beaulieu EE, Siegel S (eds): The Antiprogestin Steroid RU 486 and Human Fertility Control. pp. 179–198. New York, Plenum, 1985.
26. Herrmann W, Wyss R, Riondel A, Philibert D, Teutsch G, Sakiz E, Baulieu EE. [The effects of an antiprogesterone steroid in women: interruption of the menstrual cycle and of early pregnancy]. Comptes Rendus Seances Acad Sci III. 1982 May 17;294(18):933–8. French.
27. Vervest HAM, Haspels AA, Preliminary results with antiprogesterone RU-486. (mifepristone) for interruption of early pregnancy. FertilSteril. 1985;44: 627–32.
28. Haspels AA Interruption of early pregnancy by the antiprogestational compound RU 486 In Beaulieu EE, Siegel S (eds): The Antiprogestin Steroid RU 486 and Human Fertility Control. pp. 199–210, New York, Plenum, 1985.
29. Haspels AA. Interruption of early pregnancy by an anti-progestational compound, RU 486. Eur J Obstet Gynecol Reprod Biol. 1985 Sep;20(3):169.
30. Cameron IT, Michie AF, Baird DT. Therapeutic abortion in early pregnancy with antiprogestogen RU486 alone or in combination with prostaglandin analogue (gemeprost). Contraception 1986;34:459–68.
31. Cameron IT, Baird DT. Early pregnancy termination: a comparison between vacuum aspiration and medical abortion using prostaglandin (16,16 dimethyl-trans-delta 2‑PGE1 methyl ester) or the antiprogestogen RU 486. Br J Obstet Gynaecol. 1988 Mar; 95(3):271–6.
32. Elia D. Clinical study of RU 486 in early pregnancy In Beaulieu EE, Siegel S (eds): The Antiprogestin Steroid RU 486 and Human Fertility Control. pp. 211–220. New York, Plenum, 1985.
33. Spitz IM, Bardin W, Benton L, Robbins A, et al. Early pregnancy termination with mifepristone and misoprostol. N Engl J Med 1998;338:1241–7. DOI: 0.1056/NEJM199804303381801.
34. CDC MMWR January 11, 2008 / 57(01);1–5.
35. Preterm Birth. http://www.cdc.gov/reproductivehealth/maternalinfanthealth/pretermbirth.htm (accessed December 7, 2016).
36. Dante G, Vaccaro V, Facchinetti. Use of progestogens in early pregnancy. Facts, Views and Vision. ObGyn. 2013 5(1): 66–71.
37. Progesterone. https://www.asrm.org/detail.aspx?id=1881(accessed December 3, 2016).
38. Progesterone package insert. https://www.drugs.com/pro/progesterone-capsule.html. (accessed December, 3, 2016).
39. Hargreave M, et al. Maternal use of fertility drugs and risk of cancer in children–a nationwide population-based cohort study in Denmark. Int. J. Cancer: 136, 1931–1939 (2015).
40. Bernard N, Elefant E, Carlier P, Tebacher M, Barjhoux CE, Bos-Thompson MA, Amar E, Descotes J, Vial T. Continuation of pregnancy after first-trimester exposure to mifepristone: an observational prospective study. BJOG. 2013 Apr;120(5):568–74. DOI: 10.1111/1471–0528.12147. Epub 2013 Jan.
42. Medical Management of First Trimester Abortion. ACOG Practice Bulletin 143 March 2014, reaffirmed 2016.
Оригинал статьи на английском языке Delgado et al Issues in Law & Medicine, Volume 33, Number 1, 2018 Revisions — FINAL: The Successful Reversal of the Effects of Mifepristone Using Progesterone опубликован в журнале Issues in Law & Medicine, Volume 33, Number 1, 2018. Источник. PDF