мелкоочаговый инфаркт миокарда что это такое и последствия
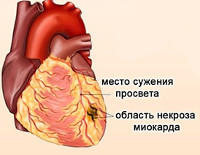
Микроинфаркт ( Мелкоочаговый инфаркт миокарда )
Микроинфаркт — это патологическое состояние, характеризующееся развитием в сердечной мышце небольших очагов некроза вследствие существенного уменьшения объема регионального коронарного кровотока. Пациенты жалуются на боль в области сердца, слабость, головокружение, одышку и лихорадку. Состояние может осложниться кардиальной недостаточностью, нарушениями ритма, тромбоэмболией или перикардитом. Клиническая картина часто отсутствует или выражена минимально. Диагностика включает в себя лабораторные методы, ЭКГ, ЭхоКГ и коронароангиографию. Лечение комплексное, осуществляются консервативные мероприятия, по показаниям применяются инвазивные методы.
МКБ-10
Общие сведения
Микроинфаркт в клинической практике обычно называют «мелкоочаговый инфаркт миокарда» или «не Q-инфаркт». Частота встречаемости патологии за последнее время значительно выросла и составляет до 50-70% от всех некротических повреждений сердечной мышцы. Это повышение объясняется улучшением качества диагностики, особенно вследствие повсеместного распространения измерения уровня биохимических маркеров распада кардиомиоцитов, а также повышением общей осведомленности населения о ранних тревожных симптомах. Перечисленные факторы позволяют своевременно диагностировать патологию, начать соответствующую терапию при малой площади поражения. Средний возраст пациентов — 65 лет, доля мужчин составляет 60%.
Причины микроинфаркта
Обычно этиология мелко- и крупноочаговых повреждений сходна. В отличие от последних, при некрозе без образования зубца Q происходит лишь частичная окклюзия просвета сосуда либо закупорка мелкой артерии с достаточной компенсацией в виде активации коллатерального кровотока. Одни и те же патологические процессы могут привести к поражениям различной площади. Велика роль предрасполагающих факторов: наличие у пациента вредных привычек и хронического стресса, гипертония, неполноценное питание, погрешности в диете, алиментарное ожирение, сопровождаемое гиперхолестеринемией, гиподинамия. Непосредственными причинами мелкоочаговых инфарктов в современной кардиологии считаются:
Патогенез
Как некроз сердечной мышцы, микроинфаркт, прежде всего, связан с нарушением коронарного кровообращения вследствие атеротромбоза. Он начинается с повреждения холестериновой бляшки, которое может быть вызвано, например, резким скачком артериального давления. Развитие местной воспалительной реакции потенцирует привлечение лейкоцитов в зону поражения. Они, в свою очередь, начинают вырабатывать специфические биологически активные вещества — медиаторы, обладающие свойством активировать свертывающую и угнетать противосвертывающую систему крови.
При повреждении интимы сосуда обнажаются коллагеновые волокна, что стимулирует переход тромбоцитов в активную форму. В результате адгезии и агрегации клетки оседают на стенке артерии с образованием тромба. Обычно этот процесс сопровождается спазмом гладкой мускулатуры сосуда. Возникает окклюзия просвета с существенным ухудшением кровоснабжения миокарда. Однако при микроинфаркте ишемия не достигает критических значений, некроз имеет небольшую площадь, не является трансмуральным и не затрагивает проводящую систему сердца.
Классификация
Понятие микроинфаркт входит в общую номенклатуру инфаркта сердечной мышцы, является его отдельной разновидностью. Ему соответствует характеристика «мелкоочаговый», однако при морфологическом исследовании размер некроза без образования патологического Q-зубца может быть сопоставимым с теми случаями, когда этот элемент ЭКГ наблюдался. Поэтому более важным признаком является наличие либо отсутствие нарушений нормального движения сигнала по проводящей системе сердца. В настоящее время используется классификация патологии, в основе которой лежат причины и механизмы ее возникновения. Выделяют пять типов микроинфаркта:
Симптомы микроинфаркта
Заболевание имеет слабовыраженные клинические проявления вплоть до их полного отсутствия. Возможна ситуация, когда пациент узнает о том, что перенес микроинфаркт, только на ежегодном плановом осмотре. Симптомы крайне неспецифичны, патология иногда протекает под маской обычного ОРВИ. Больной ощущает слабость, непродолжительную субфебрильную лихорадку, головокружение, одышку и боль за грудиной. Приступ продолжается от 30 минут до 2 часов. При улучшении состояния пациент, как правило, не обращается за медицинской помощью, болезнь остается нераспознанной.
При атипичном течении процесса, характерном для молодых людей, формируются особые клинические формы с существенным преобладанием тех или иных явлений. Например, при астматическом варианте микроинфаркта затруднено дыхание, невозможен полный вдох и выдох; при церебральном — часто возникают синкопальные состояния. При поражении участков миокарда, расположенных близко к диафрагме, к клинике микроинфаркта добавляются абдоминальные боли, тошнота и рвота.
Возможно появление дополнительных признаков, связанных с общими нарушениями деятельности кровеносной системы: похолодание, отечность конечностей, частые головные боли, повышенное потоотделение, редкие колющие боли в кардиальной области, посинение носогубного треугольника. Пожилые люди и пациенты, страдающие сахарным диабетом, из-за особенностей физиологии и патофизиологии имеют более высокий болевой порог. У этих категорий больных микроинфаркт практически всегда протекает бессимптомно.
Осложнения
Чаще всего после перенесенной патологии наблюдается формирование кардиальной недостаточности с застойными явлениями по обоим кругам кровообращения вплоть до развития сердечной астмы. При распространении повреждения на основные пути проводящей системы могут наблюдаться различные по характеру нарушения ритма и проводимости. К другим осложнениям относят тромбоэмболии, перикардиты и повторные инфаркты.
Диагностика
Главными задачами врача-кардиолога на этапе обследования пациента являются установление того факта, что предъявляемые жалобы развиваются именно вследствие ишемических процессов в миокарде, оценка риска развития осложнений и неблагоприятных исходов. При физикальном обследовании микроинфаркт часто никак себя не проявляет либо выявляются только неспецифические признаки, поэтому на первое место выходят дополнительные методы диагностики. К ним относятся:
Дифференциальная диагностика состояния может вызывать затруднения, особенно при отсутствии специфических методов исследования и стертой клинической картине. Чаще всего различение проводится с другими сердечно-сосудистыми заболеваниями (расслаивающаяся аневризма аорты, тромбоэмболия легочной артерии, миокардит) и плевритом. При атипичных формах с наличием абдоминальных симптомов важно дифференцировать некроз кардиальной мышцы от язвенной болезни желудка, кишечной колики, холецистита и панкреатита.
Лечение микроинфаркта
Принципы лечения мелкоочаговых процессов в целом сходны с таковыми при более обширных инфарктах миокарда. Главными целями являются восстановление или максимально возможное улучшение коронарного кровотока, улучшение качества жизни пациента и профилактика осложнений. При любом обоснованном подозрении на некроз кардиомиоцитов необходима госпитализация, строгий постельный режим, ингаляции кислорода и постоянный ЭКГ-контроль. Варианты возможной терапии:
После выписки больной должен придерживаться назначаемой ему комплексной терапии, направленной на профилактику прогрессирования коронарного атеросклероза и ишемических явлений. Используются дезагреганты, ингибиторы АПФ и гиполипидемические средства, при необходимости – антиангинальные препараты. Из-за приема достаточно больших доз медикаментов, угнетающих активность тромбоцитов, осуществляется профилактика геморрагических осложнений.
Прогноз и профилактика
При своевременном оказании необходимого объема медицинской помощи прогноз благоприятный. Частота развития серьезных осложнений у пациентов при госпитализации по поводу микроинфаркта составляет не более 5%, после выписки из больницы — 15%. Профилактика заключается в регулярном прохождении осмотров, посещении кардиолога со снятием ЭКГ, особенно лицами старшего возраста. Важными моментами являются отказ от курения, рациональное питание с уменьшенным количеством насыщенных жиров, достаточный уровень физической активности, контроль артериального давления и уровня липидов крови.
Острый инфаркт миокарда (субэндокардиальный и трансмуральный)
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагностика
Электрокардиограмма позволяет выявить очаг некроза в мышце сердца, его глубину и локализацию, состояние переинфарктной зоны, динамику процесса. На ЭКГ отведениях, активный электрод которых располагается над зоной некроза, образуется патологический зубец Q и снижается высота зубца R вплоть до полного его исчезновения. Изменения зубца Q сочетается с характерной для ИМ ЭКГ динамикой, отражающей временную динамику заболевания.
Электрокардиографические признаки можно систематизировать следующим образом:
Дифференциальный диагноз
Особенно трудно дифференцировать инфаркт миокарда и поражение грудного отдела аорты. В последнем случае боль в грудной клетке, как правило, сильная, нестерпимая. Она начинается внезапно, сразу с максимальной интенсивностью, иррадиирует вдоль позвоночника, имеет волнообразное течение.
При дифференциальной диагностике следует учитывать резкое несоответствие интенсивности и длительности боли скудным изменениям ЭКГ. Во всех сложных диагностических случаях серьезным подспорьем является экспресс-тест с тропонином-Т или гликоген-фосфорилазой ВВ.
Лечение
3. Стабилизация артериального давления и ритма сердца.
Информация
Источники и литература
Информация
Сотрудники кафедры скорой и неотложной медицинской помощи, внутренних болезней №2 Казахского национального медицинского университета им. С.Д. Асфендиярова: к.м.н, доцент Воднев В.П.; к.м.н., доцент Дюсембаев Б.К.; к.м.н., доцент Ахметова Г.Д.; к.м.н., доцент Бедельбаева Г.Г.; Альмухамбетов М.К.; Ложкин А.А.; Маденов Н.Н.
Заведующий кафедрой неотложной медицины Алматинского государственного института усовершенствования врачей – к.м.н., доцент Рахимбаев Р.С.
Сотрудники кафедры неотложной медицины Алматинского государственного института усовершенствования врачей: к.м.н., доцент Силачев Ю.Я.; Волкова Н.В.; Хайрулин Р.З.; Седенко В.А.
Острый субэндокардиальный инфаркт миокарда (I21.4)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Основные особенности инфаркта миокарда без зубца Q:
Несколько показателей помогают отличить инфаркт без зубцов Q от инфаркта с зубцом Q и от нестабильной стенокардии:
— характеристики тромбообразования;
— время разрешения тромба;
— наличие либо отсутствие коллатеральных сосудов.
Этиология и патогенез
Причины инфаркта миокарда без подъемов сегмента ST (ИМ БП ST) в порядке распространенности:
Эпидемиология
Признак распространенности: Распространено
Факторы и группы риска
Клиническая картина
Cимптомы, течение
Острый период
На вторые сутки ферменты из поврежденных клеток и разрушенные ткани попадают в кровь, вызывая температурную реакцию: может появляться лихорадка до 39°С, а также недомогание, слабость, потливость.
Действие стрессовых гормонов (адреналина, норадреналина, дофамина) утихает, в результате чего артериальное давление снижается, иногда очень значительно.
Подострый период
В этот период болевые ощущения, как правило, отсутствуют. Учитывая тот факт, что сократительная способность сердца снижена, поскольку участок миокарда «выключен» из работы, могут появиться симптомы сердечной недостаточности: одышка, отеки ног. В целом же состояние пациента улучшается: температура нормализуется, артериальное давление стабилизируется, риск развития аритмии уменьшается.
В сердце происходят процессы рубцевания: организм устраняет образовавшийся дефект, замещая разрушенные кардиомиоциты соединительной тканью.
Период рубцевания инфаркта миокарда
В этот период продолжается и завершается образование полноценного рубца из грубоволокнистой соединительной ткани. Самочувствие пациента зависит от величины площади поражения и наличия или отсутствия осложнений инфаркта миокарда.
В целом, состояние нормализуется. Болевых ощущений в сердце нет либо имеется стабильная стенокардия определенного функционального класса. Человек привыкает к новым условиям жизни.
Диагностика
При субэндокардиальном инфаркте миокарда некроз располагается полосой у эндокарда левого желудочка. Поскольку возбуждение субэндокардиальных слоев проходит значительно быстрее субэпикардиальных, то патологический зубец Q не успевает образоваться и зарегистрирован быть не может.
Об инфаркте миокарда судят по изменениям ЭКГ, обусловленным субэндокардиальным повреждением, сопутствующим некрозу (отведения V1-V6, I, aVL):
Изменения ЭКГ при субэндокардиальном инфаркте миокарда следует отличать от реципрокных изменений в грудных отведениях, вызванных инфарктом миокарда задней стенки.
Лабораторная диагностика
В соответствии с рекомендациями ВОЗ, основное значение в диагностике острого инфаркта миокарда (ОИМ) наряду с клинической картиной заболевания и изменениями ЭКГ придают исследованию кардиоспецифичных маркеров.
В клинической практике наиболее часто исследуют:
1. Концентрацию креатинфосфокиназы (КФК), аспартатаминотрансферазы (АСТ), лактатдегидрогеназы (ЛДГ).
2. К маркерам гибели миоцитов относятся гликогенфосфорилаза (ГФ), миоглобин (Мг), миозин и кардиотропонин Т и I.
3. Специфичны для поражения только кардиомиоцитов (но не миоцитов скелетных мышц) изоферменты КФК-МВ и ЛДГ-1, а также иммунохимическое определение КФК-МВ, массы ГФ-ВВ, изоформы изофермента КФК-МВ и кардитропонины I и Т.
Критерии диагностической эффективности того или иного маркера:
— диапазон диагностической значимости, то есть период времени, в течение которого определяется повышенный, «патологический» уровень определяемого маркера;
— степень его увеличения относительно уровня нормальных значений; как правило, относительно верхней границы этого уровня.
Диагностическая ценность вышеперечисленных маркеров зависит от сроков и частоты их определения в динамике развития ОИМ.
Патогномоничным для инфаркта миокарда является повышение активности ферментов не менее чем в 1,5-2 раза с последующим снижением до нормальных значений.
Если в динамике не прослеживается закономерного снижения того или иного маркера, то врач должен искать другую причину его длительного повышения.
Изменение кардиальных маркеров при остром инфаркте миокарда
| Показа- тель | Мг | КФК | КФК-МВ | Изоформы КФК | ЛДГ | ЛДГ-1 | Тн-Т | Тн-I |
| Диапазон нормаль- ных значений | 24-195 Ед/л | 10-25 Ед/л ( | МВ | 35-88 Ед/л | 14-36% общей ЛДГ | |||
| Время подъема *** | 0,5-2 ч. | 3-8 ч. | 3-8 ч. | 1-4 ч. | 8-18 ч. | 8-18 ч. | 3-6 ч. | 3-6 ч. |
| Пик через *** | 5-12 ч. | 10-36 ч. | 9-30 ч. | 4-8 ч. | 24-72 ч. | 24-72 ч. | 10-24 ч. | 14-20 ч. |
| Снижение до нормы через *** | 18-30 ч. | 72-96 ч. | 48-72 ч. | 12-24 ч. | 6-10 дн. | 6-10 дн. | 10-15 дн. | 5-7 дн. |
| Чувстви- тельность 0-6 ч. (%) | 50-100 | 50-75 | 17-62 | 92-96 | н.д. | н.д. | 50-59 | 6-44 |
| Специфич- ность 0-6 ч. (%) | 77-95 | 80-98 | 92-100 | 94-100 | н.д. | н.д. | 74-96 | 93-99 |
Однократное исследование миокардиальных маркеров у больных с подозрением на ОИМ является неприемлемым и практически полностью обесценивает диагностическую значимость данного метода диагностики.
Абсолютно специфичных маркеров повреждения кардиомиоцитов не найдено. В таблице представлены состояния, при которых может выявляться повышение тех или иных маркеров, применяемых в диагностике ОИМ.
Повышение кардиальных маркеров при других заболеваниях
1. АСТ и ЛДГ:
— з аболевания и повреждения скелетной мускулатуры (прогрессирующая мышечная дистрофия, травмы, ожоги, физическая нагрузка, дерматомиозит);
— заболевания печени (хронические гепатиты, циррозы печени, токсические повреждения);
— заболевания кроветворной системы;
— внутрисосудистый гемолиз;
— оперативные вмешательства с применением искусственного кровообращения;
— шок;
— гипоксия;
— гипертермия;
— отек легких;
— алкогольная интоксикация;
— инфекционный мононуклеоз.
2. КФК:
— воспалительные и дистрофические поражения мышечной ткани (дистрофия всех типов, миопатии, дерматомиозиты, рабдомиолиз);
— любые оперативные вмешательства, травмы, ушибы мягких тканей, ранения, ожоги;
— интенсивная мышечная нагрузка;
— шок;
— гипоксия;
— кома;
— миоглобинурия;
— в/м инъекции;
— гипертермия и гипотермия;
— в/в введение мышечных релаксантов;
— отек легких;
— генерализованные судороги;
— беременность;
— гипокалемия;
— э лектроимпульсная терапия;
— коронарография;
— реанимационные мероприятия.
3. КФК-МВ:
— воспалительные, дистрофические и некротические процессы в скелетной мускулатуре;
— кардиохирургические операции с применением искусственного кровообращения;
— шок;
— острая гипоксия;
— гипотермия и гипертермия;
— передозировка или длительное применение теофиллина, амитриптилина, изопротеренола, салицилатов;
— уремия и гипотериоз (иногда).
4. Миоглобин:
— дистрофические и воспалительные процессы в скелетных мышцах;
— любые оперативные вмешательства, травмы, ушибы мягких тканей, ранения, термические ожоги;
— артериальная окклюзия с ишемией мышц;
— шок;
— острая гипоксия;
— выраженная почечная недостаточность;
— в/м инъекции;
— чрезмерная физическая активность;
— генерализованные судороги;
— применение миорелаксантов, ловастатина, клофибрата;
— гипотиреоз;
— вторичная токсическая миоглобинурия.
Наибольшей специфичностью на сегодняшний день обладают тропонины Т и I. В стадии клинической апробации находятся такие маркеры, как α-актин и белок, связывающий жирные кислоты.
Важное значение в диагностике инфаркта миокарда имеет исследование динамики кардиоспецифических маркеров некроза в крови.
Одним из ранних признаков ОИМ может быть нейтрофильный лейкоцитоз до 12-14-10 9 /л, который выявляется уже в первые часы заболевания и сохраняется на протяжении 3-6 суток от начала болевого синдрома. По мере уменьшения лейкоцитоза, на 3-4 сутки от начала заболевания, в периферической крови определяется ускоренное СОЭ, которая может оставаться повышенной 1-2 недели.
Для ОИМ также характерно увеличение уровня фибриногена и положительная реакция С-реактивного белка.
Регистрация указанных изменений не является специфичной, однако имеет определенную ценность при диагностике Q-необразующего ИМ и при отсутствии возможности определения активности других маркеров.
Дифференциальный диагноз
Интенсивная боль в грудной клетке может быть обусловлена патологическим процессом в различных органах и системах.
2. Заболевания легких и плевры:
— острая пневмония с плевритом ;
— спонтанный пневмоторакс.
3. Заболевания пищевода и желудка:
— грыжа пищеводного отверстия диафрагмы;
— эзофагит;
— язвенная болезнь желудка;
— острый панкреатит.
4. Заболевания опорно-двигательного аппарата:
— остеохондроз шейно-грудного отдела позвоночника;
— миозит;
— межреберная невралгия.
5. Вирусная инфекция: опоясывающий лишай.
Вариантная стенокардия
По клиническим и ЭКГ-критериям наиболее близка к ОИМ. Появление интенсивного болевого синдрома в покое, часто в ночные и предрассветные часы, сопровождающегося у половины больных нарушениями ритма сердца, соответствует клинике коронарного тромбоза.
На ЭКГ, снятой во время болей, регистрируется элевация сегмента ST с дискордантной его депрессией в контрлатеральных отведениях, что также характерно для острейшей стадии ИМ.
В данной ситуации исключить развитие некроза сердечной мышцы позволяет нормализация ЭКГ-картины после купирования болевого синдрома, отсутствие гиперферментемии.
УЗИ сердца, проведенное после стабилизации состояния больного, также не выявляет нарушения локальной сократимости миокарда (гипо- и/или акинез) в зоне, соответствующей элевации сегмента ST.
УЗИ подтверждает диагноз гипертрофической кардиомиопатии:
— асимметричная гипертрофия межжелудочковой перегородки;
— уменьшение полости левого желудочка;
— систолическое движение вперед митрального клапана;
— нарушение диастолической функции миокарда;
— у части больных отмечаются признаки обструкции выносящего тракта левого желудочка (подклапанный стеноз).
ЭКГ может оказаться мало информативной при наличии полной блокады ножек пучка Гиса, когда отсутствуют достоверные признаки ИМ. В то же время выявление тахикардии, желудочковых аритмий, нарушений атриовентрикулярного проведения возможно при том и другом заболевании.
В случае отсутствия достоверных ЭКГ-признаков некроза миокарда ведущую роль занимает УЗИ сердца как метод, позволяющий оценить нарушения сократительной способности сердечной мышцы. Для миокардита характерно диффузное снижение инотропной функции обоих желудочков, в то время как при инфаркте отмечают сегментарное нарушение сократимости миокарда.
Окончательно поставить диагноз можно при выполнении коронарографии, радиоизотопной вентрикуло- и сцинтиграфии миокарда.
На ЭКГ изменения отсутствуют или обнаруживается депрессия сегмента ST и инверсия зубца Т, нарушения ритма сердца, что не дает права исключить мелкоочаговый ИМ. В данном случае приходится ориентироваться на уровень ферментов крови: нормальные значения тропонина, миоглобина или креатинфосфокиназы позволяют отвергнуть диагноз некроза сердечной мышцы.
Подтверждение расслаивания стенки аорты достигается применением УЗИ, аортографии.
В пользу ТЭЛА свидетельствует выявление у больного характерных факторов:
— наличие недавно перенесенной травмы, операции;
— длительный постельный режим;
— указания в анамнезе на острое нарушение мозгового кровообращения с плегией конечностей;
— флеботромбоз глубоких вен голеней;
— прием больших доз диуретиков.
О патологии легких говорит появление у больного сухого кашля, кровохарканья (30%), аускультативных признаков поражения легких и плевры.
Рентгенологическое исследование подтверждает локальное уменьшение легочного кровотока и повышение давления в легочной артерии:
— обеднение легочного рисунка;
— «хаотический» легочный рисунок;
— высокое стояние купола диафрагмы и уменьшение объема корня на стороне поражения;
— выбухание ствола легочной артерии;
— через сутки возможно выявление инфарктной пневмонии, плеврита, расширения правых отделов сердца.
ЭКГ, как правило, достаточно информативна. Выявляют признаки перегрузки и гипертрофии правого предсердия и желудочка:
— остроконечный высокоамплитудный (более 2,5 мм) зубец Р;
— поворот оси сердца вправо;
— появление непатологического Q в III отведении;
— увеличение амплитуды R;
— появление депрессии сегмента ST в правых грудных отведениях;
— смещение переходной зоны влево;
— у части больных появляются глубокие (более 5 мм) зубцы S в V5-6, блокада правой ножки пучка Гиса.
Ферментная диагностика выявляет увеличение активности трансаминаз при нормальных уровнях МВ-КФК, тропонинов.
Окончательно диагноз ТЭЛА верифицируют данные вентиляционно-перфузионной сцинтиграфии легких или ангиопульмонографии.
Ущемление диафрагмальной грыжи
Может сопровождаться появлением острой боли в нижней части грудной клетки с иррадиацией в левую половину груди или верхние отделы живота. Расспрос больного позволяет установить, что ранее боли за грудиной возникали после приема пищи; в горизонтальном положении возникали отрыжка воздухом или съеденной пищей, могли беспокоить изжога и тошнота при сопутствующем рефлюкс-эзофагите.
Отсутствие изменений ЭКГ и данные рентгенологического исследования желудка позволяют поставить правильный диагноз.
Эзофагит и язвенная болезнь желудка
заболевания могут симулировать клинику ИМ нижней локализации (абдоминальный вариант). Анамнестические указания на заболевание пищевода или желудка, связь болей с приемом пищи, элементы кислотной диспепсии заставляют сомневаться в патологии сердца.
При объективном исследовании обращают на себя внимание болезненность и напряжение мышц в эпигастрии, в то время как для инфаркта более характерно вздутие живота. При электрокардиографическом исследовании не находят характерных признаков ОИМ, в крови отсутствует повышение кардиоспецифических ферментов.
Острый панкреатит
Может начинаться с постепенно усиливающихся болей в верхних отделах живота с иррадиацией в спину, левую руку, лопатку. Болевой синдром, тошнота, рвота, бледность кожных покровов в сочетании с артериальной гипотензией, тахикардией позволяют заподозрить абдоминальный вариант ОИМ.
Повышение температуры тела, лейкоцитоз в крови присущи обоим заболеваниям.
ЭКГ при панкреатите может выявить депрессию сегмента ST и инверсию зубца Т, что наблюдается при инфаркте миокарда без зубца Q.
Диагностике помогает исследование сывороточных ферментов:
— при панкреатите в первые часы выявляется повышение аминотрансфераз, амилазы, ЛДГ при нормальных значениях КФК и ее МВ-фракции, тропонинов;
— для ИМ характерно повышение в крови уровня тропонинов и КФК в первые 6-12 часов заболевания с последующим нарастанием активности трансфераз и ЛДГ.
УЗИ сердца и поджелудочной железы позволяет окончательно уточнить поражение органов.
Миозит, межреберная невралгия и остеохондроз позвоночника часто сопровождаются интенсивными болями в грудной клетке. Болевой синдром сохраняется долго, не купируется нитратами, имеет четкую связь с переохлаждением, дыханием, поворотами туловища.
При миозите пальпируются уплотненные болезненные участки мышцы, при поражении нервных пучков имеется локальная болезненность в соответствующих зонах.
Осложнения
Группы осложнений инфаркта миокарда (ИМ):
2. Гемодинамические осложнения:
2.1 Вследствие нарушений насосной функции сердца:
— острая левожелудочковая недостаточность;
— острая правожелудочковая недостаточность;
— бивентрикулярная недостаточность;
— кардиогенный шок;
— аневризма желудочка;
— расширение инфаркта.
2.2 Вследствие дисфункции сосочковых мышц.
2.3 Вследствие механических нарушений:
— острая митральная регургитация вследствие разрыва сосочковых мышц;
— разрывы сердца, свободной стенки или межжелудочковой перегородки;
— аневризмы левого желудочка;
— отрывы сосочковых мышц.
2.4 Вследствие электромеханической диссоциации.
По времени появления осложнения ИМ классифицируют на:
Лечение
Этап скорой помощи
Основная цель этапа: как можно более быстрая госпитализация (не тратить время на вызов специализированной бригады).
3. Антикоагулянты прямого действия (не обязательно на догоспитальном этапе, при необходимости выбор из ниже перечисленных, что есть):
3.1 Фондапаринукс (2,5 мг в день п/к) рекомендуется как препарат с наиболее оптимальным профилем безопасности/эффективности в отношении антикоагуляции (I А).
3.2 Эноксапарин (1 мг/кг 2 раза в день п/к) рекомендуется, если фондапаринукс недоступен, допускается первоначальное в/в введение болюса 30 мг у пациентов с повышенным риском, при возрасте меньше 75 лет (I В). У пациентов с клиренсом креатинина ) (IIа С).
5. Атропин в дозе 0,25-0,5-1 мг в/в в случае брадикардии в сочетании с гемодинамической нестабильностью.
Необходимо оценить выраженность факторов, способствующих усугублению ишемии (гипертония, сердечная недостаточность, аритмия), и принять меры к их устранению или уменьшению.
Госпитальный этап
Пациент с болями в грудной клетке и подозрением на ОКС должен быть немедленно осмотрен квалифицированным врачом. В первую очередь пациенту ставят рабочий диагноз, на котором будет основана стратегия лечения.
Для оценки используются следующие критерии:
— качество дискомфорта/боли в груди и физикальное обследование, ориентированное на выявление симптомов;
— оценка вероятности ИБС (возраст, факторы риска, перенесенные инфаркт миокарда, чрескожные коронарные вмешательства, аортокоронарное шунтирование;
— ЭКГ в 12 стандартных отведениях (для определения отклонения сегмента ST или других нарушений).
Промежуточный риск:
— приступы стенокардии в покое (> 20 мин.), разрешившиеся в покое или после приема нитроглицерина;
— изменения зубца Т;
— патологические зубцы Q (рубец) на ЭКГ;
— возраст > 70 лет.
Низкий риск: впервые возникшая стенокардия (II или III класса по классификации Канадского сердечно-сосудистого общества (ССS)), отсутствие изменений на ЭКГ.
Отделение реанимации и интенсивной терапии
1. Необходимо продолжать первоначальные лечебные мероприятия, если они начаты на предыдущих этапах.
6. Морфин: в/в при продолжающейся боли, с учетом дозы введенной до госпитализации.
После присвоения пациенту категории «острый коронарный синдром без подъема сегмента ST» должно быть начато пероральное и парентеральное антитромботическое лечение:
1. Аспирин (независимо от стратегии лечения, если не дан ранее, при отсутствии противопоказаний): 150-300 мг (не кишечнорастворимая форма) с последующей дозой 75-100 мг в день (допустимо в/в введение).
3. Тикагрелор: 180 мг, затем по 90 мг, 2 раза в день. Рекомендуется для всех пациентов с умеренным или высоким риском развития ишемических событий (например, повышенный уровень тропонинов), независимо от первоначальной стратегии лечения и включая пациентов, ранее получавших клопидогрел (прием которого следует прекратить в случае, если пациент начинает прием тикагрелора).
1. Фондапаринукс: 2,5 мг в день п/к. Рекомендуется как препарат с наиболее оптимальным профилем безопасности/эффективности в отношении антикоагуляции (I А).
2. Эноксапарин: 1 мг/кг 2 раза в день п/к. Рекомендуется, если фондапаринукс недоступен. Допускается первоначальное в/в введение болюса 30 мг у пациентов с повышенным риском, при возрасте меньше 75 лет (I В). У пациентов с клиренсом креатинина (при отсутствии фондапаринукса или эноксапарина) в/в болюс 60-70 МЕ/кг (максимум 5000 МЕ) с последующей инфузией 12-15 МЕ/кг/ч (максимум 1000 МЕ/ч). Титрование до поддержания АЧТВ (50-70 с) на уровне в 1,5-2,5 выше контрольного (I С). Не рекомендуется использовать с целью контроля гепаринотерапии определение времени свертываемости крови.
Во время выбора стратегии и до перехода из острого состояния в стабильное лучше использовать короткодействующие препараты.
Инвазивная стратегия
Оптимальный расчет времени зависит от профиля риска отдельного пациента и оценивается по нескольким клиническим признакам в ходе лечения и наблюдения.
Пациентов с очень высоким риском ишемических осложнений (с персистирующим ангинозным синдромом, нестабильностью гемодинамических показателей, рефрактерными нарушениями ритма сердца) необходимо немедленно транспортировать в ангиографическую лабораторию.
Можно рассмотреть применение ингибитора рецептора гликопротеинов IIb/IIIa (эптифибатид) у пациентов с признаками очень высокого риска при продолжающейся ишемии и низком риске кровотечений для того, чтобы переждать время до катетеризации.
Пациенты высокого риска, набравшие больше 140 баллов по шкале GRACE и/или при наличии, как минимум, одного критерия высокого риска из нижеуказанных, должны пройти инвазивную оценку в течение 24 часов:
— повышение или снижение уровня тропонинов;
— динамические изменения сегмента ST или зубца Т (с симптомами ишемии или без них);
— сахарный диабет;
— почечная недостаточность (клиренс креатинина 2 );
— снижение функции левого желудочка ( (85 МЕ/кг с учетом АЧТВ или 60 МЕ/кг в случае сопутствующего применения ингибиторов гликопротеинов IIb/IIIa.
Переход на другой антикоагулянт во время стентирования категорически не рекомендуется (за исключением бивалирудина).
Антикоагулянтная терапия в зависимости от достижения стабилизации состояния может быть прекращена через 24 часа после инвазивной процедуры. При консервативном лечении фондапаринукс или эноксапарин могут применяться до выписки из стационара.
Если планируется АКШ, следует прекратить прием клопидогрела/тикагрелора и отложить операцию, только если позволяют клиническое состояние и результаты ангиографии.
Тикагрелор является блокатором рецепторов к АДФ, который не относится к группе тиенопиридинов и вызывает обратимое торможение функции тромбоцитов, что может оказаться важным преимуществом для пациентов, нуждающихся в проведении экстренного АКШ.
Отсутствие критических коронарных поражений не исключает диагноз, если клинические проявления напоминали ишемическую боль в груди и если тест на биомаркеры был положительным. В данной ситуации, пациенты должны получать оптимальную медикаментозную терапию в соответствии с рекомендациями.
Прогноз
Госпитализация
Профилактика
Профилактические мероприятия в острой фазе ИМ
Важнейшее профилактическое значение с первых минут от начала инфаркта имеет антитромбоцитарная и антикоагулянтная терапия. Также целесообразно применение таких препаратов, как β-блокаторы, ингибиторы АПФ, нитраты, блокаторы кальциевых каналов, глюкозо-инсулино-калиевая смесь (ГИК) и др.
Вопрос о необходимости раннего, в том числе внутривенного, назначения бета-блокаторов в острой фазе остается открытым. В настоящее время рекомендуется дождаться стабилизации состояния больного и только после этого назначить бета-блокаторы обычным способом, перорально.
Не обнаружено существенных преимуществ раннего назначения нитратов, поэтому они не рекомендованы для рутинного использования, хотя возможность их применения у отдельных пациентов с продолжающейся ишемией миокарда не исключается.
Напротив, ингибиторы АПФ, назначаемые с первого дня ИМ, не намного, но достоверно уменьшают раннюю летальность больных. Поэтому в руководстве ESC рекомендуется начать прием ингибиторов АПФ в первые 24 часа от начала инфаркта, если нет противопоказаний.
Вторичная профилактика – общие принципы
Около 8-10% пациентов, выживших после ИМ, в течение года после выписки из стационара переживают повторный инфаркт. Летальность постинфарктных больных гораздо выше, чем смертность в общей популяции. На сегодняшний день известен ряд профилактических мероприятий, оказывающих достоверное благоприятное влияние на прогноз и уровень выживаемости таких пациентов.
1. Всем пациентам, перенесшим инфаркт, настоятельно рекомендуется отказаться от курения. Для медикаментозной поддержки больного, который бросает курить, могут использоваться бупропион и никотинсодержащие препараты, антидепрессанты.
2. Показана достаточная и регулярная физическая активность – аэробная нагрузка умеренной интенсивности как минимум 5 раз в неделю. Для больных высокого риска рекомендованы специальные реабилитационные программы с наблюдением медработников.
3. Если индекс массы тела ≥30 кг/м 2 либо окружность талии превышает 102 см у мужчин или 88 см у женщин, необходимо снижение веса. Питание постинфарктных больных должно включать регулярное употребление фруктов, овощей, рыбы, отличаться низким содержанием соли и насыщенных жиров. Целесообразным может быть увеличение потребления омега-3-полиненасыщенных жирных кислот; с этой целью можно включать в рацион жирные сорта рыбы или же принимать рыбий жир. Не следует запрещать пациенту употреблять алкоголь в умеренных количествах.
2. β-блокаторы (независимо от уровня АД или состояния функции левого желудочка).
3. Ингибиторы АПФ (независимо от уровня АД или состояния функции левого желудочка); при непереносимости – блокаторов рецепторов ангиотензина-II.
4. Гиполипидемическую терапию:
— статины рекомендованы у всех пациентов для достижения уровня холестерина липопротеинов низкой плотности (ЛПНП) 150 мг/дл (1,7 ммоль/л) и/или содержание холестерина ЛПВП