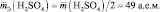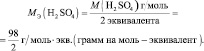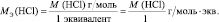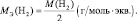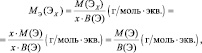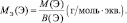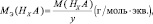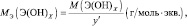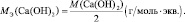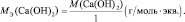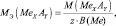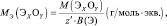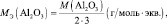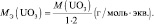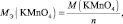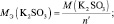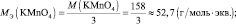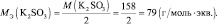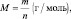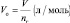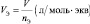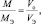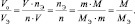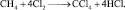Как посчитать молярную массу эквивалента
Эквивалент. Закон эквивалентов
Материалы портала onx.distant.ru
Эквивалент. Закон эквивалентов
Эквивалент – реальная или условная частица вещества Х, которая в данной кислотно-основной реакции или реакции обмена эквивалентна одному иону водорода Н + (одному иону ОН — или единичному заряду), а в данной окислительно- восстановительной реакции эквивалентна одному электрону.
Фактор эквивалентности fэкв(X) – число, показывающее, какая доля реальной или условной частицы вещества Х эквивалентна одному иону водорода или одному электрону в данной реакции, т.е. доля, которую составляет эквивалент от молекулы, иона, атома или формульной единицы вещества.
Наряду с понятием “количество вещества”, соответствующее числу его моль, используется также понятие количество эквивалентов вещества.
Закон эквивалентов: вещества реагируют в количествах, пропорциональных их эквивалентам. Если взято n(экв1) моль эквивалентов одного вещества, то столько же моль эквивалентов другого вещества n(экв2) потребуется в данной реакции, т.е.
При проведении расчетов необходимо использовать следующие соотношения:
1. Молярная масса эквивалента вещества X равна его молярной массе, умноженной на фактор эквивалентности:
2. Количество эквивалентов вещества X определяется делением его массы на молярную массу эквивалента:
3. Объём моль-эквивалента газа Х при н.у. равен молярному объёму газа, умноженному на фактор эквивалентности:
4. Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов составляющих это вещество атомов (ионов).
5. Молярная масса эквивалента оксида равна молярной массе эквивалента элемента плюс молярная масса эквивалента кислорода.
6. Молярная масса эквивалента гидроксида металла равна молярной массе эквивалента металла плюс молярная масса эквивалента гидроксила, например:
М[½Са(ОН)2] = 20 + 17 = 37 г/моль.
М(½ СаSO4) = 20 + 48 = 68 г/моль.
Эквивалент в кислотно-основных реакциях
На примере взаимодействия ортофосфорной кислоты со щелочью с образованием дигидро-, гидро- и среднего фосфата рассмотрим эквивалент вещества H3PO4.
Эквивалент NaOH соответствует формульной единице этого вещества, так как фактор эквивалентности NaOH равен единице. В первом уравнении реакции молярное соотношение реагентов равно 1:1, следовательно, фактор эквивалентности H3PO4 в этой реакции равен 1, а эквивалентом является формульная единица вещества H3PO4.
В третьем уравнении реакции количество веществ реагентов относятся друг к другу как 1:3. Следовательно, фактор эквивалентности H3PO4 равен 1/3, а её эквивалентом является 1/3 часть формульной единицы вещества H3PO4.
Таким образом, эквивалент вещества зависит от вида химического превращения, в котором принимает участие рассматриваемое вещество.
Следует обратить внимание на эффективность применения закона эквивалентов: стехиометрические расчёты упрощаются при использовании закона эквивалентов, в частности, при проведении этих расчётов отпадает необходимость записывать полное уравнение химической реакции и учитывать стехиометрические коэффициенты. Например, на взаимодействие без остатка 0,25 моль-экв ортофосфата натрия потребуется равное количество эквивалентов вещества хлорида кальция, т.е. n(1/2CaCl2) = 0,25 моль.
Эквивалент в окислительно-восстановительных реакциях
Фактор эквивалентности соединений в окислительно-восстановительных реакциях равен:
где n – число отданных или присоединенных электронов.
Для определения фактора эквивалентности рассмотрим три уравнения реакций с участием перманганата калия:
В результате получаем следующую схему превращения KMnO4.
в кислой среде: Mn +7 + 5e = Mn +2
в нейтральной среде: Mn +7 + 3e = Mn +4
в щелочной среде: Mn +7 + 1e = Mn +6
Схема превращений KMnO4 в различных средах
Таким образом, в первой реакции fэкв(KMnO4) = 1/5, во второй – fэкв(KMnO4) = 1/3, в третьей – fэкв(KMnO4) = 1.
Следует подчеркнуть, что фактор эквивалентности дихромата калия, реагирующего в качестве окислителя в кислой среде, равен 1/6:
Примеры решения задач
Задача 1. Определить фактор эквивалентности сульфата алюминия, который взаимодействует со щелочью.
Решение. В данном случае возможно несколько вариантов ответа:
Задача 2. Определить факторы эквивалентности Fe3О4 и KCr(SO4)2 в реакциях взаимодействия оксида железа с избытком хлороводородной кислоты и взаимодействия двойной соли KCr(SO4)2 со стехиометрическим количеством щёлочи КОН с образованием гидроксида хрома (III).
Задача 3. Определить факторы эквивалентности и молярные массы эквивалентов оксидов CrО, Cr2О3 и CrО3 в кислотно-основных реакциях.
CrО3 – кислотный оксид. Он взаимодействует со щёлочью:
Молярные массы эквивалентов рассматриваемых оксидов равны:
Мэкв(CrО) = 68(1/2) = 34 г/моль,
Задача 4. Определить объём 1 моль-экв О2, NH3 и H2S при н.у. в реакциях:
Vэкв(NH3) = 22,4× 1/3 = 7,47 л – в первой реакции.
Vэкв(NH3) = 22,4× 1/5 = 4,48 л – во второй реакции.
В третьей реакции для сероводорода Vэкв(H2S)=22,4 1/6 = 3,73 л.
Задача 5. 0,45 г металла вытесняют из кислоты 0,56 л (н.у.) водорода. Определить молярную массу эквивалента металла, его оксида, гидроксида и сульфата.
Задача 6. Рассчитать массу перманганата калия, необходимую для окисления 7,9 г сульфита калия в кислой и нейтральной средах.
fэкв(K2SО3) = 1/2 (в кислой и нейтральной среде).
В кислой среде Мэкв(KMnO4) = 158·1/5 = 31,6 г/моль, m(KMnO4) = 0,1·31,6 = 3,16 г.
В нейтральной среде Мэкв (KMnO4) = 158·1/3 = 52,7 г/моль, m(KMnO4) = 0,1·52,7 =5,27 г.
Задача 7. Рассчитать молярную массу эквивалента металла, если оксид этого металла содержит 47 мас.% кислорода.
Выбираем для расчётов образец оксида металла массой 100 г. Тогда масса кислорода в оксиде составляет 47 г, а масса металла – 53 г.
В оксиде: nэкв (металла) = nэкв(кислорода). Следовательно:
53:Мэкв(Ме) = 47:(32·1/4). В результате получаем Мэкв(Ме) = 9 г/моль.
Задачи для самостоятельного решения
2.1. Молярная масса эквивалента металла равна 9 г/моль. Рассчитать молярную массу эквивалента его нитрата и сульфата.
Ответ: 71 г/моль; 57 г/моль.
2.2. Молярная масса эквивалента карбоната некоторого металла составляет 74 г/моль. Определить молярные массы эквивалентов этого металла и его оксида.
Ответ: 44 г/моль; 52 г/моль.
2.3. Рассчитать объём 1 моля эквивалента сероводорода (н.у.), который окисляется до оксида серы (IV).
Ответ: 3,73 л.
2.4. Определить молярную массу эквивалента Ni(OH)Cl в реакциях:
Ni(OH)Cl + NaOH = Ni(OH)2 + NaCl.
Ответ: 55,6 г/моль; 111,2 г/моль.
2.5. При взаимодействии 4,8 г неизвестного металла и 13 г цинка с соляной кислотой выделяется одинаковый объём водорода. Вычислить молярные массы эквивалентов металла, его оксида и его хлорида.
Ответ: МЭ(металла)=12 г/моль; МЭ(оксида)=20 г/моль, МЭ(хлорида)=47,5 г/моль.
2.6. Рассчитать молярные массы эквивалентов металла и его гидроксида, если хлорид этого металла содержит 79,7 мас.% хлора, а молярная масса эквивалента хлора равна 35,5 г/моль.
Ответ: МЭ(металла)=9 г/моль; МЭ(оксида)=26 г/моль.
2.7. Какой объём 0,6 М раствора H2O2 пойдёт на окисление 150 мл 2н. раствора FeSO4 в реакции:
Ответ: 250 мл.
2.8. Определить объём хлора (н.у), необходимый для окисления 100 мл 0,5н раствора K2MnO4.
Ответ: 0,56 л.
2.9. 0,66 г кислоты требуются для нейтрализации 10 мл 1М раствора КОН. Найти молярные массы эквивалентов кислоты и ее кальциевой соли в обменной реакции.
Ответ: МЭ(кислоты)=66 г/моль; МЭ(соли)=85 г/моль.
2.10. Бромид металла в результате обменной реакции полностью переведен в сульфат, при этом масса уменьшилась в 1,47 раз. Найти молярную массу эквивалента металла. Определить какой это металл.
Ответ: МЭ(металла)=20 г/моль; Са.
Научная электронная библиотека
§ 2.1.2. Эквивалент
Эквивалент молекулы сложного вещества – это условная часть молекулы, являющаяся носителем одной функциональной связи или одного электрона, участвующего в окислительно-восстановительном процессе.
Эквивалентная масса 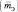
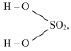
Например, если серная кислота (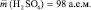
М (Н2 SO4) = 98 г/моль), имеющая структурную формулу:
взаимодействует с NaOH по реакции:
Н2SO4 + 2NaOH = Na2SO4 + 2Н2О, (2.1),
то у неё функциональны две связи Н – О. Вся молекула оказывается носительницей двух функциональных связей, а, значит, двух эквивалентов. Поэтому эквивалентом в данном случае является половина молекулы Н2SO4. Следовательно,
Молярная масса эквивалента (МЭ) – это масса одного моля эквивалента. В данном случае (MЭ(Н2SO4)) для приведённой реакции рассчитывается по формуле:
В аналогичной реакции взаимодействия NaOH с НСl молярная масса эквивалента соляной кислоты численно совпадает с молярной массой НСl:
НСl + NaOH = NaСl + Н2О;
Эквивалент молекулы простого вещества – это условная часть молекулы, являющаяся носителем одной валентности.
Например, молекула водорода состоит из двух атомов, каждый из которых обладает валентностью, равной единице. Поэтому, суммарная валентность молекулы этого простого вещества равна двум. Вся молекула оказывается носительницей двух валентностей, а, значит, согласно последнему определению, двух эквивалентов. Эквивалентом водорода оказывается половина молекулы. Молярная масса эквивалента ((MЭ(Н2)) рассчитывается по формуле:
Следует подчеркнуть, что хотя молекула водорода, также как и молекула соляной кислоты, содержит только одну функциональную связь, однако формулы для расчёта молярных масс эквивалентов этих веществ существенно различаются, потому что одно из них является простым, а другое сложным.
В общем случае, молярные массы эквивалентов (МЭ) рассчитываются следующим образом.
Для простых веществ:
где МЭ(ЭХ) – молярная масса эквивалента простого вещества, состоящего из х атомов элемента Э; М(ЭХ) – молярная масса этого вещества; М(Э) – молярная масса элемента; В(Э) – валентность элемента.
Для элементов (Э), входящих в состав сложного вещества:
То есть, молярные массы эквивалентов простых веществ и молярные массы эквивалентов элементов, входящих в состав сложного вещества, могут рассчитываться по одной и той же формуле.
Для кислот НХА, где А – кислотный остаток:
где y – основность кислоты, т. е. количество ионов H+, принимающих участие в процессе (y ≤ х).
Например, в реакции (2.1) основность серной кислоты равна двум. А для процесса:
Н2SO4 + NaOH = NaНSO4 + Н2О,
основность кислоты равна единице и не совпадает с общим количеством ионов Н+, принимающих участие в процессе.
Для оснований (Э(ОН)Х):
где у’ – кислотность основания, т. е. количество гидроксогрупп, принимающих участие в процессе. (y’ ≤ х).
Например, для реакции:
Са(ОН)2 + 2НСl = СаСl2 + 2Н2О;
Са(ОН)2 + НСl = СаОНСl + Н2О;
Для солей (МеХАу, где Ме – металл):
где В(Ме) – валентность металла; z – количество атомов металла, принимающих участие в процессе (z ≤ х).
где Э – элемент или фрагмент молекулы, неизменяемый в реакции; z′ – количество Э, принимающее участие в процессе.
Например, для реакции:
Аl2O3 + 6HCl = 2АlCl3 + 3H2O;
Э ≡ Al;
UO3 + 2HCl = UO2Cl2 + H2O;
Э ≡ UO2;
Из приведённых примеров видно, что значение молярной массы эквивалента сложных веществ зависит от конкретной реакции, в которой они принимают участие. А значение молярной массы эквивалента элементов, входящих в состав сложного вещества – не зависит от реакции.
Следует подчеркнуть, что рассмотренные выше формулы для нахождения молярных масс эквивалентов сложных веществ, справедливы только в том случае если эти вещества не участвуют в окислительно – восстановительном процессе. Например, в реакции
2КMnO4 + 3 K2SO3 + H2O = 2MnO2 + 3 K2SO4 + 2KOH;
где n – количество электронов, получаемых перманганатом калия
n′ – количество электронов, отдаваемых сульфитом калия. В данном случае
Обобщив, приведённые выше равенства, можно утверждать, что молярную массу эквивалента любого вещества (МЭ) рассчитывают по формуле (2.2):
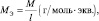
где M – молярная масса вещества, измеряемая в г/моль; l – количество эквивалентов, приходящееся на одну молекулу, численно равное количеству:
– валентностей (для простых веществ);
– функциональных связей (для сложных веществ, не участвующих в окислительно-восстановительном процессе);
– электронов, получаемых или отдаваемых молекулой (для сложных веществ, участвующих в окислительно-восстановительном процессе).
Подобно тому, как молярная масса вещества (М) представляет собой отношение массы (m) к количеству этого вещества (n)
а молярный объём газа (Vo) – отношение объёма (V), занимаемого им при нормальных условиях (p ≈ 105 Па; t °C ≈ 0 °C)[19] к количеству газа (nг):
молярный объём эквивалента газообразного вещества (VЭ) представляет собой отношение V к количеству молярных масс эквивалента nЭ:
из последних двух равенств вытекает соотношение
в котором все величины являются параметрами одного и того же газа.
Задачи для самостоятельного решения
1. Определить молярные массы эквивалентов соединения Н3РО4 в реакциях:
Н3РО4 + 3КОН = К3РО4 + 3Н2О;
Н3РО4 + 2КОН = К2НРО4 + 2Н2О;
Н3РО4 + КОН = КН2РО4 + Н2О.
Рассчитать молярные массы эквивалентов каждого из атомов в Н3РО4.
2. Определить эквивалентную массу Na2SO4 в реакциях:
Na2SO4 + ВаСl2 = ВаSO4 + 2NaСl;
Na2SO4 + H2SO4 = 2NaHSO4.
3. Определить молярную массу эквивалента Na2O в реакциях:
Na2O + 2НСl = 2NaСl + Н2О;
4. Определить эквивалентную массу Аl(OH)3 в реакциях:
2Аl(OH)3 + 3H2SO4 = Аl2(SO4)3 + 6Н2О;
Аl(OH)3 + H2SO4 = АlOHSO4 + 2Н2О.
5. Рассчитать молярную массу эквивалента кислорода и определить объём, занимаемый молярной массой эквивалента кислорода при н.у.
6. Определить эквивалентные массы, молярные массы эквивалента метана (СН4) и хлора в реакции
1. Дайте определения эквиваленту молекулы сложного вещества и эквиваленту молекулы простого вещества?
2. По какой формуле можно рассчитать молярную массу эквивалента любого вещества?
3. Какое уравнение связывает молярную массу, молярный объём, молярную массу эквивалента и молярный объём эквивалента одного и того же газа.
Как посчитать молярную массу эквивалента
МОЛЯРНАЯ МАССА ЭКВИВАЛЕНТА. РАСЧЕТ МОЛЯРНОЙ МАССЫ ЭКВИВАЛЕНТА ЭЛЕМЕНТА В СОЕДИНЕНИИ
Итак, эквивалент всегда в z раз меньше, чем соответствующая формульная единица; следовательно, для некоторого вещества В молярная масса эквивалента М(1/ z В) всегда в z раз меньше молярной массы этого вещества:
М(1/ z В) = 
Молярный объем эквивалента газообразного вещества В всегда в z раз меньше его молярного объема:
V (1/ z В) = 
Для элемента в соединении эквивалентное число z равно его валентности, или степени окисления (С.О.), взятой по модулю:
Решение: а) Для расчета молярной массы эквивалента элемента в соединении используем формулы (1) и (3).
Значение молярной массы атома углерода берем из периодической системы Д.И.Менделеева: М(С)=12 г/моль.
Эквивалентное число углерода в метане С –4 Н4 + равно:
Таким образом, химический эквивалент углерода в соединении СН4 – это условная частица, составляющая 1/4 часть реально существующего атома углерода, или 1/4 С.
Далее рассчитаем молярную массу эквивалента углерода:
M (1/4С) = 

б) Значение молярной массы атома кальция берем из периодической системы Д.И.Менделеева: М(Са)= 40 г/моль.
z (Са) = | С.О. | = | +2 | = 2.
Молярная масса эквивалента кальция составляет:
M (1/2Са ) =

Ответ : а) 12 г/моль; б) 20 г/моль.
Если элемент проявляет постоянную степень окисления во всех соединениях, то для него молярная масса эквивалента всегда одинакова. Такими элементами мы будем считать водород (степень окисления +1) и кислород (степень окисления –2).
М(1/ z Н) =
М(1/ z О) =
Примечание: Водород в соединениях с металлами может проявлять степень окисления –1. Кислород в пероксидах проявляет степень окисления –1, в соединениях с фтором +2.
Эквивалент (стр. 1 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 |
Алтайский государственный технический университет
Бийский технологический институт
Учебно-методическое пособие по неорганической химии
Учебно-методическое пособие по неорганической химии
Издательство Алт. гос. техн. ун-та, 1998. – 26с.
Приведены современная терминология количества вещества в соответствии с рекомендациями ИЮПАК, методические указания к лабораторной работе, контрольные вопросы и задачи для самостоятельной работы студентов.
Учебно-методическое пособие предназначено для студентов всех форм обучения, изучающих курс “Неорганическая химия”.
Рассмотрено и утверждено на заседании
кафедры неорганической и аналитической химии
Протокол № 000 от 06.07.98
кандидат химических наук, доцент
Основные физические величины
Молярная масса вещества
Относительная молекулярная масса
Относительная атомная масса
Фактор эквивалентности вещества
Молярная масса эквивалента вещества
Количество вещества эквивалента
Эквивалентный объем вещества
1 ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
1.1 Основные понятия
Символ количества вещества – n. Количество вещества x записывают как n(x).
Реальные частицы – это атомы, молекулы, ионы, электроны, радикалы и т. д.
Условные частицы –- это какая-то часть реальной частицы, например,1/5 молекулы.
Экспериментально установлено, что в 12 граммах углерода-12 содержится 6,022 ×1023 атомов углерода. Эта величина носит название числа Авогадро. Следовательно, 1 моль атомов, молекул, ионов или каких-либо других объектов содержит Авогадрово число этих объектов, например:
1 моль атомов Mg=6,022×1023 атомов магния,
1 моль ионов Mg2+=6,022×1023 ионов магния,
1 моль молекул KMnO4= 6,022×1023 молекул перманганата калия.
Примеры записи количества вещества:
Количество вещества n(x) находят как отношение массы вещества m к его молярной массе M(x):

Примеры записи: Mr(HCl)=36,52 и M(HCl)=36,52г/моль;
Фактор эквивалентности fЭ(x) – число, обозначающее, какая доля реальной частицы вещества х эквивалентна одному иону водорода в данной кислотно-основной реакции или одному электрону в данной окислительно-восстановительной реакции.
Пример: В реакции окисления-восстановления fЭ(KMnO4)=1/5, следовательно, в данной реакции молекула KMnO4 взаимодействует с 5 электронами, а на один электрон приходиться 1/5 часть молекулы.
Эквивалент Э(х) – реальная или условная частица вещества х, которая в данной кислотно-основной реакции эквивалентна одному иону водорода или в данной окислительно-восстановительной реакции – одному электрону.
Молярная масса эквивалента вещества х – (МЭ(х)) – масса одного моля эквивалента этого вещества. Она равна произведению фактора эквивалентности на молярную массу вещества х:
Количество вещества эквивалента – nЭ(х) – количество вещества в молях, в котором частицами является эквиваленты. Его находят как отношение массы вещества к молярной массе эквивалента вещества:

Пример: Дано: m(Ca(OH)2)=0,74г,

Эквивалентный объем или объем моля эквивалентов 
Пример: Найти эквивалентный объем водорода.
Решение: Эквивалент водорода, согласно уравнению реакции: 
Для того, чтобы определить величину эквивалента какого-либо вещества, надо исходить из конкретной реакции, в которой участвует данное вещество. В этой связи целесообразно рассматривать нахождение эквивалента применительно к трем основным типам химических реакций:

Запишем уравнение (4) в иной форме:

Согласно уравнениям (4), (5), на всех участников реакций приходится два иона водорода. Для того, чтобы найти эквивалент, разделим правую и левую части уравнения (5) на два:

или в молекулярной форме:

Тогда один ион водорода будет эквивалентен 1/2 иона Са2+, одному иону ОН–, 1/2 иона 
Следовательно, факторы эквивалентности будут равны:
А эквиваленты этих веществ будут выражаться формулами:
Полученные результаты позволяют сделать вывод, что для кислот и оснований фактор эквивалентности можно рассчитать по числу ионов водорода Н+ или гидроксильных групп ОН–, которыми обмениваются каждая из молекул со своими партнерами, т. е.
отсюда эквиваленты кислот и оснований равны:
б) Ионно-обменные реакции
В реакции (11) эквивалент можно найти косвенным путем, введя вспомогательные реакции:
Перемножим все члены уравнения (13) на 3. Тогда при суммировании правых и левых частей уравнений 14 и 15 получим уравнение 5. (Следовательно преобразования сделаны верно!)

Из уравнений реакций (14), (15) следует, что одному иону водорода эквивалентна 1/6 молекулы Al2(SO4)3 и 1/2 молекулы BaCl2. Факторы эквивалентности для этих веществ равны:
А эквиваленты выражены формулами:
Если уравнения (14) и (15) написать в ионной форме, то для солей фактор эквивалентности может быть найден по числу замещаемых, присоединяемых и т. д. катионов (Kat) или анионов (An), умноженных на их заряд, т. е.


где n – число замещаемых, присоединяемых и т. д. катионов или анионов,
Z–заряд соответствующего иона.
в) Окислительно-восстановительные реакции
Рассмотрим реакцию, протекающую по уравнению:
В данной реакции изменяют степени окисления олово и железо. Запишем для каждого для них соответствующую полуреакцию:


Согласно полуреакциям (18), (19), один ион олова реагирует с двумя электронами, а ион железа – с одним электроном. Следовательно, Э(Sn2+)=1/2Sn2+, Э(Fe3+)= Fe3+.
Примечание: Если известна молярная масса М(х) и молярная масса эквивалента МЭ(х) данного вещества, то фактор эквивалентности можно рассчитать по формуле:
А эквивалент будет равен:

Для элемента величина, обратная его фактору эквивалентности, есть не что иное, как его валентность В:
Равенства эти столь очевидны, что предлагаем студентам самим провести логическое обоснование их справедливости.
1.3 Закон эквивалентов
Закон этот формулируется следующим образом:
Все вещества реагируют друг с другом в эквивалентных соотношениях.
Смысл этого закона заключается в том, что моль эквивалентов одного вещества реагируют точно с молем эквивалентов другого вещества, а n молей эквивалентов одного вещества с n молями эквивалентов другого вещества (nэ(А) = nэ(В)).
Математически закон эквивалентов можно записать следующим образом:

где m(А) – масса вещества А,
MЭ(A)–молярная масса эквивалента вещества А,
MЭ(В) – молярная масса эквивалента вещества В.
В тех случаях, когда в реакции участвуют газы, целесообразно выражать закон эквивалентов не через единицы массы, а через объемы, так как объем газа при постоянных температуре и давлении прямо пропорционален его массе:

где 



В практике встречаются случаи, когда одно из реагирующих веществ находится в твердом состоянии, а второе в газообразном. В этом случае закон эквивалентов можно выразить формулой:

2 экспериментальная часть
Существует достаточно много методов определения эквивалента вещества: метод вытеснения водорода из кислоты, метод прямого определения, аналитический метод, электрохимический метод, титрование. Выбор той или иной методики определяется свойствами вещества и возможностями исследователя.
В данной лабораторной работе студентам предлагается определить эквивалент вещества по методу вытеснения водорода, основанному на измерении объема водорода, который выделяется из кислоты при действии на нее металла. Ограниченность данного метода в том, что он пригоден для узкого круга веществ, а именно только для металлов, стоящих в ряду напряжений до водорода. Однако, несомненным его достоинством является простота, быстрота проведения эксперимента и хорошая воспроизводимость результатов.
Для желающих ознакомиться с другими методами в приложении дана краткая информация.
2.1 Методика эксперимента
Для проведения опыта соберите прибор, изображенный на рисунке 1, тщательно соединяя части прибора в местах стыковки, чтобы обеспечить его герметичность.
Количество металла рассчитайте, исходя из условия получения не более 200 мл водорода при н. у.

Рисунок 1- Прибор для определения эквивалента металла
Взвесьте рассчитанное количество металла с точностью до 0,01 г. В колбу 4 налейте разбавленной (1:2) соляной кислоты столько, чтобы она при горизонтальном положении колбы не вылилась в горло колбы. Внутреннюю поверхность горла колбы вытрите полоской фильтровальной бумаги, закрепите колбу на штативе, придав ей горизонтальное положение. Соблюдая осторожность, поместите взвешенный металл (навеску) в горле колбы так, чтобы он не упал в кислоту до начала опыта. Цилиндр заполните до верху водой, переверните и быстро опустите в кристаллизатор, заполненный водой наполовину. (Как перевернуть цилиндр с водой, не пролив из него воду?). Закрепите цилиндр в штативе и подведите под него газоотводную трубку от колбы.
До начала опыта необходимо произвести замер объема водяного столба в цилиндре. Записать показания термометра и барометра.
Давление насыщенных паров воды 
Затем осторожным постукиванием колбы переместите металл в кислоту. По окончании реакции дайте колбе охладиться 5. 6 мин. и проведите замеры объема всего водяного столба в цилиндре и от поверхности воды в кристаллизаторе.
Экспериментальные данные запишите в таблицу 1.