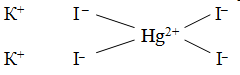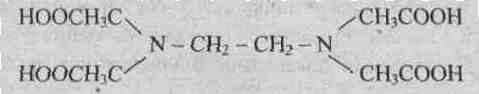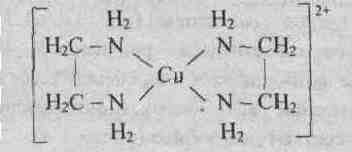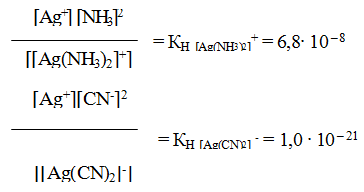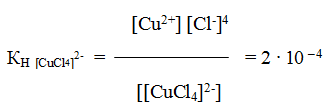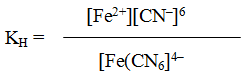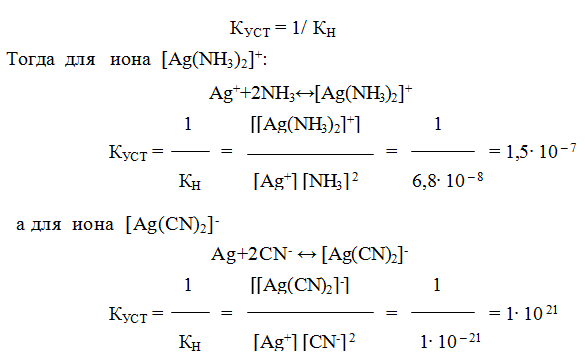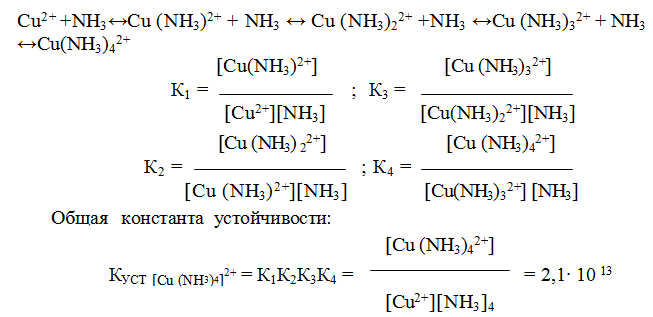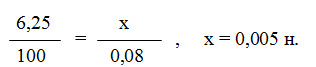Как посчитать координационное число комплексообразователя
Урок №15. Комплексные соединения
Na 2 [Zn(OH) 4 ] →2Na + + [Zn(OH) 4 ] 2-
Ионы противоположного знака, связанные с комплексным ионом, образуют внешнюю сферу.
Комплексный ион состоит из комплексообразователя и лигандов и образует внутреннюю сферу (внутреннюю сферу заключают в квадратные скобки).
Координационное число зависит:
от природы центрального атома;
условий образования комплексов.
Виды комплексов
Соединения с комплексными анионами
Соединения с комплексными катионами
[Ag(NH 3 ) 2 ]Cl – хлорид диамминсеребра
[Al(H 2 O) 5 OH]SO 4 – сульфат гидроксопентаакваалюминия
[Pt(H 2 O)(NH 3 ) 2 OH] NO 3 – нитрат гидроксодиамминакваплатины (II)
Соединения без внешней сферы
[Pt(NH 3 ) 2 Cl 2 ] – дихлородиамминплатина (II)
[Co(NH 3 ) 3 Cl 3 ] – трихлоротриамминкобальт (III)
Номенклатура
в названиях комплексных ионов сначала указываются лиганды;
название комплексного иона завершается названием металла с указанием его степени окисления (римским цифрами в скобках);
в названиях комплексных катионов используются русские названия металлов;
в названиях комплексных анионов используются латинские названия металлов: Al –алюминат, Cr – хромат, Fe – феррат;
Как посчитать координационное число комплексообразователя
Основы современной координационной теории были изложены в конце прошлого века швейцарским химиком Альфредом Вернером, обобщившим в единую систему весь накопившийся к тому времени экспериментальный материал по комплексным соединениям. Им были введены понятия о центральном атоме (комплексообразователь) и его координационном числе, внутренней и внешней сфере комплексного соединения, изомерии комплексных соединений, предприняты попытки объяснения природы химической связи в комплексах.
Все основные положения координационной теории Вернера используются и в настоящее время. Исключение составляет его учение о природе химической связи, которое представляет сейчас лишь исторический интерес.
Образование комплексного иона или нейтрального комплекса можно представить себе в виде обратимой реакции общего типа:
M + n L 
В комплексных ионах комплексообразователями являются медь(II), кремний(IV), железо(II), бор(III).
Чаще всего комплексообразователем служит атом элемента в положительной степени окисления.
Отрицательные условные ионы (т.е. атомы в отрицательной степени окисления) играют роль комплексообразователей сравнительно редко. Это, например, атом азота(-III) в катионе аммония [NH 4 ] + и т.п.
Атом-комплексообразователь может обладать нулевой степенью окисления. Так, карбонильные комплексы никеля и железа, имеющие состав [Ni(CO) 4 ] и [Fe(CO) 5 ], содержат атомы никеля(0) и железа(0).
Комплексообразователь (выделен синим цветом) может участвовать в реакциях получения комплексов, как будучи одноатомным ионом, например:
так и находясь в составе молекулы:
P H 3 + H + 
B F 3 + NH 3 
В комплексной частице может быть два и более атомов-комплексообразователей. В этом случае говорят о многоядерных комплексах.
Лиганды, как правило, не связаны друг с другом, и между ними действуют силы отталкивания. В отдельных случаях наблюдается межмолекулярное взаимодействие лигандов с образованием водородных связей.
Примером гексадентатного лиганда может служить анион этилендиаминтетрауксусной кислоты:
Полидентатные лиганды могут выступать в роли мостиковых лигандов, объединяющих два и более центральных атома.
Важнейшей характеристикой комплексообразователя является количество химических связей, которые он образует с лигандами, или координационное число ( КЧ ). Эта характеристика комплексообразователя определяется главным образом строением его электронной оболочки и обусловливается валентными возможностями центрального атома или условного иона-комплексообразователя (подробнее см. >>>).
Когда комплексообразователь координирует монодентатные лиганды, то координационное число равно числу присоединяемых лигандов. А число присоединяемых к комплексообразователю полидентатных лигандов всегда меньше значения координационного числа.
Значение координационного числа комплексообразователя зависит от его природы, степени окисления, природы лигандов и условий (температуры, природы растворителя, концентрации комплексообразователя и лигандов и др.), при которых протекает реакция комплексообразования. Значение КЧ может меняться в различных комплексных соединениях от 2 до 8 и даже выше. Наиболее распространенными координационными числами являются 4 и 6.
В аквакомплексах координационное число комплексообразователя в степени окисления +II чаще всего равно 6:
Известны комплексообразователи, которые обладают практически постоянным координационным числом в комплексах разных типов. Таковы кобальт(III), хром(III) или платина(IV) с КЧ 6 и бор(III), платина(II), палладий(II), золото(III) с КЧ 4. Тем не менее большинство комплексообразователей имеет переменное координационное число. Например, для алюминия(III) возможны КЧ 4 и КЧ 6 в комплексах и
Координационные числа 3, 5, 7, 8 и 9 встречаются сравнительно редко. Есть всего несколько соединений, в которых КЧ равно 12 – например, таких как K9 [Bi(NCS) 12 ].
Лиганды, непосредственно связанные с комплексообразователем, образуют вместе с ним внутреннюю (координационную) сферу комплекса.
Так, в комплексном катионе внутренняя сфера образована атомом комплексообразователя – меди(II) и молекулами аммиака, непосредственно с ним связанными.
Обозначается внутренняя сфера квадратными скобками:
В зависимости от соотношения суммарного заряда лигандов и комплексообразователя внутренняя сфера может иметь положительный заряд, например, либо отрицательный, например, или нулевой заряд, например, как для
При растворении в воде комплексные соединения необратимо диссоциируют на ионы:
Кислоты с комплексными анионами в водном растворе подвергаются необратимому протолизу :
в котором реализуется четверная связь Re – Re: одна σ-связь, две π- связи и одна δ-связь. Особенно большое число кластерных комплексов насчитывается среди производных d-элементов.
Многоядерные комплексы смешанного типа содержат как связь комплексообразователь–комплексообразователь, так и мостиковые лиганды.
Примером комплекса смешанного типа может служить карбонильный комплекс кобальта состава [Co 2 (CO) 8 ], имеющий следующее строение:
Здесь имеется одинарная связь Co – Co и два бидентатных карбонильных лиганда CO, осуществляющих мостиковое соединение атомов-комплексообразователей.
Комплексные соединения. Комплексообразователи, лиганды
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Комплексные соединения
9.1. Определение комплексных соединений. Такие соединения, как оксиды, кислоты, основания, соли образованы из атомов в результате возникновения между ними химической связи. Это соединения обычные, или соединения первого порядка.
Однако имеются вещества, которые образованы в результате соединения друг с другом нейтральных молекул без возникновения новых связующих электронных пар. Например:
Это молекулярные соединения, или соединения высшего порядка. Одни из них диссоциируют в водном растворе на простые ноны, например:
другие — на сложные (комплексные) ионы, состоящие, в свою очередь, из более простых ионов, как, например:
Молекулярные соединения, образующие комплексные ионы, способные к существованию как в растворе, так и в кристалле, называют комплексными. Но такое определение применимо лишь в известных пределах. Оно не охватывает соединений типа неэлектролитов, например карбонилов металлов —Ni(CO)4 и др., а потому не является и полным.
Чтобы объяснить, почему происходит присоединение одних простых молекул к другим, швейцарский химик А. Вернер ввел понятие о главной и побочной валентности. Тогда образование, скажем, K2[HgI4] можho представить так: ион ртути за счет своей главной валентности (обозначается сплошной линией), равной двум, присоединяет два иодид-иона, а за счет побочной – (обозначается пунктиром) — дополнительно еще два иодид-иона. По Вернеру, это может быть изображено формулой
В настоящее время главную валентность надо объяснить ионной или ковалентной связью, а побочную – ковалентной связью, возникшей по донорно-акцепторному механизму (см. раздел 4.8.2.). Исходя из механизма образования комплексных соединений, им можно дать более точное, не имеющее исключений определение: комплексные соединения – это соединения, характеризующиеся наличием хотя бы одной ковалентной связи, возникшей по донорно-акцепторному механизму.
9.2. Комплексообразователи. Комплексообразователями служат атомы или ионы, имеющие вакантные орбитали. Способность к комплексообразованию возрастает с увеличением заряда иона и уменьшением его размера. К наиболее распространенным комплексообразователям относятся ионы d-элементов VII, VIII, I и II групп периодической таблицы элементов.
Динатриевая соль ЕДТА и сама кислота относятся к классу соединений, называемых комплексонами. Би- и полидентантные лиганды при взаимодействии с комлексообразователями образуют замкнутые циклы, называемые хелатными, поэтому и комплексы с би- и полидентантными лигандами называют хелатными (или клешневидными), например
Пример 1. Определите заряд комплексного иона, координационное число (к.ч.) и степень окисления комплексообразователя в соединениях: a) K4[Fe(CN)6]; б) Na[Ag(NO2)2]; в) K2[MoF8]; г) [Сr(Н2O)2(NН3)3С1]С12.
Решение. Заряд комплексного иона равен заряду внешней сферы, но противоположен ему по знаку. Координационное число комплексообразователя равно числу лигандов, координированных вокруг него. Степень окисления комплексообразователя определяется так же, как степень окисления атома в любом соединении, исходя из того, что сумма степеней окисления всех атомов в молекуле равна нулю. Заряды нейтральных молекул (H2O, NН3) равны нулю. Заряды кислотных остатков определяют из формул соответствующих кислот. Отсюда:
| Заряд иона | К.ч. | Степень окисления | |
| а) | -4 | 6 | +2 |
| б) | -1 | 2 | +1 |
| в) | -2 | 8 | +6 |
| г) | +2 | 6 | +3 |
9.4. Номенклатура комплексных соединений. Название комплексного катиона записывается одним словом, начинающимся с названия отрицательного лиганда с прибавлением буквы «о», затем приводятся нейтральные молекулы и центральный атом с указанием римской цифрой его степени окисления для металлов переменной валентности. Для молекул Н2О (аква), NН3 (аммин), СО (карбонил), NO (нитрозил) даются особые названия, указанные в скобках.
Число лигандов обозначают греческими приставками (ди-, три-, тетра- и т.д.) или бис-, трис-, тетракис-, пентакис- и гексакис- для 2, 3, 4, 5 и 6 соответственно у сложных лигандов. Например, соединение [Zn(NH3)2Cl]CI называется хлорид хлородиамин цинка (II), а [Ni(En)2]Cl2 – хлорид бис(этилендиамин) никеля (II).
Комплексный анион записывается аналогично названию катиона, но с добавлением суффикса -«am» к названию комплексообразователя, например K2[Zn(CN)4] – тетрацианоцинкат (II) калия. Нейтральный комплекс записывается подобно катиону, например комплекс [Ni(CО)4] называется тетракарбонил никеля (II). Соответственно по типу лигандов комплексы называют аквакомплексы (лиганд Н2О), аминокомплексы (лиганд NH3), ацидокомплексы (лиганды анионы кислот), комплексонатные комплексы (лиганды-комплексоны) и т.д.
9.5. Диссоциация комплексных соединений. Комплексные соединения — неэлектролиты в водных растворах диссоциации не подвергаются. У них отсутствует внешняя сфера комплекса, например: [Zn(NH3)2Cl2], [Co(NH3)3(NO3)3], [Pt (NH3)2C12]. В водной среде такие молекулы гидратируются как единое образование.
Комплексные соединения — электролиты при диссоциации в водных растворах образуют комплексные ионы, например:
Такая диссоциация протекает полностью, ионы гидратируются. Комплексные ионы в свою очередь подвергаются вторичной диссоциации:
Однако эта диссоциация обычно протекает в незначительной степени. Применяя закон действующих масс к обратимым процессам (а) и (б), получаем выражения констант нестойкости комплексных ионов:
Соединения с малоустойчивой внутренней сферой называют двойными солями. Обозначают их иначе, чем комплексные соединения, а именно — как соединения молекул, например K2SO4∙A12(SO4)3. Принципиальной же разницы между двойными солями и комплексными соединениями нет. В растворе двойной соли имеется некоторое количество комплексных ионов (например, [Al (SO4)2] – ). Двойная соль отличается от комплексной соли лишь диссоциацией комплексного иона: у первой она практически полная, а у второй — незначительная.
Двойные соли — довольно распространенные соединения. К ним относятся соль Мора (NH4)2SO4∙FeSO4∙6H2O, двойной хлорид калия и меди 2КС1 ∙ СuС12 ∙ 2Н2О и многие другие. Если, например, растворить в воде двойной хлорид, то происходит диссоциация
и все образовавшиеся в растворе ионы можно обнаружить с помощью соответствующих реакций. Но если это соединение рассматривать как комплексное, то его формулу надо изобразить как K2[CuС14]∙2H2О. Диссоциация K2[CuС14]∙2H2О протекает по уравнению:
Образующийся комплексный ион устойчив только в концентрированных растворах, и его константа нестойкости при комнатной температуре
Решение. Если комплексная соль гексацианоферрат (II) калия, являясь сильным электролитом, в водном растворе необратимо диссоциирует на ионы внешней и внутренней сфер
то комплексный ион диссоциирует обратимо и в незначительной степени на составляющие его частицы:
Обратимый процесс характеризуется своей константой равновесия, которая в данном случае называется константой нестойкости (Кн) комплекса:
Чем меньше KH, тем более прочен данный комплекс.
9.6. Константы устойчивости комплексов. Для характеристики устойчивости (прочности) комплексного иона применяют также величину, обратную константе нестойкости. Ее называют константой устойчивости (КУСТ) или константой образования комплекса. Величины КН и КУСТ взаимосвязаны:
Очевидно, чем выше КУСТ, тем прочнее комплексный ион и тем больше его концентрация при равновесии.
Следует подчеркнуть, что как диссоциация комплексного иона, так и его образование являются процессами обратимыми и протекают ступенчато, как у слабых электролитов. Каждой ступени соответствует определенная величина константы устойчивости – К1, К2 …, Кn. Ион [Ag(NH3)2] + будет иметь две константы устойчивости — K1 и K2:
У иона [Cu(NH3)4] 2+ будет четыре константы устойчивости, так как комплексообразователь в четыре стадии присоединяет лиганд NH3
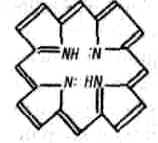
9.7.Роль комплексных соединений. Комплексные соединения широко распространены в природе. В состав многих растений и живых организмов входят соединения с макроциклическими лигандами. В упрощенном виде тетрадентантный макроцикл порфин представлен на рис. 3.3
Рис. 3.3. Структура молекул порфина
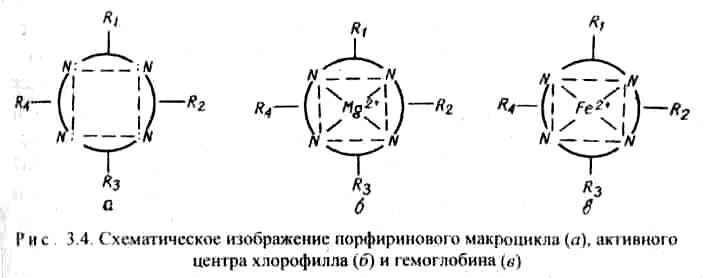
Комплексы с участием порфина называются порфи-ринами. Они отличаются друг от друга центральными ионами-комплексообразователями и заместителями, присоединенными к атомам углерода на периферии лиганда. В наиболее простом виде порфиновый цикл представлен четырьмя атомами азота, соединенными углеродными цепями (рис. 3.3). Кроме того, имеются четыре или более заместителей – радикалов R1, R2, R 3, R4. В зеленом катализаторе фотосинтеза – хлорофилле роль комплексообразователя выполняет магний (рис. 3.4). Макроциклический комплекс железа входит в состав гемоглобина (рис. 3.4).
Железо координирует кислород в комплексе гемоглобина и переносит его по организму с кровью. Связь кислорода с железом в комплексе не очень прочная и поэтому кислород в организме легко реагирует с восстановителями. Недостаток железа в организме приводит к болезни – анемии. Макроциклы крови могут взаимодействовать с каталитическими ядами, например, монооксидом углерода СО, что приводит к отравлению организма.
Пример 1. Вычислите жесткость воды, зная, что в 500 л ее содержится 202,5 г Са(НСО3)2.
Приведенные примеры решают, применяя формулу Ж = m / (mЭ ∙ V)
где: т – масса вещества, обусловливающего жесткость воды или применяемого для устранения жесткости, мг;
mэ, – молярная масса эквивалента этого вещества;
Решение. В 1 л воды содержится 202,5 : 500 = 0,405 г Са(НСО3)2, что составляет 0,405 : 81 = 0,005 ммоль/л. 81 г/моль — эквивалентная масса Са(НСО3)2. Следовательно, жесткость воды 5ммоль. (Ж = т / (mэV)= 202 500 / (81 • 500) = 5 ммоль. 81 – эквивалентная масса Са(НСО3)2, равная половине его молярной массы).
Пример 2. Сколько граммов CaSO4 содержится в 1 м 3 воды, если жесткость, обусловленная присутствием этой соли, равна 4 ммоль?
Решение. Молярная масса CaSO4 136,14 г/моль; молярная масса эквивалента равна 136,14:2 = 68,07 г/моль. В 1 м 3 воды жесткостью 4 ммоль содержится 4 · 1000 = 4000 ммоль, или 4000 · 68,07 = 272 280 мг = 272,280 г CaSO4. Из формулы Ж = m / (mэV),m = 468,071000 = 272 280 мг = 272,280 г CaSO4).
Пример 3. Какую массу соды надо добавить к 500 л воды, чтобы устранить ее жесткость, равную 5 ммоль?
Решение. В 500 л воды содержится 500 · 5 = 2500 моль солей, обусловливающих жесткость воды. Для устранения жесткости следует прибавить 2500 · 53 = 132 500 мг = 132,5 г соды (53 г/моль — молярная масса эквивалента Na2CO3).
Пример 4. Вычислите карбонатную жесткость воды, зная, что на титрование 100 см 3 этой воды, содержащей гидрокарбонат кальция, потребовалось 6,25 см 3 0,08 н. раствора НС1.
Решение. Вычисляем молярную концентрацию эквивалентов раствора гидрокарбоната кальция. Обозначив число эквивалентов растворенного вещества в 1 л раствора, через х, составляем пропорцию:
Координационные числа некоторых основных комплексообразователей
Важнейшей количественной характеристикой любого лиганда является его дентатность. Она представляет собой число атомов из одной частицы-лиганда, которые непосредственно связаны с комплексообразователем.
Дентатность лигандов-молекул NH3, H2O и CO равна 1. Если лигандами являются анионы, то очень часто их дентатность равна абсолютному значению их заряда (хотя может быть и меньше).
В любой комплексной частице координационное число комплексообразователя равно сумме дентатностей всех лигандов.
Заряд внешней сферы КС всегда равен по абсолютному значению, но противоположен по знаку заряду внутренней сферы, который, в свою очередь, равен алгебраической сумме зарядов центрального атома и лигандов.
Пример 1.10.1. Рассмотрим строение ряда комплексных соединений:
| Структурный элемент КС | Комплексные соединения | |||||
| [Cr(H2O)6]Cl3 | K[Ag(CN)2] | [Pd(NH3)2SO4] | K[Cо(NH3)3PO4] | |||
| Внутренняя сфера | [Cr(H2O)6] 3+ | [Ag(CN)2] – | [Pd(NH3)2SO4] | [Cо(NH3)3PO4]ˉ | ||
| Внешняя cфера | Cl – | K + | — | K + | ||
| Комплексообразователь и его КЧ | Cr 3+ 6 | Ag + 2 | Pd 2+ 4 | Co +2 | ||
| Лиганд и его дентатность | H2O | CN – 1 | NH3 1 | SO4 2– 2 | NH3 | PO4 3– |
Классификация комплексных соединений
В зависимости от знака заряда внутренней сферы различают:
3) Катионно-анионные КС, например [Cu(NH3)4][Zn(CN)4], состоят из двух внутренних сфер, одна из которых – катион, а другая – анион.
4)Нейтральные КС, например [Pt(NH3)2Cl2] 0 не имеют внешней сферы.
Особую группу составляют хелатные (клешневидные) комплексные соединения, в которых атомы комплексообразователей и атомы лигандов образуют циклические группировки, состоящие чаще всего из 5 или 6 атомов. К таким соединениям относятся, например, внутрикомплексные соединения.
Внутрикомплексные соединения– хелатные соединения, в которых каждый лиганд связан с комплексообразователем двумя ковалентными связями, одна из которых образована по обменному, а другая – по донорно-акцепторному механизму. Такие соединения широко распространены в живой природе. Важнейшими из них являются, например, гем крови и хлорофилл.
В зависимости от природы лигандов комплексные соединения делят на следующие основные типы:
1) Ацидокомплексы (от лат. acidum – кислота), в которых лиганды – кислотные остатки, например K4[Fе(СN)6], Na3[Ag(S2O3)2].
2) Гидроксокомплексы, в которых лиганды – гидроксид-анионы, например K[Au(OH)4], Na3[Al(OH)6].
3) Aквакомплексы (от лат. aqua – вода) или гидраты, в которых лиганды – молекулы воды, например, [Сr(Н2О)6]Сl3, [Cu(H2O)6](ClO4)2.
4)Aмминкомплексы или аммиакаты, в которых лиганды – молекулы аммиака, например [Cu(NH3)4]SO4, [Pt(NH3)6]Cl4.
Номенклатура комплексных соединений
В названиях катионных КС применяется русскоязычное наименование комплексообразователя в родительном падеже, например Сu 2+ –меди(II), Fe 3+ – железа(III).
Наименования анионных КС состоят из корня латинского названия комплексообразователя и русскоязычного суффикса «ат», например Сu 2+ – купрат(II), Fe 3+ –феррат(III).
В случае нейтральных КС используют русское название комплексообразователя в именительном падеже, например, Сu 2+ –медь(II), Fe 3+ – железо(III).
Названия нейтральных лигандов:Н2О – «аква», NH3 – «аммин», СО – «карбонил», NO – «нитрозил», N2H4 – «гидразин».
Названия лигандов-анионов. Если латинское название аниона заканчивается суффиксом «ид», его заменяют на букву «о»: F – – фторо, СN – –циано, S 2– – тио, OH – – гидроксои т. д. Исключение: Н – – гидридо.
Если латинское название аниона заканчивается суффиксом «ат» или «ит», то к нему добавляется буква «о»: 


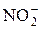
Для обозначения числа одинаковых лигандов во внутренней сфере комплекса в качестве приставок перед их названиями используют греческие числительные: ди; три; тетра; пента; гекса и т. д. Приставку моно не употребляют. Название внутренней сферы записывают в одно слово.
Названия комплексных соединений
Порядок названия комплексных соединений аналогичен порядку названий обычных солей, т. е. сначала указывается анион в именительном падеже, а затем катион в родительном падеже. Формулы комплексов читаются строго справа налево с соблюдением указанного в них порядка расположения лигандов.
Пример 1.10.2. Приведите примеры координационных соединений различных типов и назовите их.
K[Pt(NH3)Br5] – – пентабромoамминплатинат(IV) калия;
K4[Fe(CN)6] 4– – гексацианоферрат(II) калия.
Диссоциация комплексных соединений в водных растворах
Различают первичную и вторичную диссоциацию КС в растворах. Первичная диссоциация заключается в том, что катионные и анионные КС необратимо распадаются на ионы внешней и внутренней сфер, например:
КС катионно-анионного типа при этом также необратимо распадаются на комплексные катионы и комплексные анионы;
Вторичной диссоциации подвергаются комплексные частицы (внутренние сферы). Они обратимо и постадийно диссоциируют на составные части. Например, при вторичной диссоциации комплексный анион [Ag(NH3)2] + обратимо и по стадиям отщепляет частицы лигандов – молекулы NH3. Поскольку в растворе при этом устанавливаются динамические равновесия, каждой стадии вторичной диссоциации соответствует своя константа равновесия. Она называется константой нестойкости (Kнест) комплексного иона по данной стадии:
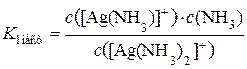

При этом всегда K1 нест > K2 нест. Но поскольку они отличаются не очень сильно, часто используют общую константу нестойкости комплексного иона Kнест. Она является константой равновесия суммарного процесса вторичной диссоциации:

Для каждого комплексного иона при данной температуре Kнест – постоянная величина (приложение 4). Чем меньше ее значение, тем устойчивее комплексный ион в растворе, тем слабее протекает его вторичная диссоциация и наоборот.
Величина, обратная общей константе нестойкости комплексного иона, называтся общей константой его устойчивости Kуст:
Соответственно чем больше Kуст комплексного иона, тем он устойчивее в растворе и наоборот.
Константы нестойкости комплексных ионов слабо зависят от температуры.
Пример 1.10.3. Напишите координационную формулу сульфата гексаамминкобальта(III). Укажите заряд и координационное число комплексообразователя, заряд внутренней сферы. Напишите уравнения первичной и вторичной диссоциации и выражение константы нестойкости комплексного иона.
2) Уравнение первичной диссоциации КС (по типу сильного электролита):
3) Общее уравнение вторичной диссоциации комплексного иона (по типу слабого электролита):
5) Выражение общей константы нестойкости комплексного иона:
Реакции с участием комплексных ионов
Реакции ионного обмена
К таким реакциям относятся, например, многочисленные реакции обмена КС с обычными солями. При этом КС обмениваются с ними своими составными частями – внешней или внутренней сферами, например:
Такие реакции протекают необратимо, если приводят к образованию малорастворимых продуктов.
Реакции лигандного обмена
Равновесия таких процессов всегда смещены в сторону более устойчивых комплексных ионов с меньшими значениями Kнест. Например,
Реакции связывания лигандов
Реакции осаждения комплексообразователей
Их суть состоит в том, что при добавлении к раствору КС специальных реагентов, содержащиеся в них ионы соединяются с ионами комплексообразователя, образуя малорастворимые вещества. Так, например, при добавлении раствора KI к раствору хлорида диамминсеребра [Ag(NH3)2]Cl выпадает осадок AgI, вследствие чего комплексные ионы разрушаются:
Это происходит потому, что ионы I – образуют с ионами Ag + чрезвычайно мало растворимый иодид серебра.
0,05 моль/дм 3 х моль/дм 3 5 моль/дм 3
3.Значения концентраций частиц подставим в выражение константы нестойкости комплексного иона:
5.Рассчитаем значение ПК ионов Ag + и Cl – в растворе после смешивания:
Пример 1.10.5. Будет ли разрушаться комплексный ион [Ag(NH3)2] + в условиях примера 10.4 при замене KCl на KI?
Реакции полного восстановления
комплексообразователей
В ходе таких реакций комплексообразователь восстанавливается до простого вещества и выделяется из раствора в виде металлического осадка. Так, например, при добавлении цинка в раствор дицианоаурата(I) калия выделяется чистое золото:
Zn 0 + 2K[Au + (CN)2] → Au 0 ↓ + K2[ 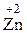
Эта реакция длительное время использовалась для промышленного получения золота по методу Багратиона.
Химическая связь в комплексных соединениях.
Геометрическая форма комплексных частиц
Между ионами внешней и внутренней координационных сфер осуществляется ионная связь. Внутри комплексных частиц центральные атомы связаны с лигандами ковалентными связями, образованными по обменному и по донорно-акцепторному механизмам.
Для наглядного объяснения образования химической связи в комплексных частицах и их геометрической формы удобно использовать метод валентных связей (МВС).
Согласно этому методу химические связи между атомами комплексообразователей и лигандами образуются по донорно-акцепторному механизму, а геометрическая форма комплексных частиц определяется типом гибридизации орбиталей центральных атомов (табл. 4).
Важнейшие типы гибридизации орбиталей и соответствующие им
геометрические конфигурации комплексных частиц
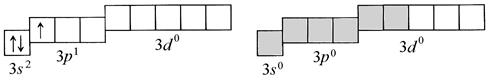
Рис. 1. Схемы распределения валентных орбиталей в атоме и в катионе алюминия
 |
 |
Вопросы для самостоятельной подготовки
1. Сформулируйте основные положения координационной теории
А. Вернера и проиллюстрируйте их на примерах.
2. Какие частицы выступают в роли комплексообразователей? Перечислите наиболее типичные из них. Что характеризует координационное число комплексообразователя? От каких факторов оно зависит?
3. Чем объясняется особая склонность атомов и катионов d-элементов выступать в качестве комплексообразователей?
4. Какие частицы выступают в роли лигандов? Приведите примеры электронейтральных и заряженных лигандов. Чему равна их дентатность и что она характеризует? Приведите примеры моно-, би-, три- и тетрадентатных лигандов.
5. Какие лиганды называются хелатирующими? Приведите примеры.
6. Может ли молекула метана быть лигандом? Ответ поясните.
7. Как классифицируются комплексные соединения в зависимости от заряда комплексной частицы? Приведите примеры.
8. Как можно рассчитать заряд комплексной частицы; комплексообразователя; внешней координационной сферы? Приведите примеры.
9. Назовите комплексные соединения:
Определите тип каждого КС; заряд комплексообразователя и его КЧ; дентатность лигандов.
10. Напишите уравнения первичной и вторичной диссоциации следующих КС: тетратиоцианодиамминхромат(III) аммония; карбонат нитратотриамминмеди(II); дицианодиамминпалладий(II). Приведите выражения общих констант нестойкости соответствующих комплексных частиц.
11. Каков тип химической связи между внешней и внутренней координационными сферами КС?
12. Каков тип химической связи между центральным атомом и лигандами?
13. Как происходит образование комплексных частиц согласно МВС?
14. На основе МВС объясните образование и геометрическую форму комплексных частиц: катиона тетраакважелеза(II); гексафтороалюминат-аниона; тетракарбонилникеля(0).
15. Какие типы изомерии присущи комплексным соединениям? Приведите примеры.
16. В чем заключается различие между комплексными соединениями и двойными солями?
17. При отравлениях соединениями Hg, Pb, Cu, Ag, Cd, Be в качестве противоядий из подручных средств принимают яичный белок или молоко. На чем основано их использование в данном случае?
18. В каких случаях в медицине используются хелатирующие лиганды, в том числе и трилон-Б? На чем основано их применение?
19. Что представляет собой гем крови? Почему гемоглобин способен взаимодействовать как с кислородом, так и с угарным газом?
Задачи и упражнения
312.Составьте максимально возможное число формул комплексных частиц (катионных, анионных, нейтральных), в состав которых могут входить:
а) комплексообразователи – Cr +3 (KЧ = 6); Pb +2 (KЧ = 4); Ag + (KЧ = 2);
Определите заряды комплексных частиц.
314.Напишите координационные формулы следующих комплексных соединений: нитрат карбонатоакватриамминкобальта(III); дибромотетрацианоплатинат(IV) калия; сульфатотиоцианотриаквахром(III). Чему равны координационные числа комплексообразователей и дентатность лигандов в этих соединениях? Напишите уравнения электролитической диссоциации комплексных соединений и соответствующие выражения общих констант нестойкости комплексных частиц.
315.Из раствора КС условного состава PtCl4 · 6NH3 нитрат серебра осаждает весь хлор в виде хлорида серебра, а из раствора соли PtCl4 · 3NH3 – только 1/4 часть входящего в ее состав хлора. Напишите координационные формулы и назовите эти КС. Укажите координационное число платины в каждом из них. Как диссоциироуют эти КС в растворе?
316.У двух КС кобальта одинаковая эмпирическая формула – CoBrSO4 · 5NH3. Одна из них в растворе реагирует только с хлоридом бария, а другая – только с раствором нитрата серебра, образуя в обоих случаях осадки. Напишите координационные формулы этих КС и назовите их. Приведите выражения констант нестойкости соответствующих комплексных ионов.
317.К раствору, содержащему КС условного состава CoCl3 · 4NH3 массой 0,2335 г, добавили в достаточном количестве раствор AgNO3. Масса образовавшегося при этом осадка составила 0,1435 г. Определите координационную формулу КС и назовите его. Напишите уравнения его первичной и вторичной диссоциации и выражение общей константы нестойкости комплексного иона.
318.Напишите в молекулярной и ионно-молекулярной формах уравнения обменных реакций между:
в) K3[Fe(CN)6] и AgNO3, имея в виду, что образующиеся КС нерастворимы в воде. Приведите их названия.
319.Напишите уравнения реакций образования комплексных кислот и оснований при взаимодействии: PtCl2 и HCl; AgCl и HCl; PbCl2 и HCl; AlF3 и HF; Pd(CN)2 и HCN; BF3 и HF; Cu(OH)2 и NH3; Ni(OH)2 и NH3. (Координационные числа комплексообразователей определите по правилу Вернера.) Приведите уравнения первичной и вторичной диссоциации полученных соединений.
320.Напишите координационные формулы следующих комплексных соединений:
а) гексанитрокобальтат(III) калия;
б) амминнитротетрахлорокобальтат(III) аммония;
в) трифторогидроксобериллат галлия(III);
г) тетратиоцианодиамминхромат(III) аммония.
Укажите для каждого КС координационное число комплексообразователя и заряд внутренней сферы.
322.Как объяснить, что комплексный катион [Ag(NH3)2] + разрушается уже при слабом подкислении раствора, а катион [Pt(NH3)4] 2+ сохраняется даже при действии концентрированных кислот?
а) почему осадок AgCl не растворяется в соляной кислоте, но растворяется в растворе аммиака?;
б) почему осадок AgI не растворяется в растворе аммиака, но растворяется в иодоводородной кислоте?
324.Чем определяется возможность замены одних лигандов в комплексных частицах на другие? Определите направление реакций в растворах:
325.Рассчитайте молярную концентрацию ионов комплексообразователей в водных растворах КС, концентрации которых составляют:
а) гидроксид диамминмеди(I) – 0,3 моль/дм 3 ;
329.Какие комплексные ионы образуются при растворении амфотерных гидроксидов цинка и алюминия в растворах кислот и в растворах щелочей?
331.Допишите приведенные ниже уравнения реакций. Укажите, к какому типу относится каждая из них и чем определяется направление ее протекания:
332.Напишите уравнения реакций, соответствующих превращениям:
Как объяснить возможность осуществления каждого из них?
2. НЕОРГАНИЧЕСКАЯ ХИМИЯ
2.1. Примерная схема описания группы
элементов, их атомов и образованных ими
простых и сложных веществ
1.Общие сведения о химических элементах (положение в таблице периодической системы, открытие, содержание в земной коре, основные природные соединения).
2.Электронные конфигурации атомов в основном и в возбужденном энергетических состояниях.
3.Закономерности изменения атомных характеристик элементов по группам (относительная атомная масса, ковалентный, металлический и ионный радиусы, энергия ионизации, сродство к электрону, электроотрицательность, степени окисления).
4.Важнейшие физико-химические свойства простых веществ (аллотропные (полиморфные) модификации, их агрегатное состояние, цвет, плотность, температуры плавления и кипения, электропроводность).
5.Способы получения простых веществ (лабораторные и промышленные).
6.Химические свойства простых веществ:
а) реакции с простыми веществами (водородом, галогенами, кислородом, серой, азотом, фосфором, углеродом, кремнием, металлами);
б) реакции с важнейшими реагентами – сложными веществами (водой, основными и кислотными оксидами, кислотами, основаниями, солями).
7.Строение, химические свойства и получение основных типов соединений.
а) Бинарные соединения:
· соединения с водородом;
· соединения с другими неметаллами;
· соединения с металлами.
б) Многоэлементные соединения:
· гидроксиды (кислотные, основные, амфотерные);
8.Взаимосвязь между основными типами соединений.
10.Биологическая роль простых веществ и соединений элементов в процессах жизнедеятельности человека и животных. Применение в медицине.
Вопросы для самостоятельной подготовки
1.Как изменяются в ряду галогенов по мере увеличения их атомных номеров радиусы атомов, энергии ионизации, сродство к электрону, электроотрицательность атомов, энергия химической связи в молекулах и их термическая устойчивость?
2. Какие степени окисления проявляют а. ч. галогенов в соединениях? Каковы особенности валентных состояний фтора?
3. Запишите уравнения реакций, отражающих промышленные и лабораторные способы получения галогенов.
4. Охарактеризуйте окислительно-восстановительные свойства простых веществ галогенов и сформулируйте соответствующие закономерности. Напишите уравнения соответствующих реакций.
5. Напишите уравнения реакций, использующихся для получения галогеноводородов в промышленности и в лабораторной практике. Каковы особенности этих процессов?
6. Как изменяются физические свойства, полярность и прочность молекул в ряду HF – HI?
7. Проанализируйте и объясните характер изменения окислительно-восстановительных и кислотных свойств в ряду галогеноводородов.
8. Напишите уравнения реакций взаимодействия галогенов с водой и растворами щелочей (холодными и горячими).
9. Напишите уравнения реакций разложения хлорноватистой кислоты под действием света; при нагревании; в присутствии водоотнимающего вещества?
10. Напишите уравнения реакций, использующихся для получения хлоратов и перхлоратов в промышленности и в лаборатории.
11. Какие галогены и в каких условиях вытесняют бром из бромида калия; бромата калия? Ответ обоснуйте, используя данные о стандартных электродных потенциалах. Напишите уравнения соответствующих реакций.
12. Как и почему изменяются кислотные и окислительные свойства в рядах:
HClO – HClO2 – HClO3 – HClO4 и HClO – HBrO – HIO?
13. Что такое хлорная известь; жавелевая вода? Где они находят применение? Напишите уравнения реакций их получения?
14. Сравните гидролизуемость солей и объясните характер ее изменения в рядах:
15. Можно ли получить оксиды галогенов взаимодействием соответствующих простых веществ? Напишите уравнения реакций, использующихся для получения важнейших оксидов хлора.
17. Какие соединения хлора, фтора, брома и иода применяются в медицине?
18. Неизвестный галогеноводород пропустили в раствор щелочи массой 100 г с массовой долей КОН 11,2 %. В образовавшемся нейтральном растворе массовая доля соли оказалась равной 13,89 %. Определите галогеноводород.
19. Рассчитайте объем хлора (н. у.) и объем раствора гидроксида калия с его массовой долей 50 % и плотностью 1,538 г/мл, необходимых для получения бертолетовой соли массой 250 г, если ее выход равен 88 %.
20. Напишите уравнения реакций, при помощи которых можно осуществить превращения:
21. Напишите уравнения следующих реакций:
а) K2Cr2O7 + HCl (конц)
г) I2 + HNO3 (конц)
Вопросы для самостоятельной подготовки
1.Рассмотрите строение и валентные состояния атомов элементов группы VI-А.
2.Как изменяются радиусы, энергии ионизации, сродство к электрону и электроотрицательность атомов в ряду кислород – полоний? Как это можно объяснить?
3.Как и почему изменяется агрегатное состояние и состав простых веществ в ряду O – Po? Какие аллотропные модификации образуют элементы этой группы?
4.Каков характер изменения окислительно-восстановительных свойств простых веществ в ряду кислород – полоний? Ответ подтвердите уравнениями соответствующих химических реакций.