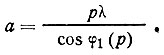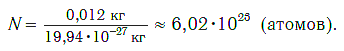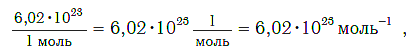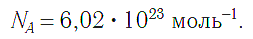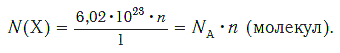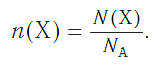Число формульных единиц
Зная модель кристаллической структуры, т. е. пространственное расположение атомов относительно элементов симметрии в элементарной ячейке — их координаты, а, следовательно, и характеристики правильных систем точек, которые занимают атомы, можно сделать ряд кристаллохимических выводов, используя достаточно простые приемы описания структур. Поскольку 14 выведенных решеток Браве не могут отразить все многообразие известных к настоящему времени кристаллических структур, необходимы характеристики, позволяющие однозначно описать индивидуальные особенности каждой кристаллической структуры. К таким характеристикам, дающим представление о геометрическом характере структуры, относятся: координационные числа (КЧ), координационные многогранники (КМ), или полиэдры (КП), и число формульных единиц (Z). Прежде всего по модели можно решить вопрос о типе химической формулы рассматриваемого соединения, т. е. установить количественное соотношение атомов в структуре. Это нетрудно сделать на основе анализа взаимного окружения — взаимной координации — атомов разных (или одинаковых) элементов.
 | ||
| а | б | в |
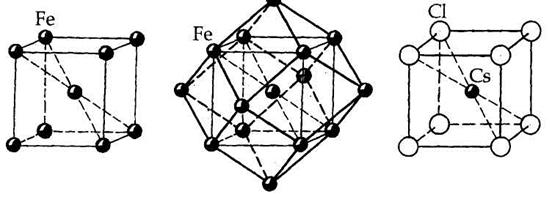
| Рис. 7.2. Кристаллические структуры α-Fe (а и б) и CsCl (в). |
В структуре α –Fe координационное число атома Fe по первой координационной сфере равно 8, с учетом второй сферы — 14 (8 + 6). Координационные полиэдры — соответственно куб и ромбододекаэдр.
Координационные числа и координационные многогранники являются важнейшими характеристиками конкретной кристаллической структуры, отличающими ее от остальных структур. На этой основе можно проводить классификацию, относя конкретную кристаллическую структуру к определенному структурному типу.
Установить тип химической формулы по структурным данным (т. е. по модели структуры или по ее проекции — чертежу) можно и иным путем, подсчитав число атомов каждого сорта (химического элемента), приходящихся на одну элементарную ячейку. Это подтверждает тип химической формулы NaCl.
В структуре NаС1 (рис. 7.4), типичной для ионных кристаллов типа АВ (где А—атомы (ионы) одного сорта, В—другого), в построении элементарной ячейки принимают участие 27 атомов обоих сортов, из них 14 атомов А (шары большого размера) и 13 атомов В (меньшие шары), но полностью входит в ячейку лишь один. атом, находящийся в ее центре. Атом, находящийся в центре грани элементарной ячейки, принадлежит одновременно двум ячейкам—данной и смежной с ней. Поэтому данной ячейке принадлежит лишь половина этого атома. В каждой из вершин ячейки сходится одновременно по 8 ячеек, поэтому данной ячейке принадлежит лишь 1/8 атома, расположенного в вершине. От каждого атома, находящегося на ребре ячейки, ей принадлежит лишь 1/4.
Вычислим общее число атомов, приходящихся на одну элементарную ячейку NаС1:
| Положение атома | Объем входящих в ячейку | Число атомов | Всего в ячейку приходится |
| В вершине В середине ребра В центре грани В центре ячейки | 1/8 1/4 1/2 |
Итак, на долю ячейки, показанной на рис. 7.4, приходится не 27 атомов, а всего 8 атомов: 4 атома натрия и 4 атома хлора.
 |
 — Cl — Cl  — Na — Na |
| Рис.7.4 Структура каменной соли |
Определение числа атомов в ячейке Браве позволяет кроме типа химической формулы получить еще одну полезную константу — число формульных единиц, обозначаемое буквой Z. Для простых веществ, состоящих из атомов одного элемента (Сu, Fe, Se и др.), число формульных единиц соответствует числу атомов в элементарной ячейке. Для простых молекулярных веществ (I2, S8 и т. д.) и молекулярных соединений (СО2) число Z paвно числу молекул в ячейке. В подавляющем же большинстве неорганических и интерметаллических соединений (NaCl, CaF2, СuАu и т. д.) молекул нет, и в этом случае вместо термина «количество молекул» используют термин «число формульных единиц».
Число формульных единиц можно определить экспериментально в процессе рентгеновского исследования вещества.
Как посчитать число формульных единиц
§ 1. Параметры решетки и число формульных единиц в ячейке
Параметры элементарной ячейки а, b, с входят непосредственно в условия Лауэ, их легко определить по положению дифракционных рефлексов на рентгенограммах.
Наиболее простой метод решения задачи состоит в оценке параметра по слоевым линиям рентгенограммы вращения (см. гл. II, § 8). Положение слоевых линий на рентгенограмме определяет растворы дифракционных конусов, коаксиальных оси вращения кристалла, а следовательно (через соответствующее условие Лауэ),
и период повторяемости в узловых рядах, параллельных оси вращения. Если с осью вращения совмещена ось X кристалла, то по расстоянию между p-той и экваториальной слоевой линией lp и радиусу кассеты R (см. рис. 33, а) можно определить угол раствора конуса: lp/R=ctgφ(р). Отсюда, используя условие Лауэ, находим параметр а:
Из трех рентгенограмм вращения (или вращательного качания) определяются все три линейных параметра решетки: а, b и с.
Точность определения этим методом периодов повторяемости невысока. Но его преимущество заключается в том, что для нахождения параметров не требуется знания всех трех индексов каждого рефлекса.
По геометрии размещения рефлексов на рентгенограммах можно оценить и угловые параметры решетки. Последнее существенно только при исследовании моноклинных и триклинных кристаллов.
Экспериментально определяемая плотность (например, пикнометрическим или флотационным методом) относится к реальному кристаллу, имеющему трещины и другие дефекты. Обычно она несколько ниже плотности идеального кристалла, и поэтому формула (22), как правило, дает несколько заниженный (не целочисленный) результат.
Как посчитать число формульных единиц
Ключевые слова конспекта: химическая формула, индекс, коэффициент, качественный и количественный состав, формульная единица.
Химическая формула — это условная запись состава вещества посредством химических знаков и индексов.

Если требуется обозначить не одну, а несколько молекул (или отдельных атомов), то перед химической формулой (или знаком) ставят соответствующую цифру, которую называют коэффициентом. Например, три молекулы воды обозначаются 3Н2О, пять атомов железа — 5Fe. Индекс 1 в химических формулах и коэффициент 1 перед химическими символами и формулами не пишут.
Запись 5Н2О (пять-аш-два-о) следует понимать так: пять молекул воды образованы десятью атомами водорода и пятью атомами кислорода.
| ЗАДАНИЕ. Обозначить, используя символы химических элементов а) три молекулы азота б) семь молекул сульфида железа в) четыре атома серы г) два атома кальция д) семь молекул воды е) четыре молекулы кислорода ж) две молекулы сернистой кислотыОТВЕТ: а) три молекулы азота — 3N2 б) семь молекул сульфида железа — 7FeS в) четыре атома серы — S4 г) два атома кальция — Ca2 д) семь молекул воды — 7H2O е) четыре молекулы кислорода — 4O2 ж) две молекулы сернистой кислоты — 2H2SO3Объяснение: коэффициенты показывают количество молекул, индексы — количество атомов. Формулы молекул простых веществ нужно запомнить. Одноатомные молекулы образуют инертные газы гелий He, неон Ne, аргон Ar и другие. Из двухатомных молекул состоят водород H2, кислород O2, азот N2, галогены F2, Cl2, Br2, I2. Три атома — в молекулах озона O3, четыре — в молекулах белого фосфора P4. |
По химической формуле мы можем дать веществу название, определить его качественный и количественный состав, а также подсчитать его относительную молекулярную массу.Химическая формула показывает, из атомов каких элементов состоит вещество (то есть качественный состав вещества); и каково соотношение атомов этих элементов (то есть количественный состав вещества).
Формульная единица
Химические формулы веществ, имеющих немолекулярное строение, например FeS, не описывают состав молекулы; а только показывают соотношение элементов, образующих данное вещество.
Так, кристаллическая решётка поваренной соли — хлорида натрия состоит не из молекул, а из ионов. На каждый положительно заряженный ион натрия в ней приходится один отрицательно заряженный ион хлора. Получается, что отношение индексов в записи NaCl совпадает с отношением; в котором химические элементы соединяются между собой, образуя вещество. По отношению к веществам, имеющим немолекулярное строение, такую запись правильнее называть не формула, а формульная единица.
В таком случае величина Мr должна называться не относительной молекулярной массой, а относительной формульной массой. Тем не менее по традиции выражение «относительная молекулярная масса» используют и по отношению к веществам немолекулярного строения.
Конспект урока «Химическая формула. Индекс и коэффициент. Формульная единица«.
Урок 8. Химическое количество вещества и моль
В уроке 8 «Химическое количество вещества и моль» из курса «Химия для чайников» выясним, что такое химическое количество вещества; рассмотрим моль в качестве единицы количества вещества, а также познакомимся с постоянной Авогадро. Напоминаю, что в прошлом уроке «Относительная молекулярная и относительная формульная массы» мы научились вычислять относительную молекулярную массу, а также относительную формульную массу веществ; кроме того, выяснили что такое массовая доля и привели формулу для ее вычисления.
Любое чистое вещество имеет свою химическую формулу, т. е. характеризуется определенным качественным и количественным составом.
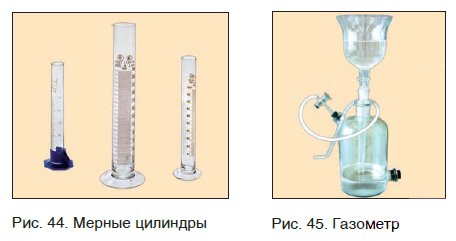
Если необходима какая-то порция твердого вещества, то для этого следует взять нужную его массу, т. е. взвесить вещество (рис. 43). Нужный объем жидкого вещества обычно отмеряют с помощью мензурки или мерного цилиндра (рис. 44). Для отбора необходимой порции (объема) газообразных веществ применяют специальные емкости — газометры (рис. 45).
Следовательно, объем и масса — это величины, характеризующие данную порцию вещества.
Химическое количество вещества
В жизни мы часто не различаем понятия «масса» и «количество». А это разные понятия. Когда вы говорите: «Я купил 2 кг груш», то здесь речь идет о массе груш. Но если вы говорите: «Я купил 10 груш», то в этом случае речь идет о количестве груш. Массу вещества измеряют в граммах, килограммах, тоннах, а количество — в штуках.
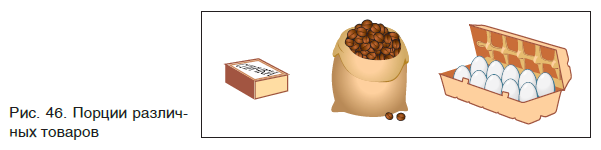
Груши можно пересчитать поштучно, а если это, например, зерна? Тут уже посчитать каждое зернышко даже в небольшой емкости сложно. Поэтому зерно обычно продают мешками, т. е. определенными порциями. В каждой такой порции — мешке (если они равны по массе и все зерна одинаковы) — будет находиться практически одно и то же число зерен. Подобным образом продают многие товары. Например, яйца — десятками, спички — спичечными коробками, в каждом из которых находится по 45 спичек (рис. 46).
В химической практике, помимо массы или объема, необходимо знать число структурных единиц (атомов, молекул, формульных единиц), которые содержатся в данной порции вещества, поскольку именно они участвуют в химических реакциях. Поэтому в химии, как и в других естественных науках, используют физическую величину, характеризующую число частиц в рассматриваемой порции вещества. Эта физическая величина называется количеством вещества или, как следует называть ее при химических расчетах, — химическое количество вещества.
Химическое количество вещества — физическая величина, пропорциональная числу структурных единиц, содержащихся в данной порции вещества.
Другими словами, химическое количество вещества — это порция данного вещества, содержащая определенное число его структурных единиц. Химическое количество вещества обозначают латинской буквой n . Это одна из семи основных физических величин Международной системы единиц (СИ).
Моль — единица химического количества вещества
Каждая из основных физических величин имеет свою единицу. Например, единица длины — метр (м), массы — килограмм (кг), времени — секунда (с). Единицей химического количества вещества является моль.
Моль — порция вещества (т. е. такое его химическое количество), которая содержит столько же структурных единиц, сколько атомов содержится в углероде массой 0,012 кг.
Сокращенное обозначение единицы химического количества записывается, как и полное, — моль. Поэтому, если слово «моль» стоит после числа, то оно не склоняется, так же, как и другие сокращенные единицы величин: 3 кг, 5 л, 8 моль. При чтении вслух и при записи числительного буквами слово «моль» склоняется: три килограмма, пять литров, восемь молей.
На заметку. Термины «молекула» и «моль», как нетрудно заметить, однокоренные. Они действительно произошли от одного и того же латинского слова «moles». Но это слово имеет, по крайней мере, два значения. Первое — «маленькая масса». Именно в этом смысле в XVII в. оно превратилось в термин «молекула». А понятие «моль» (в смысле кучка, порция) появилось значительно позже, в начале ХХ в. Автор этого термина известный немецкий химик и физик Оствальд толковал его смысл как «большая масса», как бы противопоставляя термину «молекула».
получила название постоянной Авогадро. Она является одной из важнейших универсальных постоянных и обозначается символом NA :
Единица в числителе дроби (1/моль) заменяет название структурной единицы.
если 1 моль вещества содержит 6,02·10 23 молекул, то n моль вещества содержат N(Х) молекул.
И наоборот, по числу структурных единиц можно рассчитать химическое количество вещества:
Пример 1. Определите число молекул, содержащихся в серной кислоте химическим количеством 3 моль.
Пример 2. Рассчитайте химическое количество CuSO4 в порции, содержащей 36,12·10 23 формульных единиц (ФЕ).
Краткие выводы урока:
Надеюсь урок 8 «Химическое количество вещества и моль» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Лабораторная работа № 14



Лабораторная работа № 13
Расчёт плотности поликристаллических материалов рентгенографическим методом
Введение
Цель работы— изучить методику расчета плотности кристаллических веществ, используя результаты рентгенографического эксперимента, и рассчитать рентгенографическую плотность заданного кристаллического вещества.
Плотность — одно из наиболее важных свойств материалов, характеризующее соотношение между массой и объемом и в значительной мере определяющее их потребительские свойства, а также экономические показатели производства и реализации товарной продукции.
Методы определения объемной, относительной и насыпной плотности твердых материалов условно можно разделить на две основные группы: объемно-весовые и основанные на использовании физических констант. Теоретическую плотность кристаллических веществ нередко и притом наиболее точно определяют с помощью рентгенографического метода (рассчитанная таким образом плотность носит название рентгенографической).
Рентгенографический метод определения плотности обладает рядом преимуществ: не требует специальных приборов, устройств и приспособлений для определения массы и размеров образца, не зависит от других физических свойств вещества (достаточно микронавески порошкового образца массой не более 1 г).
Термины и определения
IIлотность — мера количества вещества (массы) в единице объема:
Плотность, определенная для однородных веществ, может рассматриваться как теоретическая. Плотностью, близкой к теоретической, обладают, как правило, металлы, жидкости, некоторые полимеры и др. Для неоднородных веществ используют понятие «средняя плотность».
Объемная плотность — величина, определяемая отношением массы неоднородного вещества ко всему занимаемому им объему, включая имеющиеся в нем поры и пустоты, Vе, кг/м 3 : r= т/Vе.
Для инженерных расчетов используются понятия «относительная плотность» и «насыпная плотность».
Относительная плотность— отношение плотности вещества r к плотности эталонного вещества rэт при определенных внешних условиях:
Плотность твердых и жидких материалов обычно сравнивают с плотностью воды при температуре 4°С (1000 кг/м3).
Насыпная плотность — масса единицы объема свободно насыпанных дисперсных материалов (например, цемент, песок, минеральная вата и др.).
Сингония кристаллов — классификационный признак симметрии элементарной ячейки кристалла, характеризующийся соотношениями между ее параметрами.
Основы теории
1.1. Параметры, сингония и объемэлементарной ячейки.
В природе твердые вещества могут находиться в аморфном и кристаллическом состоянии. В аморфных веществах атомы (молекулы) расположены беспорядочно, произвольно. Для кристаллических веществ характерно упорядоченное взаимное расположение атомов, ионов и молекул. К кристаллическим веществам относятся металлы и их сплавы в твердом состоянии.
Рис. 1.Кристаллографические сингонии: а — кубическая; б — тетрагональная; в — ромбическая; г — моноклинная; д — триклинная; е — тригональная;
ж — гексагональная
Строение кристаллического вещества графически изображается в виде кристаллической решетки, которая состоит из элементарных ячеек. Элементарные ячейки по признаку симметрии делятся на семь сингоний, каждая из которых характеризуется определенным соотношением между длинами ребер и углами между ними: кубическую, гексагональную, тетрагональную, тригональную, ромбическую, моноклинную и триклинную (рис. 1). Кубическая решетка является простейшей кристаллической решеткой твердого тела.
Длины ребер в элементарной ячейке кристалла относятся к параметрам кристаллической решетки. В частности, кубическую решетку определяет один параметр — длина ребра куба.
Координационное число — число ближайших равноудаленных соседних атомов, окружающих каждый атом в кристалле. Коэффициент компактности решетки h — отношение объема, занятого атомами, ко всему объему решетки. Числом формульных единиц Z называют число атомов, приходящихся на одну элементарную ячейку.

Объем элементарной ячейки кристаллического вещества определяется исходя из сингонии ее кристаллической ячейки и формально-геометрических соображений (приложение П1).
1.2. Понятие о числе атомов в элементарной ячейке.
Большинство металлов образуют одну из следующих кристаллических решеток с плотной упаковкой атомов: объемно-центрированную кубическую (ОЦК), гранецентрированную кубическую (ГЦК) и гексагональную плотно упакованную (ГНУ) (рис.2). Зная вид кристаллической решетки, можно рассчитать число атомов в элементарной ячейке.
На одну элементарную ячейку объемно-центрированной кубической ячейки приходятся два атома: один в центре куба, а другой — располагающийся в вершине куба (каждый атом в вершине куба принадлежит одновременно восьми сопряженным элементарным ячейкам, и, таким образом, на данную ячейку приходится лишь 1/8 массы этого атома, а на всю ячейку — 1/8 8 = 1 атом) (рис. 2, а).
Рис.2.Кристаллические решетки металлов: а — объемно-центрированная кубическая; б — гранецентрированная кубическая; в —. гексагональная плотно
упакованная
На элементарную ячейку гранецентрированной кубической решетки приходятся четыре атома: из них один образуется за счет атомов в вершинах куба, а три — суммарная (1/2 * 6 = 3) доля атомов, находящихся в серединах граней, так как каждый из этих атомов принадлежит двум ячейкам.
На элементарную ячейку гексагональной плотноупакованной решетки приходятся шесть атомов: 3 + (1/6 * 12) + (1/2 * 2) = 6.
1.3. Расчет рентгенографической плотности кристаллических веществ
При определении плотности по данным рентгенографического анализа используется связь значений плотности вещества (металл, минерал) с атомными массами составляющих его элементов и объемом, занимаемым ими.
r = 
Так как параметры элементарной ячейки измеряются в ангстремах


Для химических соединений вместо A подставляют SAi т.е. грамм-формульный вес. Атомная молекулярная масса веществ Aв рассчитывается по справочным данным (приложение П2).
Объем элементарной ячейки для известных кристаллических веществ определяется по справочным данным об их параметрах и сингонии. Для расчета плотности веществ с неизвестными параметрам элементарной ячейки необходимо снять рентгенограмму вещества и рассчитать эти параметры.
Значение рассчитанной таким образом рентгенографической плотности кристаллического материала характеризует идеализированную кристаллическую решетку с реальными параметрами. Справочные значения плотности кристаллических веществ, как правило, будут отличаться от рентгенографической в меньшую или большую сторону. Эта разница может быть вызвана наличием в реальных кристаллах примесей, дефектов кристаллической решетки, внутренних напряжений.
Практическая часть
2.1. Порядок расчета
2.1.1. Получить у преподавателя вариант индивидуального задания. в соответствии с п. 2.2.
2.1.2. Рассчитать плотность вещества (число формульных единиц определить, исходя из сведений о кристаллической структуре заданного материала и геометрических представлений).
2.1.3. Сравнить полученные результаты расчета со справочными данными приложений П2 и П3.
2.2. Примерный перечень кристаллических материалов для выполнения индивидуальных заданий
Примечание.Твёрдость некоторых веществ в перечне приведена в единицах шкалы твёрдости Мооса.
Формулы для расчета объема элементарной ячейки
Атомные веса и плотности некоторых химических элементов
| Химический элемент | Атомный номер | Атомный вес | Плотность г/см3 |
| Аl | 13 | 26,97 | 2,7 |
| Аg | 47 | 107,880 | 10,5 |
| Аu | 79 | 197,2 | 19,3 |
| С | б | 12,01 | 2,3 |
| Са | 20 | 40,08 | 1,5 |
| Сl | 17 | 35,457 | 0,0032 |
| Сu | 29 | 63,57 | 8,9 |
| Fе | 26 | 55,85 | 7,9 |
| К | 19 | 39,102 | 0,86 |
| Na | И | 22,997 | 0,97 |
| Ni | 28 | 58,69 | 8,9 |
| O | 8 | 16,000 | 0,0014 |
| РЬ | 82 | 207,21 | 11,3 |
| S | 16 | 32,06 | 2,0 |
| Si | 14 | 28,06 | 2,3 |
| Sn | 50 | 118,70 | 7,3 |
| Zn | 30 | 65,38 | 7,1 |
Плотности некоторых минералов
| Минерал | Плотность, г/см3 | Минерал | Плотность, г/см3 | Минерал | Плотность, г/см3 |
| Алмаз | 3,47—3,56 | Графит | 2,09—2,23 | Сера | 2,08 |
| Гематит | 5,274 | Мусковит | 2,834 | Гипс | 2,13 |
| Галит | 2,163 | Магнетит | 5,2 | Пирит | 5,016 |
| Галенит | 7,597 | Кварц | 2,648 | Кальцит | 2,712 |
1. Расчет рентгенографической плотности трех кристаллических материалов.
2. Рисунки кристаллических решеток расчетных материалов.
3. Краткое объяснение полученных результатов.
4. Ответить устно на вопросы.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Назовите основные типы кристаллических решеток.
2. Для каких материалов используется понятие “средняя плотность”?
3. Что такое “насыпная плотность”?
4. Что такое “относительная плотность”?
5. Что такое “объемная плотность”?
6. Какие сингонии кристаллов вам известны?
7. Что такое “сингонии кристаллов”?
8. Назовите основные методы определения объемной, насыпной и относительной плотности.
9. В чем преимущества рентгенографического метода?
10. Что такое координационное число?
11. Что такое :коэффициент компактности” кристаллической решетки?
12. Что показывает число формульных единиц?