Муравьиная кислота, получение, свойства, химические реакции
Муравьиная кислота, получение, свойства, химические реакции.
Муравьиная кислота (также – метановая кислота) – органическое вещество, относящееся к насыщенным одноосновным карбоновым кислотам.
Муравьиная кислота, формула, характеристики:
Муравьиная кислота (также – метановая кислота) – органическое вещество, относящееся к насыщенным одноосновным карбоновым кислотам.
Химическая формула муравьиной кислоты CH₂O₂. Рациональная формула муравьиной кислоты HCOOH. Изомеров не имеет.
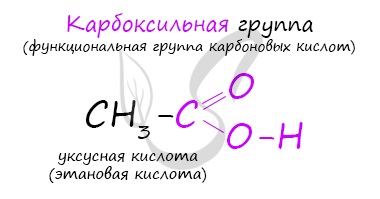
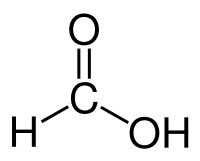
Строение молекулы муравьиной кислоты:
Муравьиная кислота (метановая кислота) – простейшая карбоновая кислота, родоначальник класса карбоновых кислот.
Муравьиная кислота – легковоспламеняющаяся жидкость с температурой вспышки 60 °С, температурой самовоспламенения 504 °С.
Водный раствор, содержащий 85% муравьиной кислоты, также является горючей жидкостью с температурой вспышки (в открытом тигле) 71 °С, температурой воспламенения 83 °С.
При температуре выше 69°C муравьиная кислота может образовывать взрывоопасныe смеси пар/воздух.
В качестве пищевой добавки муравьиная кислота зарегистрирована как E236.
Муравьиная кислота своё название получила из-за того, что была впервые выделена в 1670 году английским натуралистом Джоном Рэйем из рыжих лесных муравьёв.
В природе муравьиная кислота содержится в яде пчел, в крапиве, хвое, выделениях медуз, фруктах (яблоках, малине, клубнике, авокадо и пр.).
Соли и анионы муравьиной кислоты называются формиатами.
Название муравьиной кислоты на английском – formic acid.
Муравьиная кислота обладает токсическим действием, опасна для жизни и здоровья (опасность зависит от концентрации), обладает разъедающими свойствами.
Физические свойства муравьиной кислоты:
Химические свойства муравьиной кислоты:
Муравьиная кислота, кроме кислотных свойств, проявляет также некоторые свойства альдегидов, в частности, восстановительные.
Для нее характерны следующие химические реакции:
HCOOH + NaOH → HCOONa + H2O,
HCOOH + KOH → HCOOK + H2O.
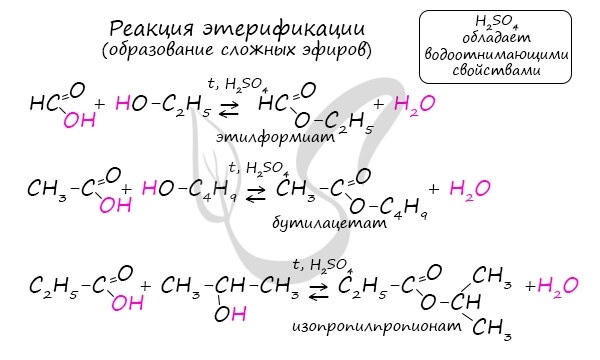
Муравьиная кислота, вступая в реакцию со спиртами, образует сложные эфиры.
Получение муравьиной кислоты:
Муравьиную кислоту получают:
– окислением метанола (СН3ОН);
– как побочный продукт при окислении бутана в производстве уксусной кислоты;
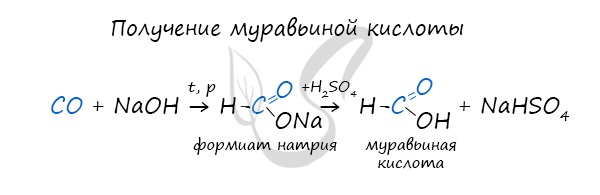
– реакцией монооксида углерода с гидроксидом натрия (основной промышленный способ) в две стадии.
NaOH + CO → HCOONa → HCOOH
На первой стадии получают формиат натрия, затем его обрабатывают серной кислотой;
– разложением глицериновых эфиров щавелевой кислоты.
Безопасность при обращении с муравьиной кислотой. Требования ГОСТа:
Муравьиная кислота относится к веществам 2-го класса опасности (ГОСТ 12.1.007-76). Предельно допустимая концентрация ее в воздухе рабочей зоны производственных помещений (ПДК) составляет 1 мг/м 3 (см. ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия (с Изменениями N 1, 2, 3)).
При превышении предельно допустимой концентрации пары муравьиной кислоты действуют раздражающе на слизистую оболочку верхних дыхательных путей и глаз; муравьиная кислота вызывает также ожог кожи.
Все помещения, в которых проводятся работы с муравьиной кислотой, должны быть оборудованы общей приточно-вытяжной механической вентиляцией. Анализ муравьиной кислотой следует проводить в вытяжном шкафу лаборатории.
При работе с ней следует применять индивидуальные средства защиты. Не допускать попадания препарата внутрь организма. Первая помощь при ожогах – обильное промывание водой.
Применение муравьиной кислоты:
Муравьиная кислота применяется:
– в сельском хозяйстве, как консервант сена и силоса,
– в химической промышленности в качестве растворителя,
– в текстильной промышленности для окрашивания шерсти,
– в пчеловодстве как средство для борьбы с паразитами.
Муравьиная кислота, получение, свойства, химические реакции
Муравьиная кислота (также – метановая кислота) – органическое вещество, относящееся к насыщенным одноосновным карбоновым кислотам.
Муравьиная кислота, формула, характеристики:
Муравьиная кислота (также – метановая кислота) – органическое вещество, относящееся к насыщенным одноосновным карбоновым кислотам.
Химическая формула муравьиной кислоты CH₂O₂. Рациональная формула муравьиной кислоты HCOOH. Изомеров не имеет.
Строение молекулы муравьиной кислоты:
Муравьиная кислота (метановая кислота) – простейшая карбоновая кислота, родоначальник класса карбоновых кислот.
Муравьиная кислота – бесцветная жидкость, обладающая резко пахнущим запахом.
Муравьиная кислота – легковоспламеняющаяся жидкость с температурой вспышки 60 °С, температурой самовоспламенения 504 °С.
Водный раствор, содержащий 85% муравьиной кислоты, также является горючей жидкостью с температурой вспышки (в открытом тигле) 71 °С, температурой воспламенения 83 °С.
При температуре выше 69°C муравьиная кислота может образовывать взрывоопасныe смеси пар/воздух.
Растворима в ацетоне, бензоле, глицерине, толуоле. Смешивается с водой, диэтиловым эфиром, этанолом.
В качестве пищевой добавки муравьиная кислота зарегистрирована как E236.
Муравьиная кислота своё название получила из-за того, что была впервые выделена в 1670 году английским натуралистом Джоном Рэйем из рыжих лесных муравьёв.
В природе муравьиная кислота содержится яде пчел, в крапиве, хвое, выделениях медуз, фруктах (яблоках, малине, клубнике, авокадо и пр.).
Соли и анионы муравьиной кислоты называются формиатами.
Муравьиная кислота обладает токсическим действием, опасна для жизни и здоровья (опасность зависит от концентрации), обладает разъедающими свойствами.
Физические свойства муравьиной кислоты:
Химические свойства муравьиной кислоты:
Муравьиная кислота, кроме кислотных свойств, проявляет также некоторые свойства альдегидов, в частности, восстановительные.
Для нее характерны следующие химические реакции:
HCOOH + NaOH → HCOONa + H2O,
HCOOH + KOH → HCOOK + H2O.
HCOOH + 2Cu(OH)2 → CO2 + Cu2O + 3H2O.
HCOOH → CO + H2O (to, kat = H2SO4 (конц.) или P4O10).
Муравьиная кислота, вступая в реакцию со спиртами, образует сложные эфиры.
HCOOH + СН3ОН→ HCOOCH3 + H2O.
HCOOH + 2[AgNH3)2]ОН→ 2Ag + (NH4)2CO3 + 2NH3 + H2O.
Поскольку муравьиная кислота проявляет свойства альдегидов, то для нее характерна реакция «серебряного зеркала». Реакция «серебряного зеркала» является качественной реакцией на альдегиды. В результате реакции образуется металлическое серебро. Если реакция проводится в сосуде с чистыми и гладкими стенками, то серебро осаждается на них в виде тонкой плёнки, образуя зеркальную поверхность. При наличии малейших загрязнений серебро выделяется в виде серого рыхлого осадка.
Получение муравьиной кислоты:
Муравьиную кислоту получают:
NaOH + CO → HCOONa → HCOOH
Безопасность при обращении с муравьиной кислотой:
Муравьиная кислота относится к веществам 2-го класса опасности (ГОСТ 12.1.007-76). Предельно допустимая концентрация ее в воздухе рабочей зоны производственных помещений (ПДК) составляет 1 мг/м 3 ( см. ГОСТ 5848-73 Реактивы. Кислота муравьиная. Технические условия (с Изменениями N 1, 2, 3)).
При превышении предельно допустимой концентрации пары муравьиной кислоты действуют раздражающе на слизистую оболочку верхних дыхательных путей и глаз; муравьиная кислота вызывает также ожог кожи.
Муравьиная кислота и ее растворы – легковоспламеняющиеся жидкости. Все работы с муравьиной кислотой следует проводить вдали от огня.
Все помещения, в которых проводятся работы с муравьиной кислотой, должны быть оборудованы общей приточно-вытяжной механической вентиляцией. Анализ муравьиной кислотой следует проводить в вытяжном шкафу лаборатории.
При работе с ней следует применять индивидуальные средства защиты. Не допускать попадания препарата внутрь организма. Первая помощь при ожогах – обильное промывание водой.
Применение муравьиной кислоты:
Муравьиная кислота применяется:
Муравьиная кислота
В 1670 г. английский ботаник и зоолог Джон Рей (1627—1705) провёл необычный эксперимент. Он поместил в сосуд рыжих лесных муравьёв, налил воды, нагрел её до кипения и пропустил через сосуд струю горячего пара. Такой процесс химики называют перегонкой с паром и широко используют для выделения и очистки многих органических соединений. После конденсации пара Рей получил водный раствор нового химического соединения. Оно проявляло типичные свойства кислот, поэтому и было названо муравьиной кислотой (современное наименование — метановая). Названия солей и эфиров метановой кислоты — формиатов — также связаны с муравьями (лат. formica — «муравей»).
Муравьиная кислота есть также в пчелином яде, сосновой хвое, гусеницах шелкопряда, в небольших количествах она найдена в различных фруктах, в органах, тканях, выделениях животных и человека. В XIX в. муравьиную кислоту (в виде натриевой соли) получили искусственно действием оксида углерода(II) на влажную щёлочь при повышенной температуре: NaOH + СО = HCOONa. И наоборот, под действием концентрированной серной кислоты муравьиная кислота распадается с выделением газа: НСООН = СО + Н2О. Эта реакция используется в лаборатории для получения чистого СО. При сильном нагревании натриевой соли муравьиной кислоты — формиата натрия — идёт совсем другая реакция: углеродные атомы двух молекул кислоты как бы сшиваются и образуется оксалат натрия — соль щавелевой кислоты: 2HCOONa = NaOOC—COONa + Н2.
Важное отличие муравьиной кислоты от других карбоновых кислот в том, что она, как двуликий Янус, обладает одновременно свойствами и кислоты, и альдегида: в её молекуле с одной «стороны» можно увидеть кислотную (карбоксильную) группу —СО—ОН, а с другой — тот же атом углерода, входящий в состав альдегидной группы Н—СО—. Поэтому муравьиная кислота восстанавливает серебро из его растворов — даёт реакцию «серебряного зеркала», которая характерна для альдегидов, но не свойственна кислотам. В случае муравьиной кислоты эта реакция, что тоже необычно, сопровождается выделением углекислого газа в результате окисления органической кислоты (муравьиной) до неорганической (угольной), которая неустойчива и распадается: НСООН + [O] = НО—СО—ОН = СО2 + Н2O.
Муравьиная кислота — самая простая и при этом сильная карбоновая кислота, она в десять раз сильнее уксусной. Когда немецкий химик Юстус Либих впервые получил безводную муравьиную кислоту, оказалось, что это очень опасное соединение. При попадании на кожу оно не только жжёт, но и буквально растворяет её, оставляя трудно заживающие раны. Как вспоминал сотрудник Либиха Карл Фогт (1817—1895), у него на всю жизнь остался шрам на руке — результат «эксперимента», проведённого совместно с Либихом. И неудивительно — впоследствии обнаружилось, что безводная муравьиная кислота растворяет даже капрон, нейлон и прочие полимеры, которые не берут разбавленные растворы других кислот и щелочей.
Неожиданное применение муравьиная кислота нашла при изготовлении так называемых тяжёлых жидкостей — водных растворов, в которых не тонут даже камни. Такие жидкости нужны геологам для разделения минералов по плотности. Растворяя металлический таллий в 90-процентном растворе муравьиной кислоты, получают формиат таллия НСООТl. Эта соль в твёрдом состоянии, может быть, и не рекордсмен по плотности, но её отличает исключительно высокая растворимость: в 100 г воды при комнатной температуре можно растворить 0,5 кг (!) формиата таллия. У насыщенного водного раствора плотность изменяется от 3,40 г/см 3 (при 20 о С) до 4,76 г/см 3 (при 90 о С). Еще большая плотность у раствора смеси формиата таллия и малоната таллия — соли малоновой кислоты CH2(COOTl)2.
Муравьиная кислота обладает сильными бактерицидными свойствами. Поэтому её водные растворы используют как пищевой консервант, а парами дезинфицируют тару для продовольственных товаров (в том числе винные бочки), уничтожают пчелиных клещей. Слабый водно-спиртовой раствор муравьиной кислоты (муравьиный спирт) применяют в медицине для растираний.
Карбоновые кислоты
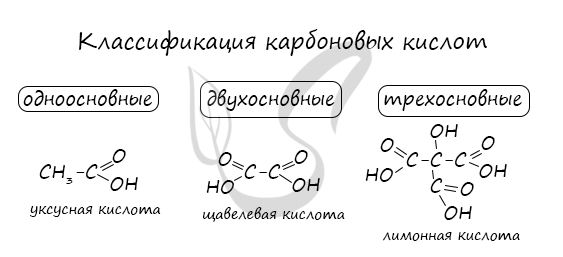
Классификация карбоновых кислот
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
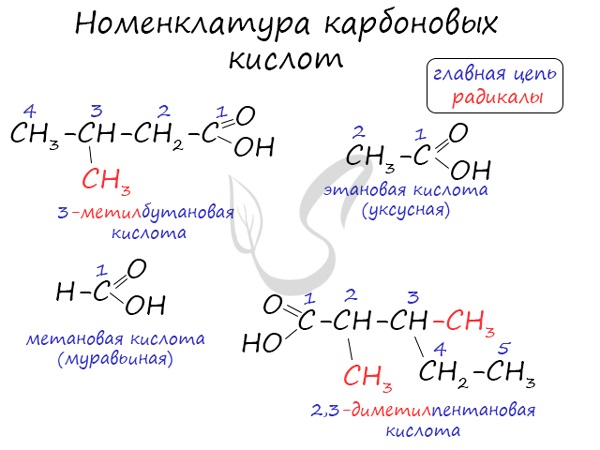
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
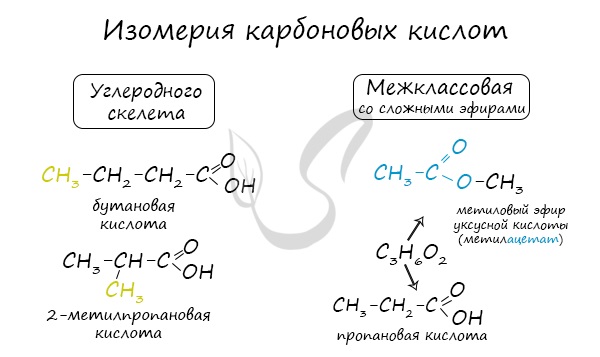
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
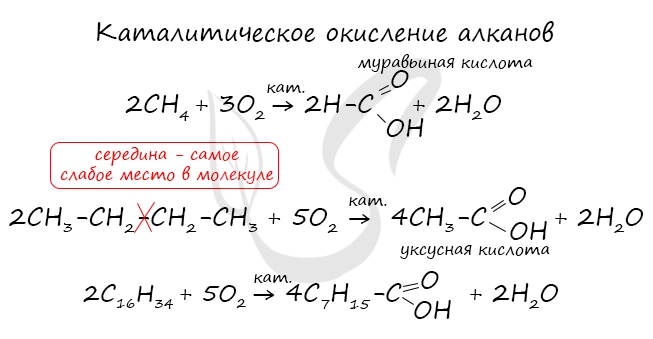
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
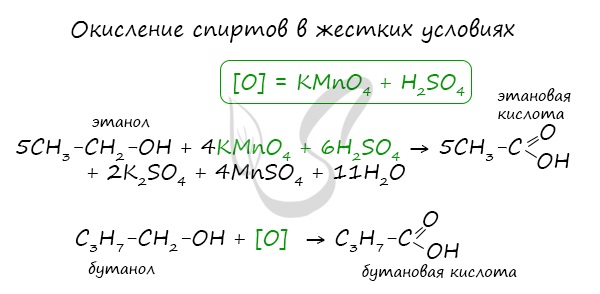
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
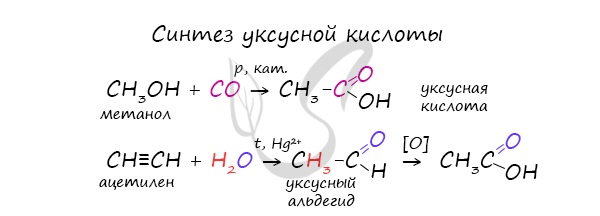
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
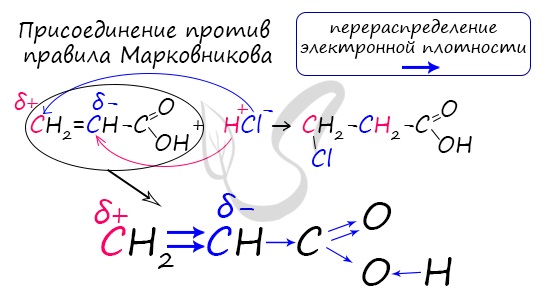
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
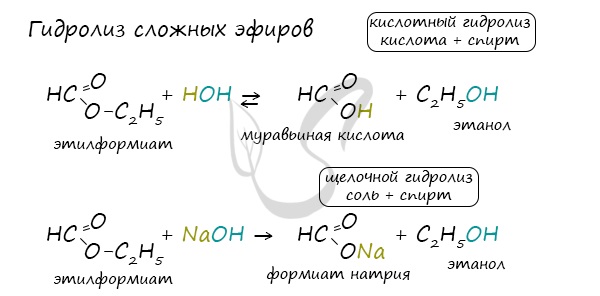
Сложные эфиры
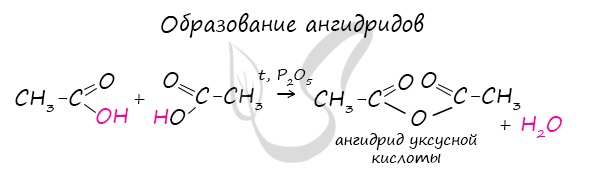
Ангидриды
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
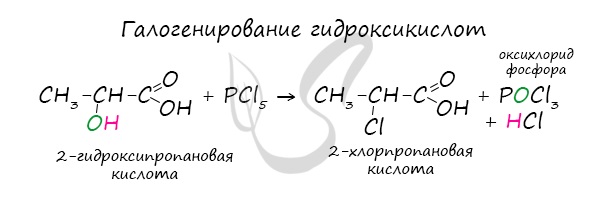
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Муравьиная кислота
Характеристики и физические свойства муравьиной кислоты
Смешивается с водой, диэтиловым эфиром, этанолом.
Рис. 1. Строение молекулы муравьиной кислоты.
Таблица 1. Физические свойства муравьиной кислоты.
Плотность (20 o С), г/см 3
Температура плавления, o С
Температура кипения, o С
Получение муравьиной кислоты
Основной способ получения муравьиной кислоты — окисление предельных метана (1), метилового спирта (2), формальдегида (метановый альдегид) (3):
CH4 + 3[O] → H-COOH + H2O (t = 150 – 200 o C, p = 30 – 60 atm) (1);
Химические свойства муравьиной кислоты
В водном растворе муравьиная кислота способна диссоциировать на ионы:
Муравьиная кислота обладает химическими свойствами, характерными для растворов неорганических кислот, т.е. взаимодействует с металлами (1), их оксидами (2), гидроксидами (3) и слабыми солями (4):
H-COOH + KOH → H-COOK + H2O (3);
При нагревании и в присутствии концентрированной серной кислоты муравьиная кислота взаимодействует со спиртами с образованием сложных эфиров:
Применение муравьиной кислоты
Муравьиная кислота широко применяется для получения сложных эфиров, используемых в парфюмерии, в кожевенном деле (дубление кож), текстильной промышленности (как протрава при крашении), в качестве растворителя и консерванта.
Примеры решения задач
| Задание | При каталитическом гидрировании 35 г метаналя образовалась муравьиная кислота. Рассчитайте какая масса кислоты была получена. |
| Решение | Запишем уравнение реакции каталитического окисления метаналя: |
Вычислим количество вещества метаналя (молярная масса равна 30 г/моль):
n(HCOH) = m(HCOH) / M(HCOH);
n(HCOH) = 35 / 30 = 1,2 моль.
Согласно уравнению реакции n(HCOH) : n(HCOOH) = 1:1, т.е.
n(HCOOH) = n(HCOH) = 1,2 моль.
Тогда масса муравьиной кислоты будет равна (молярная масса – 46 г/моль):
m(HCOOH) =1,2 × 46 = 55,2 г.
| Задание | Муравьиную кислоту массой 5,40 г поместили в сосуд объемом 4,50 л и нагрели до температуры 200 °С. Давление паров при этом составило 43,7 кПа. Определите число молекул димера муравьиной кислоты в газовой фазе. |
| Решение | В парах муравьиная кислота находится частично в виде димеров, а частично в виде отдельных молекул: |
Исходное количество муравьиной кислоты:
n(HCOOH) = m(HCOOH)/ M(HCOOH) = 5,4 / 60 = 0,09 моль.
Пусть в реакцию димеризации вступило х моль HCOOH, тогда образовалось х/2 моль димера (HCOOH)2и осталось (0,09 — х) моль HCOOH. Общее количество веществ в газовой фазе равно:
n = PV / (RT) = 43,7 × 4,50 / (8,31 × 473) = 0,05 = х/2 + (0,09 – х),
откуда х = 0,08 моль.
Число молекул димера муравьиной кислоты в газовой фазе равно: