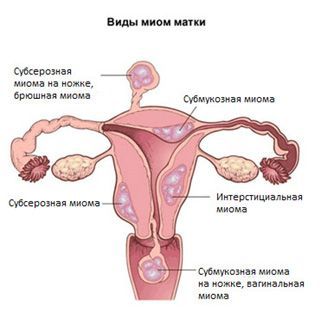
Миома матки в постменопаузе

Содержание женских половых гормонов, которые вырабатываются яичниками, становится настолько низким, что все пролиферативные процессы в норме в организме останавливаются. Менструальный цикл прекращается, а с ним, и циклические гормональные изменения. Постепенно уменьшаются размеры матки и яичников, эндометрий (слизистая оболочка) матки истончается и не растет.
Одновременно с процессами «угасания» яичников уменьшаются и исчезают миоматозные узлы.
Факторами риска отсутствия уменьшения миомы матки в постменопаузе являются наличие кистом яичников и гиперплазия эндометрия.
Если миома матки не регрессирует в постменопаузу и первые 1-2 года постменопаузы, то дальнейшее ее существование сопровождается опасностью возникновения рака эндометрия, рака яичников и саркомы матки!
Основными клиническими проявления нерегрессирующей (неуменьшающейся) миомы матки являются следующие:
Онкологическую настороженность должны вызывать пациентки с миомой матки в постменопаузе в следующих случаях :

2. Женщины, вступающие в менопаузу:
Пациентки с миомой матки в постменопаузе, попадающие в группу риска, подлежат обязательному оперативному лечению (как правило, лапароскопическим доступом в объеме удаления матки) для профилактики развития онкологических заболеваний женской половой сферы.
Чем опасна миома матки?
Влияние миомы матки на беременность
Миома матки может появляться и у молодых женщин, планирующих рождение ребенка, и у женщин старшего возраста, нередко болезнь обнаруживается с наступлением менопаузы. Опасна ли миома матки — вопрос, возникающий непременно при обнаружении этого заболевания.
В некоторых случаях с миомой можно благополучно дожить до глубокой старости, но нередко опухоль способна достигать больших размеров, представляя серьезную опасность для женщины. Прогноз зависит от скорости роста опухоли; если миома стремительно увеличивается в размерах, отсутствие лечения может привести к серьезным осложнениям. Прежде всего риск развития осложнений зависит от вида миомы.
Чем опасна субмукозная миома?
Субмукозные узлы (подслизистые), растущие в полость матки — наиболее неблагоприятные среди миом. Они чаще диагностируются у пациенток 30-40 лет, с наступлением климакса практически не развиваются. Расположенные под слизистой, эти образования способны «рождаться», выходя через цервикальный канал во влагалище. При этом непрекращающееся кровотечение способно привести к развитию геморрагического шока. Также возможно ущемление ножки узла с последующим некрозом. Тяжелым осложнением является выворот матки, сопровождающийся некрозом и инфицированием; в подобной ситуации проводится удаление органа.
У большей части пациенток фертильного возраста субмукозная опухоль становится причиной бесплодия. Миоматозный узел, расположенный в устьях маточных труб, препятствует продвижению сперматозоидов, способность опухоли вырабатывать собственные гормоны становится причиной ановуляции, зачатие становится невозможным. Если же беременность все же наступает, то наличие миомы делает невозможным полноценную имплантацию, что приводит к отторжению плодного яйца. На поздних сроках вероятны преждевременные роды.
Чем опасна субсерозная миома матки?
Субсерозные, называемые также подбрюшинными, миомы чаще появляются у женщин до наступления менопаузы, при этом имеющиеся опухоли подвергаются инволюции. Узлы могут располагаться на тонкой ножке или на широком основании, при наличии ножки существует риск ее перекрута, ишемии, некроза, которые приведут к инфицированию, что чревато перитонитом, сепсисом и т.п. Следует учитывать, что даже небольшой по размеру узел может вызвать деформацию сосудов матки. В отличие от субмукозного вида, в этом случае проблемы с зачатием возникают, если миома привела к деформации матки. Однако субсерозная миома матки даже небольшого размера при беременности может стать причиной ее прерывания.
Размеры миомы — когда возникает опасность?
Миоматозный узел даже в несколько миллиметров оказывает влияние на организм, становясь причиной различных симптомов и осложнений, многие из которых опасны для здоровья. Однако в половине случаев какие-либо симптомы при миоме отсутствуют, и болезнь обнаруживается случайно.
Какие размеры миомы считаются опасными? При величине матки, соответствующей 12 неделям беременности, из-за сдавления нарушается функция тазовых органов: мочевого пузыря, мочеточников, что приводит к затруднению оттока мочи. При отсутствии лечения не исключено развитие, например, гидронефроза, почечной недостаточности. Также опухоль сдавливает кишечник, при больших размерах не исключено развитие непроходимости и некроза, при которых нужна срочная операция. Не менее опасным осложнением является сдавление крупных сосудов, когда тромбоз оканчивается летальным исходом.
Чем опасна множественная миома матки?
Наличие двух и более узлов — разных размеров, локализации или типа, увеличивает риск развития различных осложнений. Кровотечения разной интенсивности приводят к анемии, опухоли больших размеров сдавливают соседние органы, возможен перекрут ножки с развитием некроза и т.д. Невозможность зачатия связана с нарушением овуляции вследствие гормонального дисбаланса. Также препятствует зачатию нарушенная проходимость труб и цервикального канала, к тому же затруднена имплантация плодного яйца в полости матки. Если зачатие все же происходит, множественные узлы сделают невозможным нормальное протекание беременности. Вероятность ее прерывания, отслойка плаценты, кровотечения, преждевременные роды, послеродовые кровотечения — неполный перечень возможных рисков.
Чем опасна миома матки после климакса?
Следует учитывать, что миома с наступлением климакса не исчезает, возможно снижение активности клеток опухоли, ее уменьшение в размерах, но полного регресса не наблюдается никогда. Более того, при крупных размерах, наличии эндометриоза, при субмукозном расположении узлов существует риск развития кровотечения и гиперплазии эндометрия. Поэтому все пациентки, отказавшиеся от хирургического лечения, должны находиться под наблюдением специалиста.
Лечение миомы матки
Метод лечения для каждой пациентки я подбираю только индивидуально. В некоторых случаях возможно динамическое наблюдение, в других — эффективно только оперативное лечение. Какая тактика окажется наиболее эффективной, можно определить только после обследования. Показанием к операции являются:
«Золотым» стандартом при лечении миоматоза считается миомэктомия — органосохраняющая операция, в ходе которой узел «вылущивается», при этом повреждение миометрия исключено. В нашей клинике операция, как правило, проводится методом лапароскопии или резектоскопии.
Чтобы исключить риски, которые присутствуют во время оперативного вмешательства (кровотечение из ложа узла, ухудшение видимости зоны операции и риск иссечения миометрия или вскрытия маточной полости, ожог тканей с последующим формированием несостоятельного рубца) я провожу операцию по уникальной авторской методике, позволяющей избежать удаления матки даже при наличии больших или множественных миоматозных узлов.
Оригинальная авторская методика проведения бескровной миомэктомии
В ходе операции сосуды, питающие матку, временно пережимаются, таким образом, из-за отсутствия кровотока зона вмешательства остается сухой, что позволяет визуализировать границы узла и тела матки, качественно сопоставить и надежно сшить слои миометрия; в дальнейшем здесь образуется полноценный рубец. В заключение операции, длительность которой не превышает одного часа, кровоток восстанавливается.
Наша клиника оснащена современным качественным оборудованием, например, использование во время операции аппарата электротермического лигирования тканей «LigaSure» дает возможность одновременного рассечения и запаивания тканей, что исключает риск кровотечения. Для минимального травмирования здоровых тканей и лучшего заживления используются ультразвуковые ножницы. В сложных случаях мы используем шовную систему V-lock, позволяющую более тщательно сопоставить края раны, что обеспечивает лучшее заживление, при этом шов формируется в 3-4 раза быстрее. Для профилактики появления спаек в ходе вмешательства активно используются противоспаечные субстанции, что сводит к минимуму вероятность сращений.
Я всегда стремлюсь провести органосохраняющую операцию — и у женщин репродуктивного возраста, и у пациенток, желающих сохранить матку, как орган. При наличии у женщины сопутствующих заболеваний органов таза или брюшной полости, требующих оперативного лечения, существует возможность проведения симультанных операций.
Органосохраняющие операции по моей методике в нашей клинике проводятся на протяжении более чем 12-и лет. Лично мною было проведено более 4 тысяч хирургических вмешательств по удалению миом. Сегодня авторская методика, на которую получен патент, активно используется также в ведущих клиниках Европы и Америки.
Миома матки
Миома матки — доброкачественное узловое образование в миометрии (мышечной стенке матки).
Опухоль относится к самым распространённым гинекологическим заболеваниям и наиболее часто встречается у женщин позднего репродуктивного возраста, перед климаксом. Частота заболевания составляет примерно 25% от всех патологий по гинекологическому профилю.
Причины
Специалисты по всему миру не могут со 100% точностью назвать причину возникновения патологии. Повлиять на рост новообразования может повреждение ткани яичников. Это ухудшает их основную функцию, что приводит к усиленной выработке женских половых гормонов. В ходе исследований было доказано, что эстрогены способствуют росту новообразования. Как только женщины прекращали прием оральных контрацептивов, рост миомы прекращался, а в дальнейшем она полностью рассасывалась. Но и это не является точной причиной, так как миома матки может развиваться при отсутствии эндокринных нарушений. Среди остальных причин эксперты выделяют:
Симптомы заболевания
Симптомы миомы матки разнообразны и зависят от локализации миоматозных узлов, величины и индивидуальных особенностей организма. Самые характерные проявления таковы:
Неспецифические симптомы, сопутствующие в отдельных случаях миоме матки, — бесплодие, неспособность выносить ребёнка. Они не всегда являются признаками опухоли, но часто — её следствием при выраженном увеличении узлов.
Миома матки: диагностика
В первую очередь, необходимо, конечно, обратиться к врачу-гинекологу для осмотра. Самое простое и информативное (до 95 % точности) исследование на предмет наличия/отсутствия опухоли — УЗИ. В ходе исследования миома проявляет себя округлыми очагами с пониженной эхогенностью. Точное расположение узлов можно получить с помощью 3D-исследования.
Чтобы дифференцировать миоматозные узлы и опухоли яичника, при необходимости назначают МРТ. Для диагностики малых субмукозных узлов применяют гистероскопию — малоинвазивное эндоскопическое исследование полости матки гистероскопом.
Миома матки
Миома матки – доброкачественная опухоль матки, довольно часто встречающееся заболеванием. Диагностируется заболевание у 20% тридцатилетних женщин. Длительное время миому было принято считать опухолью доброкачественного характера, которая может стать злокачественной исключительно при определенных условиях. Единственным методом лечения при диагностировании миомы до недавнего времени считалось удаление опухоли вместе органом, то есть с маткой. Сегодня специалисты рассматривают миому как реакцию организма на причиненные матке повреждения. Факторами болезни являются:
Формируется миома из соединительной или мышечной ткани. Размер ее может составлять от пары миллиметров до 1-8 сантиметров. Локализоваться опухоль может на шейке матки или на теле. При обследовании нередко выявляется несколько узлов разной величины.
Возникает миома по причине активного деления клеток матки, которое стимулируют эстрогены. Одной из особенностей данного заболевания является то, что выявление в результате анализа крови нормального баланса содержания прогестерона и эстрогенов не является гарантией того, что миома отсутствует. Для того чтобы быть уверенным в отсутствии данного заболевания, требуется серьезное обследование с использованием современных методов диагностики. Диагностика позволяет также выявить место расположения образования: в полости матки, в брюшной полости, в стенке матки.
Миома практически никогда не диагностируется у девушек до 25 лет и у женщин после 50 лет. Наибольшей опасности подвергаются женщины после 25 и до 50. Особенно высока вероятность развития миомы в периоды общего снижения иммунитета, во время воспалений половой сферы, во время беременности. В последние годы диагноз «миома матки» нередко ставят девушкам 17-18 лет.
Симптомы миомы матки
О том, что у женщины развивается миома матки, она может и не подозревать, поскольку внешние признаки могут и не проявляться. Нередко случается так, что осмотр пациентки гинеколог проводит по совершенно другим причинам (например, профосмотр) и во время обследования выявляет новообразование. Симптомы проявляются активно в случаях, когда матка вырастает до больших размеров, но если опухоль небольшая, симптомов может и не быть.
Миома матки схожа симптоматикой со многими болезнями репродуктивных органов. Среди наиболее частых симптомов, по которым можно определить образование и развитие миомы, являются:
Своевременное обращение к специалисту позволяет выявить проблему на ранних стадиях, избежав таким образом необходимости в оперативном вмешательстве.
Причины возникновения миомы
Основная причина – гормональные сбои по причине увеличения концентрации эстрогенов. Во время менопаузы концентрация эстрогена понижается, и миома может самостоятельно исчезнуть, без какого-либо лечения. Но рассчитывать на такой результат специалисты не рекомендуют, советуя женщинам при появлении первых симптомов как можно скорее обращаться к врачу.
Спровоцировать появление болезни может целый ряд факторов:
Некоторые факторы, являющиеся причиной появления миозных новообразований, заслуживают более пристального внимания.
В группу риска входят женщины до 35 лет, у которых диагностирована гипертония или наличествуют проблемы ожирением (обмен веществ). Также причиной могут стать воспаление, принявшее форму хронического, травмы и применение контрацептивов орально.
Вероятность развития заболевания зависит в немалой степени от того, сколько и как часто женщина рожала, продолжительности и наличия грудного вскармливания, сколько было доношенных и сколько было прерванных беременностей. У рожавшей хоть единожды женщины вероятность развития миомы значительно меньше, чем у нерожавшей.
Неправильное питание или несбалансированный рацион. Недостаточное количество волокон в пище, высокий процент жирных кислот и избыточная калорийность продуктов питания значительно повышают шансы на возникновение новообразования. Если в организме процент жира значительно превышает норму, гормональный баланс может сместиться и числа эстрогенов увеличится, что, в свою очередь, повышает риск образования опухолей.
Диагностика миомы матки
Самый простой и надежный способ своевременно выявить миому – ежегодно посещать осмотры врача-гинеколога. Установлено наличие развивающейся миомы может быть во время влагалищного гинекологического исследования – матка определяется как бугристая, плотная, увеличенная. При обнаружении заболевания для подтверждения диагноза может быть проведено диагностическое выскабливание, после чего соскоб исследуют гистологическими методами. Диагностирование опухоли возможно также с применением следующих методов:
В некоторых случаях специалист, при наличии некоторых симптомов, но при отсутствии узлов миомы, рекомендует пациентке пройти УЗИ через 6 месяцев.
Какой врач лечит миому матки
При проявлении определенных симптомов, указывающих на наличие новообразования (тянущие боли внизу живота, нестабильные месячные, длительные кровотечения и пр.), женщины задумываются о том, к какому специалисту им следует обратиться. Лечением миомы занимаются гинекологи и гинекологи-хирурги. Гинекологи проводят первичный осмотр, дают назначения на диагностику и по результатам диагностирования определяют способ (метод) наиболее эффективный для восстановления здоровья женщины. В случае если по результатам анализов, показана операция, ее проводят гинекологи-хирурги.
Клиника АО «Медицина» в Москве оказывает услуги диагностики и лечения миомы матки. К услугам пациенток высококвалифицированные специалисты, владеющие самыми современными методиками лечения и эффективно использующие традиционные методики. Клиника оснащена современным оборудованием диагностическим и лечебным, что позволяет специалистам медицинского заведения успешно излечивать самые сложные случаи.
Для того чтобы удостовериться в высокой квалификации специалистов в области гинекологии, работающих в клинике АО «Медицина», достаточно посетить раздел «Наши врачи» на официальном сайте клиники.
Методы лечения миомы матки
При выборе метода гинеколог учитывает множество факторов, основными из которых являются:
возраст пациентки (если пациентка вышла из детородного возраста, специалист может порекомендовать медикаментозное лечение);
Пациентки с диагнозом «миома матки» в обязательном порядке наблюдаются у гинеколога, в большинстве случаев частота визитов составляет раз в три месяца.
В зависимости от состояния опухоли и других факторов гинеколог выбирает один из двух способов лечения:
Лечение миомы без хирургии
Консервативное или терапевтическое лечение может быть назначено специалистом, если:
Консервативное лечение заболевания предусматривает применение лекарственных препаратов. В перечне базовых мероприятий, проведение которых позволяет устранить миому без операции, действия, направленные на достижение следующих целей:
Нормализация обмена веществ путем коррекции диеты пациентки.
Нормализация менструального цикла для того, чтобы исключить вероятность длительных кровотечений.
Предотвращение проявления симптомов анемии.
Восстановление иммунитета в целях повышения защитных свойств организма.
Восстановление микрофлоры половых органов и лечение диагностированных заболеваний.
Консервативное лечение применяется в случаях, если диагностирована миома небольших размеров при отсутствии четко выраженных симптомов. Наиболее распространенным способом лечения является назначение гормональных препаратов. Данные препараты представляют собой производные прогестерона и действуют следующим образом: одновременно нормализуют функцию яичников и препятствуют дальнейшему развитию новообразования. Препараты вводятся путем инъекций раз в месяц на протяжении 6 месяцев. Прием препаратов позволяет уменьшить размеры матки на 55% и более.
Данная методика используется в большинстве случаев при диагностировании миомы у женщин старшего возраста, поскольку о молодых женщин вероятно развитие остеопороза. Недостаток методики в том, что консервативные методы могут только затормозить развитие болезни, но не устранить ее полностью. При лечении таким способом женщин старшего возраста высока вероятность того, что при наступлении менопаузы миома рассосется самостоятельно.
Ультразвуковой метод
Методика ФУЗ-абляции относится к прогрессивным методам лечения. Основой методики является коагуляция узлов миомы путем направленных импульсов ультразвука фокусированного. Контролируется процесс с помощью МРТ. Данная процедура имеет множество преимуществ по сравнению с удалением миомы путем операции, но эффективна она только при наличии определенных характеристик, поэтому решение о применении ФУЗ-абляции принимается исключительно в индивидуальном порядке после тщательного обследования.
Применение метода ФУЗ-абляции имеет множество преимуществ:
Операбельное лечение миомы матки
Проведение операций при постановке диагноза «миома матки» возможно в тех случаях, когда все другие способы лечения неэффективны. Наиболее щадящим вариантом операбельного лечения является проведение лапароскопии, щадящей для организма и позволяющей полностью сохранить репродуктивную функцию. Среди преимуществ данной методики:
Метод эмболизации маточных артерий (ЭМА)
ЭМА начали применять сравнительно недавно. Методика заключается в том, что питание миоматозного узла прекращается, поскольку останавливается кровоток по артериям. После того, как хирург обнаруживает сосуд, в него вводится препарат, останавливающий кровоток. После прекращения кровоснабжения узлы миомы полностью исчезают или значительно уменьшаются в размерах. Одним из преимуществ операции является полное исчезновение симптомов. Кроме того, после проведения операции полностью отсутствует риск рецидива.
Хирургия миомы
Хирургия показана, если:
В зависимости от результатов обследования, возраста пациентки и других факторов гинеколог может назначить:
Молодым нерожавшим женщинам назначается консервативное хирургическое лечение.
Миомэктомия, представляющая собой процедуры, направленные на вылущивание миозных узлов, позволяет сохранить репродуктивную функцию:
Если пациентка не намерена рожать, а результаты обследования указывают на полное удаление органа, гинекологи используют одну из методик радикальной хирургии:
Показания к операционному лечению миомы матки
Хирургическое вмешательство является единственным способом излечения при следующих факторах:
Способ миэктомии определяется хирургом в зависимости от локализации новообразования, тяжести заболевания, типа миомы, индивидуальных особенностей пациентки.
Противопоказания при диагностировании миомы матки
Существует несколько противопоказаний, в частности, категорический запрет на посещение саун, бань, пляжа – то есть, любого места, где вероятен перегрев.
При выборе метода лечения противопоказаны следующие способы:
Стоимость обследования, диагностики и лечения миомы матки
Клиника АО «Медицина» предлагает услуги первичного обследования, диагностики и лечения по ценам, ознакомиться с которыми можно в таблице ниже или в соответствующем разделе сайта клиники.
Общая стоимость лечения определяется после первичного обследования и выбора наиболее эффективного курса лечения. Специалисты АО «Медицина» (клиника академика Ройтберга) в Москве используют наиболее эффективные методики, современное высокоточное диагностическое оборудование, безопасные материалы и эффективные препараты.
Преимущества лечения миомы в клинике АО «Медицина»
АО «Медицина» (клиника академика Ройтберга) в Москве предлагает услуги специалистов высокой квалификации, имеющих богатый опыт в области лечения миомы матки и располагающих современным оборудованием. Весомыми факторами в пользу выбора клиники АО «Медицина» для лечения миомы матки являются:
Обратившись в клинику АО «Медицина» в Москве, вы гарантированно получите высокопрофессиональную медицинскую помощь и первоклассное обслуживание.
Неоперативные методы лечения миомы матки
Лейомиома матки — одно из самых распространенных заболеваний у женщин, однако, несмотря на успехи в диагностике миомы матки, до настоящего времени не существует «золотого» стандарта лечения, что обусловлено как нерешенными проблемами патогенеза миомы матк
Лейомиома матки — одно из самых распространенных заболеваний у женщин, однако, несмотря на успехи в диагностике миомы матки, до настоящего времени не существует «золотого» стандарта лечения, что обусловлено как нерешенными проблемами патогенеза миомы матки, так и традиционно сложившимися представлениями «о бесполезности» матки при реализованной репродуктивной функции. Поэтому наиболее распространенным методом лечения миомы матки остается гистерэктомия. Подобный радикализм у большинства больных не обоснован, поскольку практически отсутствует риск озлокачествления и отмечается прогресс в появлении методов, тормозящих рост опухоли и вызывающих регресс симптомов заболевания [1, 4] Использование малоинвазивных и неинвазивных методов лечения на ранних этапах развития миомы матки позволяет остановить развитие заболевания, привести к его регрессу и не допустить в дальнейшем нарушения репродуктивной функции [2, 3].
Эпидемиология. Факторы риска
Частота возникновения миомы матки составляет 15–17% у женщин старше 30 лет и 30–35% у женщин, достигших пременопаузального возраста [1, 5]. Однако в последние годы наблюдается тенденция к «омоложению» миомы матки — возникновение ее у женщин до 30 лет, что обусловлено как совершенствованием диагностики, так и широким распространением «агрессивных» акушерских и гинекологических вмешательств. Частое сочетание миомы матки с доброкачественными заболеваниями эндометрия, эндометриозом осложняет течение заболевания и затрудняет тактику лечения.
Средний возраст выявления миомы матки составляет 32,8 ± 0,47 года, а показания к активному хирургическому лечению появляются примерно к 45 годам. Установлено, что развитие этой опухоли занимает в среднем 5 лет и в 84% случаев узлы являются множественными [1, 5,].
Эпидемиологические исследования выявили ряд факторов риска развития этой опухоли — этнические, генетические, паритет, вредные привычки, питание [1, 7]. У афро-американских женщин встречаемость миомы матки самая высокая, причем возникают в более молодом возрасте, достигают больших размеров и частота анемий выше, особенно по сравнению с кавказскими и азиатскими женщинами. Объяснением служит повышенный уровень циркулирующих эстрогенов по сравнению с женщинами другой расы.
Исследования близнецов и семей выявили генетический фактор риска [1]. Так, вероятность развития этой опухоли значительно выше и возникает в более молодом возрасте у женщин, матери и/или сестры которых страдали этим заболеванием. Недавно был определен фактор наследственности, как предполагают, играющий роль в этиологии опухоли матки. Хотя 50–60% миом матки являются кариотипически нормальными, однако часто встречаются аберрации, которые затрагивают хромосомы 6, 7, 12 и 14 (Gross K. L., 2001). Перестройки в этих хромосомах последовательно влияют на две недавно обнаруженные группы генов белка — HMGIC и HMGIY. Они кодируют те белки, которые, вероятно, играют роль в транскрипции и могут играть свою роль в аномальном росте миом. Однако, несмотря на доказательство наследования, не выявлено, какие именно генные мутации могут привести к развитию данного заболевания, а следовательно, не существует и превентивных мер.
Отсутствие детей и раннее наступление менархе повышает в 2–3 раза риск развития миомы. Причем степень уменьшения риска тем выше, чем больше детей в семье, — так у женщин с тремя доношенными беременностями риск снижается на 50–90%, хотя не выявлено никакой корреляции между возрастом при первых родах и миомами, а также для женщин 45 лет и старше защитный эффект parity не столь очевиден [7]. Объяснить это можно либо более высокой степенью риска вследствие более длительного периода с момента последних родов, либо более длительного периода воздействия стероидных гормонов в целом. Противоречивы данные о действии оральных контрацептивов. Однако в большинстве работ доказано, что применение оральных контрацептивов не повышает риск развития миомы матки. Так же как и нет никаких доказательств увеличения роста и количества миоматозных узлов на фоне приема заместительной гормональной терапии (ЗГТ) (Luoto R., 2002).
Избыточный вес, особенно в сочетании с низкой физической активностью на фоне хронического стресса, повышает риск миомы матки в 2–3 раза, причем прибавка веса после 18 лет влияет более значительно, чем ожирение в детском и пубертатном возрасте. Это объясняется повышенной периферической конверсией в жировых клетках андрогенов в эстрогены под воздействием ароматазы и более высокой биодоступностью факторов роста, типа инсулиноподобного фактора роста-1 (ИПФР-1).
Не выявлено корреляций с курением, хотя теоретически курение могло бы снижать риск миомы матки, поскольку напоминает состояние, характерное для относительного дефицита эстрогена, т. е. с характерными признаками остеопороза, ранней менопаузой и более низкими показателями рака эндометрия [5]. Однако данные, которыми мы располагаем сегодня, достаточно противоречивы, и только некоторые исследователи отмечают среди курильщиц уменьшение риска на 30–50% [1, 16].
Аналогии между опухолями гладкой мускулатуры и атеросклеротическими бляшками и, следовательно, возможную корреляцию между атерогенными факторами и риском миомы матки изучали Faerstein et al. Исследователи зафиксировали увеличение риска миом в 2,1 раза у пациенток до 35 лет с артериальной гипертензией, принимающих гипотензивную терапию дольше пяти лет и при длительности заболевания не менее пяти лет.
Таким образом, дальнейшие исследования, особенно посвященные цитогенетическим и молекулярным аспектам миом, приведут нас к определению тех генетических локусов, которые играют важную роль в индуцировании данных опухолей.
Патоморфология. Патогенез
Лейомиома матки представляет собой доброкачественную опухоль моноклонального происхождения, развивающуюся из гладкомышечных клеток и содержащую различное количество волокнистой соединительной ткани. Большинство ученых считают, что миома матки соответствует критериям истинной опухоли, о чем свидетельствуют: моноклональный характер развития миомы (как и большинство опухолей, в том числе и злокачественных), большие размеры и автономный рост опухоли, обусловленный воздействием факторов роста и цитокинов, активизация процесса неоангиогенеза, генетическая нестабильность (до 40% миом имеют генетические нарушения), т. е. вследствие мутаций уменьшается точность воспроизведения генетического аппарата, нарушается механизм репарации ДНК, изменяется регуляция клеточного цикла в поврежденных клетках, что приводит к неуклонной опухолевой прогрессии [1, 4, 25].
По мнению большинства ученых, миомы возникают в результате множественных соматических мутаций в нормальных клетках миометрия, что ведет к постепенному снижению регуляции их роста. Опухоль растет из клетки-прародительницы, в которой произошла первоначальная мутация и является следствием нарушения тканевого гомеостаза, поддерживаемого балансом клеточной пролиферации и апоптоза. В последнее десятилетие установлено, что образование и рост опухоли связаны с изменениями сложных взаимодействий между стероидными гормонами и их рецепторами, местными факторами роста и состоянием внеклеточного матрикса [20, 25, 12].
В настоящее время наибольшее подтверждение находит теория Fujii S., согласно которой развитие гладкомышечных клеток мезодермального происхождения происходит на эмбриональном этапе длительно: от 14 до 30 недель внутриутробного периода развития. Поэтому эти еще недифференцированные клетки за счет длительного периода внутриутробного развития могут подвергаться воздействию многочисленных факторов из организма матери (тропных гормонов, половых стероидов, факторов роста) и окружающей среды. Эти клетки-предшественники (уже с соматическими мутациями) сохраняются в миометрии и начинают расти после менархе. Их рост продолжается в течение многих лет на фоне выраженной активности яичников под действием как эстрогенов, так и прогестерона [12, 20, 27].
Также возможен и другой путь образования клеток-предшественников, при котором неопластическая трансформация миометрия может происходить в результате соматических мутаций нормального миометрия под влиянием половых стероидов и факторов роста. Однако молекулярные изменения, инициирующие эту трансформацию, до конца неизвестны.
Этиология и патофизиология остаются малопонятными, хотя к настоящему времени и определены основные молекулярно-генетические детерминанты возникновения этого заболевания. К ним относятся цитогенетические нарушения, изменения половых стероидов и гормональной чувствительности тканей, нарушение процесса ангиогенеза. В ткани миоматозных узлов в 40–50% имеются опухоль-специфические дефекты хромосом, определяемые кариотипически, что подтверждает роль генетических механизмов в росте и развитии миомы матки. Согласно современным представлениям, рост миомы происходит главным образом за счет пролиферации, стимулированной половыми стероидами через факторы роста по аутокринно-паракринному механизму, при относительно низкой готовности опухолевых клеток к апоптозу.
Несомненно, миома матки является гормонозависимой опухолью. До настоящего времени не известны механизмы, запускающие рост опухоли, но несомненна центральная роль половых стероидов — эстрогенов, прогестерона и их рецепторов в моделировании роста, дифференцировки и функции миометрия. Известно, что ключевую роль в контроле роста и развития миоматозных узлов играют эстрогены. Подтверждением этому служит повышенный уровень экспрессии эстрогеновых рецепторов в ткани узлов, по сравнению с неизмененным миометрием [8], а также стимулирующий эффект эстрогенов на синтез ДНК и клеточную пролиферацию в тканях матки. Также имеются данные о повышении уровня антигена клеточной пролиферации Ki-67 в нормальном миометрии [11] и усиление роста миомы матки преимущественно в лютеиновую фазу [20], что подтверждает роль прогестерона в индуцировании митогенного эффекта факторов роста. Очевидно, влияние эстрогенов и прогестерона комплементарны, т. е. эстроген создает условия для стимуляции пролиферации прогестероном [13]. Это подтверждается и работами, в которых прогестерон вызывает увеличение экспресии PCNA и эпидермального фактора роста в клетках миомы, тогда как эстрадиол в тех же клетках увеличивает экспрессии PCNA и ЭФР-рецептора [25, 11]. Следовательно, сочетанное действие эстрадиола и прогестерона стимулирует пролиферативный потенциал клеток миомы.
Другим потенциальным механизмом образования миомы матки является торможение механизмов апоптоза [12, 17]. В многочисленных работах доказано влияние половых стероидов не только на пролиферативные процессы, но и на регуляцию апоптоза в миометрии. Установлено, что протеин Bcl-2, тормозящий апоптоз, значительно меньше экспрессируется при лейомиоме по сравнению с нормальным миометрием. Причем эстрадиол, подавляя экспрессию этого протеина, снижает апоптоз.
Таким образом, развитие пролиферативных процессов, к которым относится и лейомиома матки, обусловлено не только повышенной пролиферацией клеток, но, возможно, и ослаблением индукции апоптоза.
В реализации влияния половых стероидов участвуют местные ауто- и паракринные факторы (факторы роста, цитокины и др.), продукция которых находится под контролем эстрогенов и прогестерона. Митогенное действие эстрогенов опосредовано местными регулирующими ростовыми факторами. Результатом их избыточной продукции является ускорение клеточной пролиферации, гипертрофия клеток, увеличение объема межклеточного матрикса, и нередко отмечается сочетание этих явлении [8]. Наиболее значимыми факторами роста для миомы являются трансформирующий фактор роста-бета (ТФР-бета), стимулирующее влияние на продукцию которого оказывает также и прогестерон. Эстрогены действуют и на межклеточный матрикс, оказывая непосредственное стимулирующее влияние на коллаген типа I и III и протеин коннексин-43 щелевидных межклеточных контактов [14].
Таким образом, стероидные гормоны могут оказывать стимулирующее влияние на пролиферацию опухолевой ткани путем воздействия и на местные факторы роста, продуцируемые гладкомышечными клетками и фибробластами [14, 25]. Влияние медиаторов различных факторов клеточного роста, также как и половых стероидов, осуществляется через клеточные рецепторы, концентрация и чувствительность которых играют важную роль в регуляции опухолевого роста. Основными модуляторами клеточного роста, обладающими выраженными митогенными свойствами на миометрий и ткань миомы, являются ИПФР-1, эпидермальный фактор роста (ЭФР), ТФР-бета и группа ангиогенных факторов роста. В настоящее время ангиогенез рассматривается как ключевой фактор в развитии опухолевых процессов. Это касается и роли ангиогенеза в патогенезе миомы матки. Основными индукторами процесса ангиогенеза являются сосудистый эндотелиальный фактор роста (СЭФР-А), ангиогенин и основной фактор роста фибробластов (ФРФ-2).
Противоположным действием на ангиогенез и, следовательно, ограничивающим рост опухолевой ткани обладают ингибиторы ангиогенеза. Одним из основных является эндостатин, который является не только мощным ингибитором ангиогенеза, но и специфическим ингибитором пролиферации клеток эндотелия. СЭФР — является важнейшим фактором, определяющим процессы образования новых сосудов и повышенную сосудистую проницаемость. Гипоксия ткани внутри миоматозного узла стимулирует экспрессию СЭФР и, таким образом, вызывает отек узла, что обусловлено способностью СЭФР повышать проницаемость сосудов [38]. Экспрессия СЭФР в тканях матки и яичников может регулироваться гормональным путем — половыми стероидами. Следует отметить, что ТФР-бета и ФРФ могут являться и факторами, модулирующими рост сосудов; ФРФ являются потенциальными митогенами, в то время как ТФР-бета — выраженный ингибитор пролиферации клеток эндотелия. Полагают, что ФРФ стимулируют ангиогенез, непосредственно воздействуя на эндотелиальные клетки, в то время как ТФР-бета оказывает опосредованное непрямое влияние, стимулируя другие клеточные типы к выделению факторов, стимулирующих клетки эндотелия.
Процессы ангиогенеза в миомах неразрывно связаны с морфогенезом этих опухолей и в значительной степени определяют особенности возникновения, характер роста и клинико-морфологические варианты (простая и пролиферирующая миома матки), и, по мнению ряда авторов, методы лечения миомы матки в перспективе должны быть связаны с возможностью воздействия на процессы ангиогенеза [6, 14].
Следовательно, половые стероиды осуществляют регуляцию роста миомы посредством комплекса факторов, регулирующих пролиферацию, апоптоз и ангиогенез в опухолевой ткани.
Таким образом, многочисленные исследования, посвященные патогенезу данного заболевания, выявили ряд факторов роста и рецепторов, влияющих на пролиферацию гладкомышечных клеток, апоптоз, продукцию межклеточного вещества, на пролиферацию и миграцию эндотелиоцитов, играющих важную роль в процессе развития опухоли. Полученные научные данные внесли не только определенную ясность в понимание механизмов влияния половых стероидов на рост миомы матки, но наметили новые направления в медикаментозном лечении.
Диагностика. Клиника
Основными инструментальными методами диагностики миомы матки являются ультразвуковое исследование (УЗИ), значительно реже — компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). В последние два десятилетия гистероскопия и лапароскопия обеспечили новый метод диагностики и лечения миомы матки. Информативным методом распознавания субмукозной и интерстициальной с центропетальным ростом миомы матки является гистероскопия (точность достигает 99,2%). Достоинство метода — возможность одновременной биопсии эндометрия, с целью диагностики сопутствующих гиперпластических процессов. Лапароскопия используется преимущественно при необходимости дифференциальной диагностики миомы и опухоли яичника, а также для распознавания вторичных изменений в миоматозных узлах, являющихся противопоказанием к консервативной терапии.
У половины пациентов болезнь протекает бессимптомно и диагностируется только при гинекологическом или ультразвуковом исследовании. Но у каждой второй женщины возникают симптомы заболевания, которые ухудшают качество жизни и требуют лечения. Симптомы зависят от количества, размеров и расположения миоматозных узлов, а также от степени вторичных дегенеративных и воспалительных изменений в ткани узлов. Основные симптомы лейомиомы матки: 1) обильные, длительные менструации и/или ациклические кровотечения, которые сопровождаются слабостью, утомляемостью, приводят к развитию железодефицитной анемии, 2) тянущие боли внизу живота (у 20–30% больных), очень редко возникают острые боли, связанные с нарушением кровотока в миоматозных узлах, и сопровождаются повышением температуры, слабостью, 3) при больших размерах лейомиомы матки может происходить давление на соседние органы: мочевой пузырь, прямую кишку, что проявляется учащенным мочеиспусканием, запорами, 4) бесплодие, невынашивание беременности, осложнения во время родов наблюдаются у каждой третьей пациентки с множественными миомами.
Тактика ведения
Несмотря на то, что миома матки является наиболее часто выявляемым заболеванием, в тактике ведения больных данной патологией остается много нерешенных вопросов и противоречий. В разных странах имеются различные подходы к лечению заболевания, отличаются и показания к радикальным операциям. Тактика ведения больных миомой матки включает три основных направления: выжидательное, консервативное и активное воздействие на опухоль.
Выжидательное ведение больных с миомой матки возможно только при отсутствии симптоматики и небольших по размеру (до 10–12 недель) опухолях при реализованной репродуктивной функции и заключается в активном амбулаторном наблюдении: динамическое ультразвуковое исследование, цитологический контроль состояния эпителия шейки матки и эндометрия, определение уровня онкомаркеров. Однако, учитывая частоту встречаемости сопутствующей патологии при миоме матки, только у небольшого числа пациентов мы можем ограничиться выжидательной тактикой ведения.
Консервативное ведение больных миомой матки заключается преимущественно в гормональном лечении, хотя в последние годы предложены противофибротические средства, антиангиогенные, аналоги соматостатина (в настоящий момент эти препараты находятся на стадии клинических испытаний). Среди гормональных препаратов несомненное лидерство принадлежит аналогам гонадолиберина и антигестагенному препарату — мифепристону (RU 486). Эти препараты используются как в качестве самостоятельного лечения, показания к которому четко определены, так и в качестве адъювантной терапии, имеющей определенные преимущества и недостатки.
Активная тактика ведения больных с миомой матки делится на два основных направления: хирургическое лечение и малоинвазивные вмешательства. Хирургический метод продолжает оставаться основным методом лечения данной категории больных — до 80% больных подвергаются гистерэктомии или миомэктомии. Однако многие женщины в наше время стремятся отложить деторождение на более поздний возраст, когда, к сожалению, значительно чаще развивается лейомиома матки. Поэтому совершенствование медикаментозного лечения и малоинвазивных, органосохраняющих технологий является основной тенденцией в современных условиях.
Методы лечения
Поиск и применение новых лекарственных средств и малоинвазивных технологий, приближающихся по эффективности к гистерэктомии и не вызывающих побочных эффектов, является альтернативным лечением миомы матки.
В настоящее время можно выделить три основных подхода к лечению миомы матки.
Традиционно терапевтическое лечение миомы матки основывается на воспроизведении медикаментозной псевдоменопаузы и/или индукции гипоэстрогении. Медикаментозная терапия в качестве монотерапии, как правило, назначается пациенткам при бессимптомном течении заболевания и при небольших (соответствующих менее 12 нед беременности) размерах опухоли [1, 15, 16). На протяжении довольно длительного времени использовались гестагены: норэтистерон (Норколут, Примолют-нор), дидрогестерон (Дюфастон) и др. Однако результаты лечения были малоэффективны. Основываясь на прогестероновой гипотезе развития миомы матки, малоэффективные результаты лечения производными прогестерона вполне объяснимы. В настоящее время применение гестагенов оправдано только при сочетании миомы матки (небольших размеров) с гиперпластическими процессами эндометрия и аденомиозом у женщин позднего репродуктивного или пременопаузального периода при постоянном динамическом наблюдении. Современное медикаментозное лечение включает применение агонистов гонадотропин-релизинг гормона (аГн-РГ) либо в качестве долгосрочной монотерапии, либо как этап комбинированного метода [15, 16].
Однако при несомненной эффективности этих препаратов, даже при минимальном курсе лечения (3–4 месяца), они обладают выраженным побочным действием, связанным с развитием эстроген-дефицитного состояния. Механизм действия этих препаратов заключается в подавления гонадотропной функции гипофиза, вследствие которой развивается гипоэстрогения и блокада продукции прогестерона. Очевидно, агонисты гонадолиберина действуют непосредственно и на опухолевую ткань, что подтверждается наличием рецепторов к гонадолиберину, снижением уровня рецепторов к эпидермальному фактору роста, подавлением продукции ТФР-бета и пролактина непосредственно в ткани лейомиомы матки (при лечении этими препаратами). Возможна также непосредственная стимуляция аналогами гонадолиберина процессов апоптоза в опухолевой ткани, что подтверждается повышением экспрессии рецепторов Fas и их лигандов (маркеры апоптоза). Десенситизация гипофиза и подавление функции яичников приводят к уменьшению объема матки и лейомиомы примерно на 50–65% и прекращению меноррагий, благодаря развитию аменореи, что позволяет скорректировать анемию до операции. Оптимальным режимом введения данных препаратов является короткий 3–4-месячный курс с ежемесячными инъекциями. Важной особенностью действия аГн-РГ является снижение кровоснабжения узлов, что стимулирует процесс апоптоза, а также уменьшает кровопотерю и сокращает длительность оперативного вмешательства. Побочные эффекты аГн-РГ связаны с гипоэстрогенией, проявляющейся вазомоторными симптомами, снижением минеральной плотности костной ткани, что ограничивает длительность приема и требует корригирующей терапии.
Принципиально новым препаратом, применяемым при лечении больных с миомой матки, является антипрогестин — мифепристон. Мифепристон — это синтетический стероид, обладающий одновременно антипрогестероновой и антиглюкокортикоидной активностью. Механизм действия заключается в связывании с прогестероновыми рецепторами, вследствие чего блокируется их функция. Суточная доза препарата — 50 мг в течение трех месяцев перорально, непрерывно. Эффективность препарата сравнима с эффективностью аналогов гонадолиберина — на 40–49% уменьшаются размеры матки и узлов. Основная особенность действия этого препарата — отсутствие гипоэстрогении, поэтому не наблюдается ни вазомоторных симптомов, ни снижения минеральной плотности костной ткани. У большинства женщин с миомой матки развивается аменорея при 3-месячном и более длительном курсе лечения. Первоначально мифепристон у больных с миомой матки применялся в качестве предоперационной подготовки, что являлось вполне обоснованным, так как при минимальных побочных эффектах (слабые приливы, тошнота) удается добиться снижения размеров опухоли и уменьшения менометроррагий. В настоящее время проводятся научные исследования по применению этого препарата и в качестве единственного метода лечебного воздействия в более длительном режиме [10, 22, 23].
Недавно предложены совершенно новые подходы к лечению миомы матки — блокирование действия специфических факторов роста [16, 28]. Действие одной группы препаратов (так называемая антифибротическая терапия) основывается на том, что лейомиомы содержат большое количество внеклеточного матрикса, состоящего из фибронектина, коллагена типа 1, 3 и протеогликанов. Доказано, что ТФР-бета и ФРФ увеличивают продукцию межклеточного вещества гладкомышечными клетками и снижают образование коллагеназы. Пирфенидон — антифиброзный препарат, ингибирует синтез ДНК, клеточную пролиферацию и продукцию коллагена в гладкомышечных клетках лейомиомы и нормального миометрия, вызванную вышеназванными факторами роста. Этот препарат обладает дозозависимым действием, минимальным количеством побочных эффектов и не оказывают токсического воздействия на гладкомышечные клетки. (В настоящее время проводятся клинические испытания.)
Действие другой группы препаратов основывается на ингибировании ангиогенеза [6, 14, 16]. Несколько факторов роста принимают участие в процессе ангиогенеза: ФРФ, ТФР, СЭФР (последний является важнейшим, так как синтезируется большинством линий опухолевых клеток и обладает многосторонним влиянием). Двумя основными механизмами эти факторы роста индуцируют рост лейомиомы матки: первый — усиление пролиферации, миграции гладкомышечных клеток сосудов и эндотелиоцитов; второй — стимуляция формирования кровеносных сосудов. Пока только единственный препарат, обладающий ингибирующим влиянием на ангиогенез, — интерферон-альфа прошел клиническое испытание на 20 больных с лейомиомой матки. Показано достоверное уменьшение объема образования уже после первой недели лечения. Таким образом, ингибирование ангиогенеза, посредством воздействия на перечисленные факторы роста, представляет собой одну из наиболее перспективных стратегий лечения лейомиомы матки.
Следовательно, для большинства пациентов более привлекательным остается медикаментозное лечение в качестве единственного метода. Поэтому поиск новых лекарственных средств, позволяющих избежать оперативное вмешательство и в то же время не приводящих к выраженным побочным эффектам, поможет решить важную проблему женского здоровья.
Другим направлением в органосберегающих методах лечения миомы матки, которые бы при высокой эффективности обладали и максимальной (достаточной) безопасностью, стала разработка в конце 90-х годов нового неинвазивного хирургического метода, который получил название «Неинвазивная абляция миомы матки воздействием фокусированного ультразвука (ФУЗ) под контролем ядерно-магнитно-резонансной томографии».
Об эффективности и безопасности ФУЗ-МРТ-абляции сообщали C. M. Tempany и соавт. (2000), Rabinovici J. и соавт. (2002), а Jolesz F. A., Hynynen K. (2002) назвали метод ФУЗ «идеальной операцией». Технология ФУЗ-МРТ представляет собой сочетание высокоинтенсивного фокусированного ультразвука, луч которого неинвазивно нагревает выбранные участки ткани миомы и вызывает их термический некроз, и магнитно-резонансной томографии. Звуковые волны проходят сквозь ткани, не вызывая их повреждения, и за счет фокусировки волн происходит локальный нагрев ткани миомы до 55–90 °С, что вызывает термическую коагуляцию в четко ограниченной области, не оказывая никакого вредного воздействия на окружающие ткани, т. е. ФУЗ-МРТ-абляция обеспечивает локальный селективный коагуляционный некроз в малом объеме ткани (в точке фокуса), что используется для прецизионной неинвазивной абляции опухолей.
Процесс лечения состоит в последовательных воздействиях (так называемых соникаций) на небольшие фрагменты опухоли, что приводит к нагреванию их и селективному коагуляционному некрозу. Механизм действия ФУЗ-абляции включает как прямое, так и опосредованное повреждающее воздействие. Прямое — это термическое воздействие за счет высвобождения энергии звуковой волны. Опосредованное — за счет изменения локального кровотока и нарушения питания опухолевой ткани. Доказано, что при нагревании ткани до 60 °С в течение 1 секунды происходит гибель всех клеток за счет их дегидратации, повреждения сосудистых структур, денатурации белков и разрушения коллагеновых волокон. Иммуногистохимические исследования показали, что данный метод вызывает летальное или сублетальное повреждение опухолевой ткани и исчезновение ее пролиферативной активности, при этом избирательность воздействия и полная безопасность ФУЗ для интактных тканей, окружающих миому, обусловлены также разницей в перфузии крови в миоматозном узле по сравнению с нормальным миометрием и преимущественным расположением сосудов по периферии узла миомы.
ФУЗ-МРТ-абляция особенно эффективна для лечения миомы матки вследствие высокого содержания экстрацеллюлярного матрикса, хорошо поглощающего тепло. Для доброкачественной опухоли нет необходимости элиминации каждой ее клетки, поэтому достаточно произвести коагуляцию в отдельных точках внутри миомы, что позволяет сократить объем миоматозных узлов и матки и тем самым уменьшить меноррагии, боли и давление на соседние органы малого таза, значительно улучшить качество жизни.
Продолжительность процедуры ФУЗ-абляции зависит от объема и количества узлов и в среднем составляет 3–4 часа. Эта процедура проводится амбулаторно, без общей анестезии, во время нее пациентка находится в сознании. После лечения пациентки обычно наблюдаются в стационаре в течение двух часов, что обусловлено только периодом действия седативных препаратов премедикации, и на следующий день уже трудоспособны.
Показаниями к ФУЗ-МРТ-абляции миомы матки являются: меноррагии, болевой синдром, симптомы сдавления соседних органов, размеры миоматозных узлов от 2 до 15 см, интерстициально-субсерозные, интерстициальные и интерстициально-субмукозные узлы, при количестве миоматозных узлов не более 5.
Противопоказаниями для ФУЗ-МРТ-абляции миомы следующие: субсерозные миомы на ножке, сочетанная гинекологическая патология — воспалительные процессы в малом тазу, бесплодие, образования в яичниках, гиперплазия эндометрия; онкологические заболевания, нереализованная репродуктивная функция, размеры миоматозных узлов менее 2 см, выраженное retroflexio-versio матки, грубые послеоперационные рубцы на передней брюшной стенке, ожирение II–III степени, тяжелые аллергические реакции на контрастные вещества, а также клаустрофобия, наличие крупных ферромагнитных имплантантов, наличие искусственных водителей ритма сердца (противопоказания для проведения МРТ).
Индивидуализация применения ФУЗ-МРТ-абляции миомы матки заключается в определении «доступности» миоматозных узлов для фокусированного ультразвука (предпочтительна локализация узлов по передней стенке и в дне матки), определении МРТ-типов миомы, необходимости проведения дополнительных манипуляций (висцеральный массаж, наполнение мочевого пузыря физиологическим раствором и т. д.), при этом интраоперационная эффективность ФУЗ-МРТ-абляции миомы снижается.
Обычно проводится либо «малая» процедура, при которой абляции подвергается около 30–35% объема миоматозного узла, либо «большая» — коагулируется не менее 70% объема. После «малой» процедуры не происходит значительного уменьшения размеров опухоли, тем не менее в 80% случаев отмечается значительная положительная динамика, исчезновение жалоб, болей и прекращение кровотечений. Кроме того, снижается пролиферативная активность миомы, и рост узлов прекращается. Это объясняется уменьшением плотности ткани после ФУЗ-МРТ-абляции — узлы становятся более «мягкими» и не оказывают выраженного давления на окружающие ткани. В настоящее время проводится лечение миом матки диаметром до 9 см, а в случае большого размера миомы — предварительная гормональная терапия в течение трех месяцев, с целью сокращения узлов и возможности проведения процедуры. Группой исследователей из США изучена безопасность и эффективность операций фокусированным ультразвуком под контролем МРТ для неинвазивного лечения лейомиомы матки [3, 24]. Согласно этим данным происходит уменьшение миомы через 3 мес на 37%, через 6 мес на 48% [19, 24]. За последние 2 года получено 30 беременностей у женщин, перенесших ФУЗ-МРТ-абляцию миомы матки и 13 родов без осложнений [26]. Среди осложнений ФУЗ-МРТ-абляции выделяют незначительную воспалительную реакцию (субфебрильная температура) и ожог I степени.
Таким образом, ФУЗ-МРТ-абляция имеет определенные преимущества по сравнению с малоинвазивными и инвазивными методами лечения: