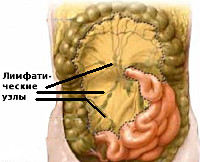
Мезаденит ( Мезентериальный лимфаденит )
МКБ-10
Общие сведения
Причины мезаденита
Заболевание развивается при наличии первичного очага воспаления в аппендиксе, кишечнике, бронхах и других органах. Лимфогенным, гематогенным или энтеральным (через просвет кишечника) путем инфекция поступает в лимфатические узлы брыжейки, где происходит размножение патогенных микроорганизмов. Причиной формирования мезаденита могут служить следующие возбудители:
Предрасполагающими факторами к развитию мезаденита являются снижение иммунитета и сопутствующие воспалительные поражения ЖКТ. Преимущественное поражение детей и подростков связано с несовершенством иммунной и пищеварительной системы, частыми пищевыми отравлениями и ОРВИ.
Патогенез
Лимфоузлы брыжейки являются барьером для проникновения инфекции из кишечника и внутренних органов в брюшное пространство. При существовании первичного воспалительного очага (в кишечнике, верхних дыхательных путях) инфекционные агенты лимфогенным, энтерогенным или гематогенным путем поступают в лимфоузлы. При наличии предрасполагающих факторов происходит рост количества патогенных микроорганизмов. Возникает отек и гиперемия брыжейки. Лимфатические узлы, преимущественно в зоне илеоцекального угла, имеют мягкую консистенцию, красный цвет. При нагноении лимфоузлов формируется инфильтрат с гнойным расплавлением и участками некроза. Генерализация инфекционно-воспалительного процесса сопровождается поражением жировой ткани брыжейки. При гистологическом исследовании отмечается лейкоцитарная инфильтрация и лимфоидная гиперплазия узлов, утолщение и отечность капсулы. В зависимости от тяжести мезаденита в брюшной полости формируется серозный или серозно-гнойный выпот.
Классификация
Заболевание вызывает поражение как отдельных лимфоузлов, так и целой группы. По течению патологического процесса выделяют острые и хронические мезадениты. Острая патология сопровождается внезапным развитием и яркой симптоматикой. Хроническое течение заболевания имеет стертую клиническую картину в течение длительного времени. В зависимости от типа возбудителя различают следующие виды мезаденитов:
Симптомы мезаденита
Острая форма заболевания характеризуется внезапным началом и быстрым развитием симптоматики. Возникают продолжительные схваткообразные боли в околопупочной области или в верхней части живота. В некоторых случаях пациенты не могут указать точную локализацию болезненных ощущений. Интенсивная боль постепенно сменяется тупой и умеренной болезненностью, которая усиливается при резкой смене местоположения, кашле. Заболевание проявляется лихорадкой, повышением частоты сердечных сокращений (до 110-120 уд./мин) и дыхательных движений (25-35 в мин). Нарастают диспепсические расстройства: появляется тошнота, сухость во рту, диарея, однократная рвота. Иногда заболевание сопровождается катаральными явлениями (насморком, кашелем, гиперемией зева), герпесом на губах, крыльях носа.
При формировании гнойного мезаденита интенсивность боли уменьшается, нарастает интоксикация организма, общее состояние пациента ухудшается. Хроническое течение болезни отличается стертой симптоматикой. Боли слабо выражены, без определённой локализации, носят кратковременный характер и усиливаются при физической нагрузке. Периодически возникает непродолжительная тошнота, запор или жидкий стул. Туберкулезный мезентериальный лимфаденит сопровождается постепенным нарастанием симптомов. Отмечается выраженная интоксикация с развитием слабости, апатии, бледности кожных покровов с появлением землистого оттенка кожи, субфебрилитета. Боли ноющие, непродолжительные, не имеющие четкой локализации.
Осложнения
Диагностика
Неспецифическая клиническая картина вызывает значительные трудности при диагностике болезни. Чтобы не упустить развития серьезных осложнений, диагностические манипуляции рекомендовано проводить в полном объеме. Диагностика мезентериального лимфаденита включает:
Диффенциальная диагностика
Дифференциальная диагностика мезаденита проводится с острой хирургической патологией брюшной полости:
При болях внизу живота болезнь дифференцируют с аднекситом, апоплексией яичника. Схожую симптоматику могут иметь доброкачественные и злокачественные новообразования, специфическое увеличение брыжеечных лимфоузлов при ВИЧ-инфекции, сифилисе, лимфогранулематозе.
Лечение мезаденита
Основной задачей при лечении заболевания служит выявление и санация первичного очага инфекции. При неосложненном остром течении болезни применяют консервативную терапию. Этиотропно назначают антибактериальные препараты, исходя из вида бактериального возбудителя. При туберкулезном мезадените показано проведение специфической терапии в условиях противотуберкулезного диспансера. Симптоматически назначают противовоспалительные, обезболивающие, иммуностимулирующие препараты. При интенсивной длительной боли проводят паранефральную блокаду. Для уменьшения интоксикации выполняют парентеральную дезинтоксикационную терапию.
При гнойном мезадените показано хирургическое лечение. Проводят вскрытие и дренирование абсцесса с ревизией брюшной полости. Всем пациентам рекомендовано соблюдать диету (стол №5). Необходимо отказаться от жирных, жареных, копченых блюд, мучных изделий, кофе, алкоголя. Предпочтение следует отдать нежирным сортам рыбы и мяса, овощным супам, кашам, морсам. Пищу рекомендовано принимать 4-5 раз в сутки небольшими порциями. Физиотерапевтическое лечение включает проведение магнитотерапии, УВЧ-терапии. В период ремиссии и реабилитации показана лечебная гимнастика под контролем врача ЛФК.
Прогноз и профилактика
Прогноз мезентериального лимфаденита благоприятный при своевременной диагностике и грамотной терапии болезни. Развитие осложнений может повлечь за собой тяжелые, жизнеугрожающие состояния (перитонит, сепсис, кишечная непроходимость). Основой профилактики служит выявление и лечение хронических очагов воспаления, которые могут послужить источником формирования мезаденита. Для профилактики большое значение имеет периодическое прохождение медицинских осмотров, поддержание здорового образа жизни и укрепление иммунитета (прием мультивитаминов, прогулки на свежем воздухе, закаливание).
Диета 5-ый стол
Основываясь на данных, полученных в многочисленных исследованиях, М. И. Певзнер разработал 15 лечебных диет, снижающих уровень риска последующего обострения и развития заболеваний жизненно важных внутренних органов, а также укрепляющих иммунитет человека. Одним из наиболее эффективных методов лечения и профилактики заболеваний мочевыводящей системы и печени признана диета № 5, которой можно следовать долгие годы даже в домашних условиях.
Лечебная программа не используется сама по себе как панацея от болезней, а только в сочетании с физиотерапевтическим и медикаментозным лечением. Начинать соблюдать эту диету желательно только после консультации с врачом.
При полном соблюдении всех правил диеты ремиссия может быть достигнута в очень короткие сроки, нормализуется работа всех органов пищеварения и печени, снимется обострение. Необходимо выполнять все предписания врача. Если указано использовать вчерашний хлеб, это означает, что свежий категорически запрещен. Если указано, что любая грубая пища должна перетираться, это необходимо сделать, иначе смысла в диете нет.
Общие правила диеты №5
Заболевания печени можно схематически разделить на две большие группы: заболевания тканей печени и заболевания желчевыводящих путей. Однако в тканях печени желчные протоки обычно более или менее вовлечены в процесс и поражаются заболеваниями желчных протоков паренхимы печени. Это следует учитывать при назначении терапии и, в частности, лечебного питания.
Функции печени регулируются центральной нервной системой, гормональными и нейрогуморальными влияниями. Интоксикация, лихорадка, голодание, инсульт и т. д. уменьшают запасы гликогена в печени и увеличивают содержание жира в печени.
Энергетическая ценность ежедневного меню варьируется от 2100 до 2500 ккал. Увеличивается частота приема пищи до 5-6 раз в день, при этом уменьшается количество еды, потребляемой за раз. Масса суточного рациона – 3 кг.
Раз в неделю полезно проводить постные дни: овощи, кисломолочные продукты, яблоки. Необходимо ограничить потребление холестерина.
Показания к диете №5
В приоритете – химически и механически щадящее воздействие на слизистую оболочку желудка и кишечника с помощью здоровой пищи. Особое внимание уделяется качеству продуктов, включаемых в рацион. Значение имеет способ приготовления и отказ от вредных добавок.
«Стол №5»: что можно и что нельзя
Будет полезно обогатить диету продуктами, содержащими магний. Этот элемент помогает выводить вредный холестерин из организма, а также снимает мышечные спазмы, выстилающие желчный пузырь, что способствует оттоку желчи. Рекомендуется включить в рацион продукты, стимулирующие моторику кишечника.
МОЖНО включать в рацион
НЕЛЬЗЯ включать в рацион
супы без мяса на овощном бульоне (предварительно протертые);
молочные супы с макаронными изделиями или крупами;
борщи (сваренные без мяса);
щи (без мяса и кости)
концентрированные грибные и мясные бульоны;
Вторые блюда (гарнир)
крупяные каши (в протертом или полувязком состоянии);
пудинги, суфле и творожные запеканки с изюмом
мюсли и овсяные хлопья
сельдь (предварительно вымоченная);
фруктовые или овощные салаты
имбирь (в маринованном виде)
Рыба, мясо и морепродукты
креветки, мидии и кальмары;
лосось и семга (на пару или слабосоленые);
мясо и рыба (до трех раз в неделю);
допустим плов и голубцы
субпродукты (печень, почки, желудочки, язык и пр.);
колбаса, сардельки, сосиски;
свекла, кабачки, картофель, морковь (отварные, запеченные);
баклажаны, брокколи, сельдерей;
салат, помидоры, огурцы, болгарский перец
капуста, редис, кукуруза;
яблоки (преимущественно в запеченном виде);
гранат (без гемохроматозов)
сырые фрукты и ягоды
печенье (только галетное)
блины и сегодняшний хлеб;
слоеное и дрожжевое тесто
вареники с начинкой из ягод и картофеля;
мармелад на пектине;
мусс, домашнее желе, кисель собственного приготовления;
сухофрукты (курага, чернослив, финики);
яблочный зефир и меренги
шоколад (горький, молочный)
йогурт, кефир, сметана;
творог, цельное пастеризованное молоко
продукты с показателем жирности более 2%
сливочное (до 30 гр);
растительные (от 10 до 15 гр)
желток (не более ½ шт. в день)
яйцо сваренное вкрутую
свежевыжатые соки (без добавления сахара);
желе (домашнее приготовление);
муссы (приготовленные на ксилите)
зеленый чай и кофе;
спиртосодержащие напитки и газировка
базилик, укроп и петрушка;
кетчуп, горчица и майонез (магазинные);
уксус и острый перец
Разновидности диеты №5
Предварительно нужно изучить разновидности диеты. Каждая из них имеет определенное предназначение и свои особенности.
Единое для всех – время приема пищи. Завтрак должен быть в 8.00-9.00, полдник – с 12.00 до 13.00, ужин – с 16.00 до 17.00, второй ужин – в 19.00-20.00. Легкий перекус в качестве третьего ужина допустим в 20.00 (кефир, ряженка и пр.).
Стол номер 5а
Диета 5а является переходным моментом после диеты №4. Благодаря правильно подобранному рациону удается значительно уменьшить нагрузку на печень и максимально восстановить функциональность органа. Основное ее отличие заключается в особом приготовлении блюд. Все продукты должны употребляться только в приготовленном и тщательно протертом виде. Супы готовятся на овощных бульонах. Крупы необходимо доводить до разваренного состояния.
Стол номер 5в
Показанием для введения диеты 5в является хронический панкреатит. Отличительная особенность предлагаемого лечебного питания заключается во введении в рацион большего количества продуктов, содержащих белок. Суточная норма должна составлять около 130 гр. При этом необходимо сократить потребление углеводов и жиров.
Стол 5в рекомендуется соблюдать на протяжении всей жизни. Диетическое питание уменьшает процесс прогрессирования болезни и снижает возможность возникновения рецидива.
Стол номер 5п (I)
Стол номер 5п (II)
Показан при хронической форме и на стадии затухания острого панкреатита. Главная цель заключается в нормализации процессов метаболизма и предотвращении дальнейшего развития заболевания, а также в исключении возникновения рецидивов.
Стол номер 5щ
Диета 5щ предполагает уменьшение симптоматики при нарушенном желчеотделении, сопровождаемом дуоденитом. Направлено лечебное питание на восстановление обменных процессов и снижения оттока желчи. При этом раз в неделю предусмотрен разгрузочный день.
Стол номер 5ж/л
Стол номер 5р
Разновидность данного дополнения к основной терапии показана при развитии демпинг-синдрома на фоне проведения операции язвы желудка. Основное направление диеты заключается в уменьшении секреторной активности ЖКТ, снижении раздражения слизистой желудка.
Особенности стола №5 при желчнокаменной болезни
Имеется ряд продуктов, которые запрещены к употреблению. Среди них следует выделить жирные сорта мяса и рыбы, животные жиры и желток куриного яйца. Недопустимо включать в рацион жареные, копченые и маринованные продукты. Исключить следует концентрированные грибные супы. Отказаться нужно от мучных и сдобных изделий, а также от кисло-сладких сортов ягод. Негативно сказывается на состоянии желчного пузыря крепкий кофе и чай, а также черный шоколад. Недопустимы спиртные напитки, маринады и пряности.
Таблица – Диета №5 при желчнокаменной болезни – образцовое меню
овсянки с оливковым маслом
стакан чая с молоком
порция вегетарианского супа
приготовленные на пару овощи (желательно морковь)
отвар диких роз с хлебом или сухариками
котлеты из капусты и моркови с растительным маслом
Полезно за 2 часа до сна выпивать стакан кефира. Жирность должна быть не более 2%.
Если пациент положительно реагирует на изменение диеты, стол вводят в течение длительного периода времени. Минимальная продолжительность – 5 недель или до тех пор, пока не наступит постоянная ремиссия. Продолжительность употребления обусловлена максимальным приближением диеты №5 к нормальному здоровому питанию.
Этот курс проводится длительное время в течение 1,5-2 лет. Питание и ингредиенты могут быть изменены в соответствии с основными рекомендациями диеты.
Диета №5 после удаления желчного пузыря
Многие люди, которые подвергаются удалению желчного пузыря, испытывают некоторые осложнения в дальнейшем. Исследования показали, что 10 – 30% пациентов, перенесших удаление желчного пузыря, страдают от диареи. Это осложнение должно проходить само по себе в течение определенного периода времени. Но бывают случаи, когда этот неприятный симптом сохраняется в течение многих лет.
При здоровом желчном пузыре секреция и поток желчи находятся под контролем гормона, называемого холецистокинином. Как только желчный пузырь удален, этот гормон больше не контролирует поток желчи. Было обнаружено, что после удаления желчного пузыря поток желчи является непрерывным.
Желчные соли необходимы для переваривания и поглощения жира. Если человек, перенесший операцию по удалению желчного пузыря, употребляет в пищу продукты с высоким содержанием жиров, происходит плохая усвояемость, что может привести к жирной диарее. Исследования показали, что содержание жира в стуле выше у людей, у которых был удален желчный пузырь.
Количество калорий, обеспечиваемых жиром, должно быть ограничено менее чем 30% от общего рациона.
Употребление овощей имеет особое значение. При удалении желчного пузыря помощь кишечнику более актуальна. Приготовленные овощи легче усваиваются и помогают снизить кислотность, вызванную желчью.
Сырые овощи более сложны для переваривания. Хотя они приносят такое же количество клетчатки, лучше не усложнять работу кишечника.
Желчная диета должна содержать около 30 г липидов в день, то есть менее 25% от общего количества.
Организм человека имеет особенность легко приспосабливаться к изменениям, со временем привычный образ жизни восстанавливается. Очень важно следовать рекомендациям врача, чтобы избежать повреждения пищеварительного тракта. Около 95% людей, у которых был удален желчный пузырь, смогли вернуться к нормальному питанию в течение короткого времени.
Лечебный рацион
Меню диеты №5 (режим питания)
Среда
Пост на кефире. Нужно взять 1-1,5 литра 1%-го кефира и употребить его за 5-6 приемов в течение дня. Допустимо также пить воду и несладкий чай.
Воскресенье
Пост на зеленых яблоках. Полтора килограмма разделить на 6 приемов в течение дня. Нужно пить много чистой негазированной воды и несладкого чая.
Такая диета поможет улучшить состояние желчного пузыря и протоков, снизить уровень холестерина.
Плюсы и минусы
В стационарных условиях пациентов кормят четыре раза в день. На завтрак приходится 25-30% суточной калорийности, на обед – 35-40%, на полдник – 10-15% и на ужин – 25-30%. Аналогично нужно поступать и в домашних условиях. Особое внимание необходимо уделить завтраку, поскольку утром энергозатраты являются максимальными, а к вечеру они снижаются.
В ежедневном рационе должны присутствовать фрукты и овощи. Белковая пища должна присутствовать 1-2 раза в день. Рыбные и мясные блюда должны сочетаться с овощами. Чем разнообразнее будет рацион, тем лучше. Но основной упор нужно делать не на количество, а на качество с медицинской точки зрения.
Номерная система диет направлена на лечение зафиксированных заболеваний, без учета потребностей конкретного пациента. Данный вариант удобен для организации коллективного, но не индивидуального питания. В современной диетологии диеты по Певзнеру уже считаются устаревшими, т. к. они рассчитаны преимущественно на обобщенные модели заболеваний, а не на больных, которые могут страдать несколькими недугами. На практике пациенты часто не «вписываются» в установленную модель болезни, поэтому и диета им не подходит.
Острый мезаденит: взгляд педиатра
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Мезаденит (мезентериальный лимфаденит, мезентерит) — воспаление лимфатических узлов брыжейки — нередко является причиной острого болевого абдоминального синдрома у детей. Диагностическая и лечебная тактика при мезадените является актуальной междисциплинарной проблемой, которая находится на стыке интересов педиатров и детских хирургов.
Цель исследования: проанализировать влияние особенностей клинической картины дебюта заболевания на сроки верификации диагноза «острый мезаденит» у детей.
Материал и методы: проведен ретроспективный анализ историй болезни 65 детей в возрасте от 1 года 6 мес. до 17 лет 9 мес., которые находились на лечении в хирургическом отделении ДГКБ св. Владимира в 2012–2017 гг. с основным клиническим диагнозом «острый мезаденит».
Результаты исследования: наиболее высока заболеваемость мезаденитом у детей младшего школьного возраста (средний возраст пациентов составил 10,5 года), что коррелирует с возрастающей инфекционной нагрузкой. Чем более выражены симптомы заболевания, тем быстрее пациент попадает в поле зрения специалиста. Отсутствие патогномоничных жалоб и симптомов при остром мезадените, полиморфность клинической картины, относительная редкость и неспецифичность сдвигов в показателях клинического и биохимического анализов крови и общего анализа мочи не позволяют установить точный диагноз без использования дополнительных исследований. Для полной верификации диагноза острого мезаденита применяются инструментальные исследования: УЗИ органов брюшной полости, забрюшинного пространства и малого таза для дифференциальной диагностики причин абдоминальной боли и диагностическая лапароскопия для окончательной верификации диагноза. Серологические исследования необходимы для установления этиологии мезаденита и выбора комплексного лечения заболевания. Целесообразно расширение алгоритма диагностического поиска среди вирусных инфекций, индуцирующих лимфоидную пролиферацию.
Заключение: острый мезаденит является междисциплинарной проблемой педиатрии и детской хирургии, которая требует квалифицированных и последовательных совместных усилий педиатров и детских хирургов, направленных на ускорение оказания специализированной помощи ребенку.
Ключевые слова: острый мезаденит, дети, дебют заболевания, дифференциальная диагностика, ультразвуковое исследование, диагностическая лапароскопия.
Для цитирования: Барденикова С.И., Шавлохова Л.А., Шувалов М.Э. Острый мезаденит: взгляд педиатра. РМЖ. Медицинское обозрение. 2019;3(5):2-10.
1 Yevdokimov Moscow State University of Medicine and Dentistry
2 Children’s City Clinical Hospital of St. Vladimir, Moscow
Mesenteric lymphadenitis (mesadenitis) — a mesenteric lymph nodes inflammation — is the common cause of acute abdominal pain in children. Diagnostic and treatment tactics for mesadenitis is a relevant interdisciplinary problem, which is at the intersection of the pediatricians’ and pediatric surgeons’ interest.
Aim: to analyze the clinical picture impact of the disease onset on diagnosis verification terms of acute mesadenitis in children.
Patients and Methods: 65 children’s case histories (with mesadenitis) aged 1 year and 6 months up to 17 years and 9 months who were treated in the Department of Abdominal Surgery of the Children’s City Clinical Hospital of St. Vladimir in 2012–2017 underwent a retrospective analysis.
The more pronounced the disease symptoms, the faster the patient comes onto the radar of specialist. Absence of pathognomonic complaints and symptoms in acute mesadenitis, clinical picture polymorphism, and relative rarity and changes’ nonspecificity in complete blood count, biochemical analysis and clinical urinalysis indicators do not allow an accurate diagnosis without the use of additional research. So,
the following instrumental methods of examination are needed for a complete diagnosis verification of acute mesadenitis: abdominal cavity ultrasound, pelvic and retroperitoneum ultrasound for the differential diagnosis of the abdominal pain causes, and diagnostic laparoscopy
for the final diagnosis verification. Serological studies are necessary to establish the etiology of mesadenitis and the complex treatment tactics for the disease. Diagnostic search algorithm expansion among viral infections that ind uce lymphoid proliferation is also advisable.
Conclusion: acute mesadenitis is the interdisciplinary problem of pediatrics and pediatric surgery that requires skilled and consistent joint efforts aimed at accelerating the provision of specialty care to the child.
Keywords: acute mesadenitis, children, disease onset, differential diagnostics, ultrasound, diagnostic laparoscopy.
For citation: Bardenikova S.I., Shavlokhova L.A., Shuvalov M.E. Acute mesadenitis: pediatrician point of view. RMJ. Medical Review. 2019;5:2–10.
Статья посвящена проблеме острого мезаденита в педиатрии, представлены результаты оригинального исследования.

Введение
Актуальность проблемы
Мезаденит, или мезентериальный лимфаденит, мезентерит — воспаление лимфатических узлов брыжейки — нередко является причиной острого болевого абдоминального синдрома у детей. Диагностика и лечение мезаденита находятся на стыке интересов педиатров и детских хирургов, что постоянно поддерживает актуальность данной проблемы. Сложности верификации заболевания, связанные с отсутствием единых диагностических критериев, не позволяют оценить истинную частоту острого неспецифического мезаденита (т. е. вызванного неспецифическими возбудителями) в детском возрасте. В хирургических стационарах заболевание регистрируется у 11,7–18,4% пациентов с острым абдоминальным синдромом [1–6]. У детей, госпитализируемых с подозрением на острый аппендицит, мезаденит выявляют в 8–9% случаев. Заболевание диагностируют преимущественно у детей в возрасте от 5 до 13 лет [1, 2, 4, 7, 8], причем чаще болеют мальчики. Заболеваемость мезаденитом возрастает в межсезонье, коррелируя с эпидемиологией ОРВИ [9]. В последние годы наблюдается рост заболеваемости как среди детского, так и среди взрослого населения, однако, возможно, этот факт отражает улучшение диагностики мезаденита [1, 9].
Воспалительные (неаппендикулярные) процессы брюшной полости, являясь причиной симптомокомплекса «острого живота», нередко приводят к гипердиагностике острого аппендицита, при этом на маскирующийся под него мезаденит у детей приходятся 4–17% [2, 4, 10]. Неспецифичность клинической симптоматики и разнообразие причин мезаденита затрудняют диагностику; в этой связи для предотвращения тактических ошибок (процент необоснованных оперативных вмешательств при остром мезадените, по данным разных авторов, составляет 23,6–67,3%) от врача требуется четкое соблюдение дифференциально-диагностических алгоритмов и совершенствование врачебного мастерства [2–4, 9]. По сложившемуся на сегодняшний день в практической медицине мнению, клиническое обследование традиционными рутинными методами не позволяет установить правильный диагноз [3, 11]. Широкое внедрение инвазивных методик, лапароскопии в частности (inspectionem oculus), ускоряет и улучшает дифференциальную диагностику и уменьшает число неоправданных лапаротомий [1, 3, 7, 9, 11].
Анатомо-физиологические особенности кишечника у детей
Этиология мезаденита
В настоящее время этиология мезаденита до конца не изучена, однако состояние иммунной реактивности организма достоверно играет значительную роль в его развитии. Мезаденит не является самостоятельным заболеванием — многие болезни и реактивные состояния, формирующие вторичные генерализованные или регионарные лимфаденопатии, могут стать его клиническими масками. Среди них: инфекции — неспецифические (вирусные, бактериальные) и специфические (туберкулез, сифилис, туляремия), паразитарные (эхинококкоз, альвеококкоз), аутоиммунные (неспецифический язвенный колит, болезнь Крона) и онкогематологические болезни (лейкоз, лимфомы Ходжкина и неходжкинские), мезентериальные лимфаденопатии аллергического, токсического и медикаментозного происхождения (вызванные приемом цефалоспоринов, пенициллинов, сульфаниламидов, атенолола, каптоприла и других лекарств) [13]. В специальной литературе высказывается мнение о ведущей роли сенсибилизации в этиопатогенезе заболевания [2].
В практической деятельности врачи чаще встречаются с неспецифическим мезаденитом, вызванным преимущественно условными патогенами, обитающими в здоровом организме и проявляющими свои болезнетворные свойства при снижении иммунной защиты [14, 15]. Возбудителями мезаденита могут стать вирусы (аденовирусы, энтеровирусы, герпес-вирусы — цитомегаловирус [ЦМВ] и вирус Эпштейна — Барр [ВЭБ], вирусы кори, краснухи, парагриппа), бактерии (иерсинии, сальмонеллы, кампилобактерии, палочки кишечные и брюшного тифа, туляремии, токсоплазмы, хламидии, стафило- и стрептококки) [9, 10, 16]. Аденовирусы (серотипы 1, 2, 3, 5) и энтеровирусы группы Коксаки считают наиболее распространенными возбудителями мезаденита. В связи с высоким уровнем инфицирования населения (90–95%) велика роль ВЭБ — клиническая картина вызываемого им заболевания также характеризуется лимфопролиферативным синдромом [5]. Следует заметить, что репликация данных вирусов происходит медленно, высока способность к мутации, замедляющей ответную реакцию иммунитета, наблюдается длительная, часто пожизненная, персистенция их в лимфоидных тканях (небных миндалинах, аденоидах, лимфатических узлах) вследствие интеграции вирусного генома с геномом лимфоидных клеток и ускользания от системы противовирусной защиты. Таким образом, вирусы и бактерии, попадая в желудочно-кишечный тракт из верхних дыхательных путей с заглатываемой слизью, интенсивно размножаются в тонкой кишке, а при снижении иммунной резистентности патогенная микрофлора прорывается в регионарные лимфатические узлы. Помимо энтерального, возможно инфицирование мезентериальных лимфоузлов из различных первичных очагов инфекции (лимфогенным путем из кишки, аппендикса или гематогенным — из дыхательной системы). Развивающийся при инфицировании мезаденит знаменуется появлением клинических симптомов острого живота, диареи, увеличением печени и, реже, селезенки (30% заболевших). При вирусной этиологии заболевания одновременно отмечаются катаральные явления в носоглотке, конъюнктивит (односторонний на старте аденовирусной инфекции) и системная полиадения [8].
Диагностика мезаденита
С учетом наиболее распространенных этиологических факторов очевидно, что диагностика мезаденита нередко начинается с педиатрической консультации; большое значение имеет не только выяснение жалоб и осмотр больного ребенка, но и опрос родителей в отношении недавно перенесенных острых инфекций и известных диспансерных заболеваний. Вместе с тем важно помнить, что, несмотря на наличие общеинфекционного синдрома (тошнота, рвота или икота, жидкий стул или запор, повышение температуры тела до 38–39 ° С) и полиморфность клинических проявлений, доминирующим симптомом при мезадените всегда является внезапная абдоминальная боль, обусловленная рефлекторным раздражением нервных рецепторов брыжейки и спастическим сокращением кишечных петель вследствие воспалительного процесса в мезентериальных лимфатических узлах. Следует заметить, что при формировании гнойного мезаденита интенсивность боли уменьшается с одновременным нарастанием симптомов интоксикации; хронизация воспаления в лимфоузле отличается слабой болью без определенной локализации с усилением диспепсических расстройств. Любая абдоминальная боль вызывает подозрение на острую хирургическую патологию и требует экстренного осмотра пациента детским хирургом для исключения в первую очередь острого аппендицита [5–7, 11, 17–21]. Клиническая картина мезаденита часто напоминает острый аппендицит, тем не менее сложности диагностики связаны с необходимостью проведения дифференциального диагноза с целым рядом как хирургических (холецистит, дивертикулит, перекрут ножки кисты яичника, апоплексия яичника, новообразования), так и терапевтических заболеваний (панкреатит, почечная колика, колит, обострение язвенной болезни желудка и двенадцатиперстной кишки, аднексит, лимфогрануломатоз), сопровождающихся болями в животе [5, 17, 18, 21]. Боль при мезадените в зависимости от возраста ребенка может локализоваться около пупка или в правой подвздошной области, в верхней части живота или стать разлитой. Часто беспокоит умеренная тупая (ноющая), почти постоянная боль, реже — схваткообразная, усиливающаяся при перемене положения тела, движении и кашле. Болевой синдром при мезадените, как правило, нарастает более медленно, держится продолжительно, не стихая (в отличие от боли при аппендиците), — в течение 3–7 дней; очень редко самопроизвольно купируется.
При пальпации хирург выявляет у пациента характерные симптомы острого мезаденита: Мак-Фаддена (болезненность по краю прямой мышцы живота на 2–4 см ниже пупка), Клейна (миграция болевой точки справа налево при повороте больного со спины на левый бок), Штернберга (болезненность при пальпации по линии, соединяющей правую подвздошную область с левым подреберьем) [3, 9]. Учитывая наличие при мезадените боли преимущественно центральной локализации, а также неумение детей детализировать свои ощущения, детские хирурги в практической деятельности весьма редко оценивают эти симптомы. Важно знать, что характерными особенностями мезаденита являются повышенное газообразование в кишечнике и отсутствие местных перитонеальных знаков [3, 7]. Пальпация увеличенных лимфатических узлов в области корня брыжейки при выраженном метеоризме весьма затруднительна, однако при наличии конгломератов лимфоузлов может быть информативна. Бимануальное исследование (пальпация живота с одновременным ректальным пальцевым исследованием) в детской практике широко используется для оценки состояния органов малого таза. Однако, по мнению ведущих специалистов, причина абдоминальной боли у половины пациентов после первичного обследования так и остается невыясненной [6, 18, 22]. Следует заметить, что в дифференциальной диагностике абдоминальных болей, у детей в частности, очень важно динамическое наблюдение за пациентом.
Таким образом, на этапе дифференциально-диагностического поиска причин болей в животе высока ценность сопоставления совокупности клинических и лабораторных данных, однако на сегодняшний день основными в диагностике являются результаты неинвазивных и инвазивных инструментальных методов [1, 3]. По данным Е.Б. Ольховой [4], ультразвуковое исследование (УЗИ) пациентам с острыми абдоминальными болями выполняется в целях продолжения дифференциальной диагностики в случаях, когда клиническим обследованием диагноз острого аппендицита не подтвержден (85%), особенно при «атипичном» расположении отростка. Данный метод помогает провести дальнейший осмотр органов брюшной полости и забрюшинного пространства, исключая заболевания со схожей клинической симптоматикой: острый панкреатит, холецистит, пиелонефрит. УЗИ демонстрирует высокую чувствительность (74–92%) и специфичность (94–98%) в диагностике острого воспаления мезентериальных узлов [4, 5, 7, 10–22]. При мезадените визуализируются единичные или множественные брыжеечные лимфатические узлы (2–3 крупных с прилежащими многочисленными мелкими, часто в виде конгломерата), увеличенные в диаметре за счет воспалительного отека (в зависимости от возраста ребенка до 25–28 мм), неправильно-округлой формы с ровными, четкими контурами, с пониженной эхогенностью коркового слоя и повышенной — мозгового. Допплеровским исследованием в воспаленных лимфоузлах определяется усиленная васкуляризация. Отмечается повышенная пневматизация и усиленная перистальтика тонкой кишки с утолщением ее стенки и отеком брыжейки [4]. Выраженный метеоризм, особенно при госпитализации больного по экстренным показаниям, затрудняет визуализацию и снижает информативность УЗИ. Диагностические возможности могут быть расширены при использовании магнитно-резонансной томографии (МРТ) с 3-мерным моделированием, обладающей высокой разрешающей способностью. Исследование позволяет с абсолютной достоверностью получить полноценную информацию о местоположении, размерах, количестве и структуре пораженных лимфатических узлов, а также состоянии прилегающих органов забрюшинного пространства и малого таза [1, 17, 21].
Диагностическая лапароскопия, выполненная в условиях общей анестезии, признана сегодня наиболее точным методом дифференциальной диагностики причин абдоминальной боли, в т. ч. верификации диагноза «мезаденит» [1, 4, 5, 9, 13]. Лапароскопическая картина острого мезаденита обычно представлена увеличенными лимфатическими узлами плотной консистенции, гиперемированными, располагающимися конгломератом в непосредственной близости от первичного очага воспаления; брыжейка тонкой кишки отечна, гиперемирована и инфильтрирована. Во время диагностической лапароскопии проводится тщательная ревизия брюшной полости, одновременно возможна интраоперационная биопсия и экспресс-цитологическое исследование лимфатического узла, выпота брюшной полости (иммуноферментный анализ [ИФА], бактериологический посев). Гистологическая картина в измененных мезентериальных лимфоузлах соответствует острому воспалению: отек капсулы, интенсивная пролиферация лимфоцитов в корковом веществе, в мозговом — нарушение структуры тяжей с диффузной клеточной инфильтрацией лимфоцитами и макрофагами (реакция иммунокомпетентных клеток на инфекционный процесс) [1, 2].
Таким образом, рационально проведенный дифференциально-диагностический поиск причины абдоминальной боли с верификацией диагноза «острый мезаденит» дает возможность своевременно начать лечение, препятствуя развитию осложнений. Однако важно понимать, что исключение острой хирургической патологии, ведущее к ранней выписке домой, в отсутствие ясности этиологии болезни и, соответственно, без адекватно проведенной терапии, чревато развитием осложнений, рецидивами заболевания, а значит, и повторными госпитализациями [9].
Осложнения при мезадените встречаются редко
[1, 2, 14], могут быть локальными (гнойный мезаденит с деструкцией узла, абсцессы брюшной полости) или генерализованными, представляющими серьезную угрозу жизни пациента (разлитой перитонит с исходом в спаечную болезнь, кишечная непроходимость, сепсис, генерализованный лимфаденит).
Лечение острого неспецифического мезаденита
Лечение острого неспецифического мезаденита, как правило, консервативное, проводится в условиях хирургического стационара. Пациенту рекомендуется [1, 22] ограничение двигательной активности с организацией постельного режима до полного выздоровления, обильное питье и дробное щадящее питание. Знание этиологии заболевания оказывает существенную помощь в выборе тактики лечения: назначаются антибактериальные препараты, противовирусные средства и иммуностимуляторы, проводится обезболивающая (спазмолитики), дезинтоксикационная терапия. Широко применяются физиотерапевтические процедуры — магнитотерапия, УВЧ. Основой профилактики служит здоровый образ жизни, укрепление иммунитета, выявление и лечение хронических очагов воспаления, которые могут послужить источником развития мезаденита.
Цель исследования — проанализировать влияние особенностей клинической картины дебюта заболевания на сроки верификации диагноза «острый мезаденит» у детей.
Материал и методы
Проведен ретроспективный анализ историй болез-
ни 65 детей в возрасте от 1 года 6 мес. до 17 лет 9 мес., находившихся на лечении в хирургическом отделении многопрофильной скоропомощной ДГКБ св. Владимира в 2012–2017 гг. с основным клиническим диагнозом «острый мезаденит». Из анализа исключены дети, которым была проведена аппендэктомия и в ходе диагностического обследования был выявлен сопутствующий неспецифический мезаденит.
Результаты и их обсуждение
Средний возраст детей с мезаденитом составил 10,5 года (медиана и мода — 11 лет), 64,6% пациентов — мальчики (рис. 1).

Согласно данным, представленным на рисунке 1, заболеваемость мезаденитом детей в дошкольном возрасте была в 7,5 раза ниже, чем у школьников, причем наибольшая регистрировалась у детей младшего школьного возраста (7–12 лет) и составляла 49,2%.
Отмечена тенденция к увеличению заболеваемости детей мезаденитом в межсезонье и теплое время года (рис. 2), что коррелирует с эпидемиологией острых вирусных респираторных и кишечных инфекций, тропных к эпителию кишечника и лимфоидной ткани.

Все дети были доставлены в хирургический приемный покой скорой медицинской помощью, из них 60 детей (92,4%) направлены с диагнозом «острый аппендицит», 2 ребенка (3,1%) — с острым панкреатитом, по одному ребенку (1,5%) — с острым холециститом, кишечной непроходимостью, пиелонефритом (рис. 3).

Представляет интерес анализ сопутствующих диагнозов при госпитализации, которые были поставлены 24 детям (37%) из обсуждаемой группы: у 13 пациентов (20%), заболевших в весенне-летний период, при направлении в стационар по поводу абдоминальной боли одновременно имелись симптомы кишечной инфекции неясной этиологии (КИНЭ), пищевой токсикоинфекции, инфекционного гастродуоденита, у 6 из них при обследовании методом реакции пассивной гемагглютинации (РПГА) были выявлены антитела к инфекционным возбудителям (сальмонеллам, дизентерии Зонне и Флекснера, иерсиниям). Также 7 детей (10,8%) были направлены на госпитализацию с сопутствующим диагнозом «ОРВИ»; 2 ребенка (3,1%) — с диагнозом «острый пиелонефрит?» (у одного из них при обследовании в отделении обнаружена невысокая лейкоцитурия). Еще 2 детям (3,1%) при направлении на госпитализацию были поставлены сопутствующие гастроэнтерологические диагнозы:
«дискинезия желчевыводящих путей» (ДЖВП), «запор».
Поводом для обращения за медицинской помощью и направления в хирургический стационар у всех детей явилась абдоминальная боль. Как показано на рисунке 4, у 48 (73,8%) детей длительность боли в животе до госпитализации была не более суток (в среднем 6,5±0,6 ч, медиана и мода ряда 5 ч). В первые 6 ч от начала болевого синдрома были госпитализированы 66,7% пациентов (рис. 5); у этих детей отмечались выраженные клинические симптомы острого заболевания (боль, повторная рвота, частый стул, фебрильная температура), что требовало срочного обращения за квалифицированной медицинской помощью. Однако экстренность госпитализации не коррелировала с возрастом ребенка и в значительной степени зависела от внимания и тревожности родителей пациента. В то же время 11 детей (17%) с болью в животе оставались дома 2–3 сут, остальные были госпитализированы еще позднее, 5 из них — лишь на 6–7 сут болезни. Таким образом, причинами поздней госпитализации пациентов с мезаденитом являются медленное развитие, умеренная выраженность и неспецифичность симптомов, а также наличие «смазывающих» клиническую картину основного заболевания сопутствующих диспепсических расстройств при кишечных инфекциях или катаральных явлений в носоглотке при ОРВИ (диагноз наблюдения на участке часто формулируется как «ОРВИ с абдоминальным синдромом») [2, 4, 8].
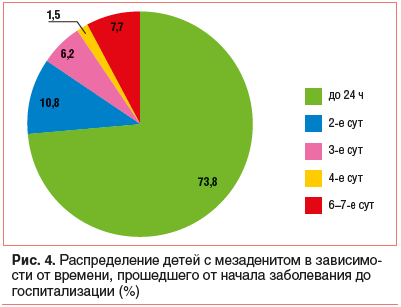

При поступлении (рис. 6) все дети жаловались на боль в животе (100%), у 25 детей (38,5%) наблюдалось повышение температуры тела (у 68% из них выше 38 ° C). Умеренно выраженный катаральный синдром отмечался у 7 детей (10,8%), что было отражено в направительном диагнозе. Диспепсические расстройства наблюдались у каждого второго пациента (47,8%): рвота 1–2 раза — у 26 пациентов (40%), у 3 детей — многократная (4–6 раз до поступления в стационар); 4 детей (6,2%) испытывали тошноту; жидкий стул 1–2 раза отмечали у 11 детей (16,9%), у 3 детей — более 5 раз; у 1 ребенка к моменту госпитализации наблюдался запор в течение 7 дней.
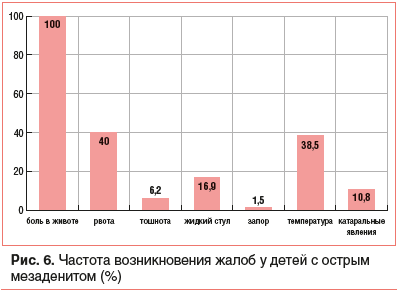
Жалобы на абдоминальные боли предъявляли все дети. Одна девочка в возрасте 11 лет с хроническим пиелонефритом в анамнезе и лейкоцитурией на момент госпитализации жаловалась также на боль в поясничной области. Практически у всех детей боль в животе носила умеренный ноющий характер, интенсивная схваткообразная боль была описана лишь у 3 пациентов (4,6%); боль возникала периодически, локализовалась преимущественно в околопупочной области. Интерпретация причин абдоминальной боли центральной локализации всегда сложна [18, 20]. Болевой синдром у детей до 3-летнего возраста (3 пациента — 1 год 6 мес., 1 год 8 мес., 2 года10 мес.) сопровождался беспокойством, громким плачем, внезапным пробуждением среди сна, рвотой, выраженным метеоризмом и яркой картиной ОРВИ. При этом диагнозы при госпитализации были разными: «острый аппендицит», «кишечная непроходимость», «острый пиелонефрит». Важно отметить, что лишь 2 из них поступили в стационар в первые сутки болезни.
При проведении мануального осмотра болезненность живота в околопупочной области с ее смещением при повороте на левый бок (что связано с натяжением брыжейки тонкой кишки) была выявлена у 57 пациентов (87,7%), реже отмечена болезненность по ходу корня брыжейки, поскольку глубокая пальпация доступна лишь у детей с астеническим типом конституции. Перитонеальных симптомов обнаружено не было или они были сомнительными. Бимануальная пальпация живота и прямой кишки позволила предположить апоплексию яичника у девочки в возрасте 12 лет, однако при проведении дальнейшего обследования данный диагноз не был подтвержден. В результате острый мезаденит заподозрен у 9 (13,8%) детей с абдоминальной болью при выявлении ведущего клинического симптомокомплекса: боль в центре живота и болезненность при пальпации увеличенных лимфоузлов в области корня брыжейки. Таким образом, несмотря на то, что большинство детей с острым мезаденитом были школьного возраста и умели достаточно четко детализировать характер и локализацию боли, установление диагноза по данным только клинического обследования является трудной задачей даже для опытного врача.
Клинический анализ крови, выполненный на старте обследования, не выявил существенных отклонений у 24,6% пациентов, у каждого третьего ребенка обнаружено повышение СОЭ (максимально до 44 мм/ч) и/или нейтрофильный лейкоцитоз (выше 8,8×10 9 /л, максимально до 28×10 9 /л), у 10,8% пациентов с выраженным палочкоядерным сдвигом лейкоцитарной формулы (максимально до 28%); моноцитоз (19%) без атипичных мононуклеаров отмечен у 1 ребенка (однако в дальнейшем антитела к ВЭБ не были обнаружены); повышение уровня эозинофилов до 7–8% регистрировали у 3 детей, при выписке им рекомендовано обследование на гельминтозы. Отклонения в биохимическом анализе крови обнаружены у 9 детей (15%): повышенный уровень СРБ (максимально до 65,6 мг/л), билирубина за счет непрямой фракции (1 ребенок страдал болезнью Жильбера), увеличение активности АСТ (до 55 Ед/л), щелочной фосфатазы (до 448 Ед/л) и амилазы (у 3 детей с яркими гастроэнтерологическими симптомами — до 102 Ед/л). Серологические исследования (РПГА со специфическими диагностикумами) выявили положительные пробы у 6 пациентов: на сальмонеллез (1:100, 1:400), дизентерию Флекснера и Зонне (1:100), иерсиниоз (1:800). Изменения в анализах мочи обнаружены у 11 (16,9%) больных, 9 из них были девочки: лейкоцитурия (до 80 лейкоцитов в поле зрения) у пациентов с пиелонефритом и КИНЭ; изолированная протеинурия (до 0,16 г/л), кетоновые тела. Исследование мочи оказалось весьма информативным для дифференциальной диагностики причин болевого синдрома и выявления сопутствующей патологии.
На этапе дифференциальной диагностики причин абдоминальной боли выполнено УЗИ брюшной полости: у 58 из 60 детей, госпитализированных с направительным диагнозом «острый аппендицит», данное заболевание исключили; у 2 пациентов были обнаружены УЗ-признаки воспаления аппендикулярного отростка, однако диссоциация данных с динамикой клинических симптомов потребовала продолжения обследования. Направительные диагнозы 5 пациентов, госпитализированных с подозрением на кишечную непроходимость, холецистит, панкреатит, пиелонефрит, окончательно сняты на основании совокупности данных, полученных при динамическом клиническом наблюдении, и результатов лабораторного обследования и УЗИ. Воспалительная трансформация мезентериальных лимфоузлов визуализировалась у 31 пациента (47,7%); у 6 (9,2%) детей патологических изменений в брюшной полости не было обнаружено. УЗ-признаки гастроэнтерологической патологии, выявленные у 73,8% пациентов в виде гастродуоденита, энтерита, диффузных изменений поджелудочной железы реактивного характера, ДЖВП, стеатогепатоза (редко), регистрировались изолированно (43,1%) или одновременно с признаками мезентериального лимфаденита. Реже обнаруживались иные патологические отклонения: УЗ-признаки острого цистита — у 1 больного; у 3 детей разного возраста, госпитализированных в первые 6–8 ч от начала появления абдоминальной боли, был выявлен лишь выраженный метеоризм, по поводу чего двум из них дополнительно выполнили обзорную рентгенографию брюшной полости. У пациентки с подозрением на апоплексию яичника результаты УЗИ позволили исключить данный диагноз.
После исключения диагноза «острый аппендицит» 4 пациентам с гастроэнтерологическими заболеваниями в анамнезе, у которых боль усиливалась на фоне целенаправленной терапии, была выполнена диагностическая эзофагогастродуоденоскопия (ЭГДС). Были обнаружены признаки гастроэзофагеальной рефлюксной болезни (катаральный эзофагит), катаральный гастродуоденит, эрозивный дуоденит. Таким образом, УЗИ дает широкие возможности ревизии брюшной полости, малого таза и забрюшинного пространства, что позволило исключить диагноз острого аппендицита пациентам с абдоминальными болями в день госпитализации, выявить сопутствующую патологию пищеварительной, мочевыделительной, генитальной систем и верифицировать диагноз мезаденита у половины пациентов. Верификация диагноза «острый мезаденит» была закончена на этапе данных клинического исследования и УЗИ у 13 детей — у них отмечали клиническую картину манифестной (преимущественно кишечной) инфекции, во всех случаях результаты исследований и динамического наблюдения за пациентами не вызывали сомнений в диагнозе.
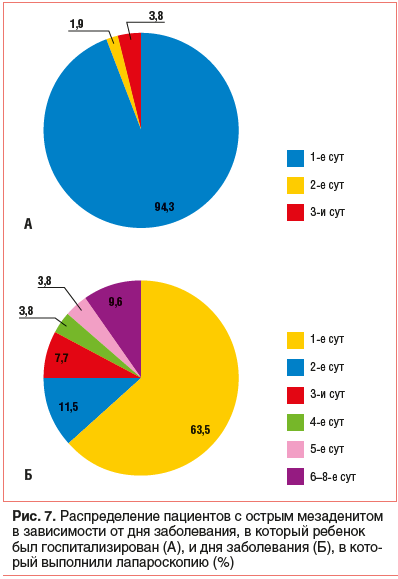
В продолжение дифференциальной диагностики 52 (80%) детям выполнили диагностическую лапароскопию, причем в 94,3% случаев — в день госпитализации; только 3 пациента (5,7%) были обследованы на 2–3 сут (рис. 7А). Явления острого мезаденита обнаружили у 98,1% пациентов. Интересно, что у 1 ребенка с 2-дневной абдоминальной болью без симптомов инфекционной патологии эндоскопических признаков воспаления мезентериальных узлов не выявили, однако на УЗИ визуализировались увеличенные брыжеечные лимфатические узлы пониженной эхогенности с усилением сосудистого кровотока при допплеровском исследовании, что дало основание выставить окончательный клинический диагноз «острый мезаденит». Учитывая влияние срока заболевания на характер эндоскопической картины мезаденита, мы проанализировали время выполнения диагностической лапароскопии в зависимости от начала абдоминальной боли (рис. 7Б). Заметим, что у 9,2% детей к моменту госпитализации давность заболевания уже составляла 4–7 дней. Как показано на рисунке 7Б, независимо от сроков госпитализации от начала заболевания и несмотря на затраты времени на выполнение лабораторно-инструментального этапа диагностического поиска, 75% больным лапароскопия выполнена не позднее вторых суток пребывания в стационаре. Однако 9 (17,3%) детей с абдоминальной болью ждали окончательной верификации диагноза 4–8 сут, и следует заметить, что эти показатели, к сожалению, напрямую зависят от быстроты обращения родителей больного ребенка за врачебной, а главное — за специализированной хирургической помощью.
Представляет практический интерес динамика основного диагноза в процессе обследования ребенка с абдоминальной болью (рис. 8).
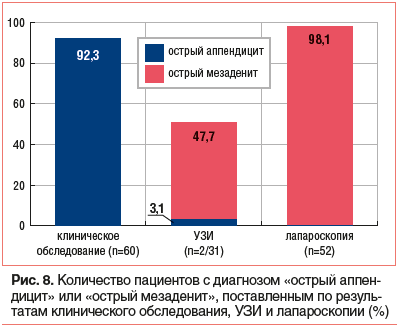
На рисунке 8 продемонстрировано кардинальное изменение представлений о причине боли в животе в процессе дифференциально-диагностического поиска при воспалении мезентериальных узлов: от диагноза «острый аппендицит», выставленного на основании клинико-анамнестических данных при направлении в стационар 60 больным из 65, к диагнозу «острый мезаденит» на этапе УЗИ —
31 пациент из 65 (и «острый аппендицит» у 2 детей) и к заключительному диагнозу при лапароскопическом исследовании — «острый мезаденит» у 51 ребенка из 52 обследованных.
После окончательной верификации диагноза 58 (89,2%) пациентам проводили антибактериальное лечение. Монотерапию цефалоспоринами II–III поколений получали 30 детей из 58 (51,7%), кроме того, проводилась терапия цефалоспоринами II–III поколений в комбинации с аминогликозидами (41,4%) и/или нитрофурановыми препаратами (17,2%) в зависимости от клинико-лабораторной картины (кишечными или уросептиками). В то же время 7 пациентов (7–14 лет) с абдоминальными болями на фоне симптомов КИНЭ или ОРВИ, продемонстрировавших быструю положительную клиническую динамику в процессе наблюдения и не имевших отклонений в анализах крови и мочи, антибактериальную терапию не получали. В комплексной терапии широко использовались биопрепараты, воздействующие на микробную флору кишечника (64,6%), антигистаминные средства (32,3%), редко — ферментные препараты (13,8%), обволакивающие (9,2%), спазмолитики (3,1%).
Длительность пребывания в хирургическом стационаре пациентов с острым мезаденитом составила в среднем 7 дней (7±0,3; медиана и мода ряда 6 дней), что, по сути, соответствует продолжительности периода времени, потраченного на диагностику заболевания и купирование болевого синдрома. Из хирургического отделения все дети были выписаны домой с улучшением, в удовлетворительном состоянии, с рекомендациями по дальнейшему лечению и наблюдению. Лечащему врачу следует информировать родителей, ориентированных в своих ожиданиях преимущественно на купирование болевого синдрома, что при первичном неспецифическом мезадените реконвалесценция может происходить медленно, что требует длительного соблюдения щадящего режима [1, 2, 10, 20]. Заметим, что ни единого эпизода повторной госпитализации с рецидивом мезаденита наблюдавшихся нами детей в наш стационар не зарегистрировано, что подтверждает приоритетную роль распространенных респираторных и кишечных инфекций (не склонных к персистенции и хронизации) в развитии неспецифического воспаления мезентериальных лимфоузлов.
Заключение
Таким образом, острый неспецифический мезаденит постоянно находится в зоне внимания педиатра, поскольку дети с абдоминальной болью обращаются к детскому врачу как к первому доступному специалисту, а при исключении острой абдоминальной патологии вновь возвращаются от хирурга к педиатру для продолжения дифференциально-диагностического поиска терапевтических и инфекционных причин заболевания, его лечения и профилактики новых обострений.
Дифференциальная диагностика абдоминальной боли у детей базируется на исключении в первую очередь жизнеугрожающих хирургических заболеваний брюшной полости, требующих экстренного оперативного вмешательства: острого аппендицита, дивертикулита, холецистита, ЖКБ, кишечной непроходимости, абсцесса, перекрута придатков матки или ножки кисты яичника. Затем исключаются инфекционные болезни, несущие эпидемиологическую опасность для близкого окружения больного (ОРВИ, сальмонеллез, иерсиниоз, дизентерия); далее продолжается поиск среди терапевтических заболеваний, сопровождающихся болями в животе: патологии желудочно-кишечного тракта (гастрит, ДЖВП, панкреатит), почек (пиелонефрит, гломерулонефрит), половой сферы (аднексит в подростковом возрасте). Выявление первичной причины заболевания может потребовать перевода в профильное (нефрологическое, гастроэнтерологическое, инфекционное) отделение для дальнейшей реабилитации пациента.
Проведенное нами ретроспективное исследование показало наибольшую частоту заболевания мезаденитом у младших школьников, что коррелирует с возрастающей инфекционной нагрузкой в этом возрасте. Анализ клинической картины показал, что чем ярче и острее симптомы мезаденита, тем быстрее пациент попадает в поле зрения специалиста: 2/3 пациентов с данным диагнозом госпитализируются в первые 6 ч заболевания, однако каждый десятый ребенок направляется в стационар после 4–7 дней страдания, что напрямую зависит от трактовки врачом и родителями катарально-диспепсических симптомов на старте заболевания у ребенка с абдоминальной болью. Отсутствие патогномоничных жалоб и симптомов, полиморфность клинической картины, относительная редкость и неспецифичность сдвигов в показателях традиционных лабораторных тестов (отражающих в основном интоксикационный синдром и/или фоновую соматическую патологию) не позволяют установить точный диагноз без помощи дополнительных исследований.
В настоящее время совершенствование методов диагностики мезаденита перспективно лишь в области инструментальных исследований (УЗИ, лапароскопия). Являясь неинвазивным методом оценки состояния практически всех анатомических структур и функций органов брюшной полости, УЗИ имеет высокую эффективность на всех этапах дифференциально-диагностического поиска, что, безусловно, базируется на знаниях врачей и опыте применения технических приемов сканирования у детей. Диагностическая лапароскопия в большинстве случав выполняется пациентам в первые сутки госпитализации (75%) вслед за УЗИ и, обладая максимальной информативностью (98%), позволяет с высокой точностью провести ревизию брюшной полости ad oculus [4, 9, 21]. Однако каждому шестому ребенку с абдоминальной болью окончательный диагноз был верифицирован лишь на 4–8 сут, что могло привести к серьезным осложнениям. Следует заметить, что ультразвуковая и эндоскопическая картина коррелирует со сроками заболевания. По мере стихания остроты воспалительного процесса редукция лимфоузлов происходит медленно — в течение недель или месяцев.
Установление этиологического фактора, вызвавшего развитие мезаденита, помогает определить дальнейшую тактику ведения пациента. На вероятный этиологический фактор могут указать клиническая симптоматика и сезонная эпидемиология. К сожалению, серологическая диагностика вирусных инфекций в хирургических отделениях не используется в должной мере, напротив, широко внедрены тесты обнаружения бактериальных кишечных инфекций, однако в итоге врач не обладает знанием полного спектра необходимых для исключения инфекционных причин.
Вопрос применения при остром мезадените противовирусных средств и иммуномодуляторов остается открытым. Однако с учетом высокой частоты вирусных инфекций с лимфопролиферативной индукцией у пациентов в преддверии развития неспецифического мезаденита очевидна актуальность их назначения. Требует внимания факт медленной элиминации инфектов и длительной их персистенции, способствующих рецидивам заболевания при снижении иммунной резистентности. В этой связи противовирусная терапия может внести принципиальный вклад в профилактику рецидивирования мезаденитов. Таким образом, острый мезаденит является междисциплинарной проблемой педиатрии и детской хирургии, когда последовательные совместные усилия специалистов могут ускорить оказание специализированной помощи ребенку.
Выводы
Пациентам с прогрессирующей абдоминальной болью всегда необходима консультация хирурга для исключения острых хирургических заболеваний.
Острый мезаденит не имеет специфической клиники и часто маскируется под острую инфекцию (респираторную, кишечную) или обострение диспансерной патологии.
Для полной верификации диагноза острого мезаденита необходимы инструментальные исследования: УЗИ органов брюшной полости, забрюшинного пространства и малого таза, диагностическая лапароскопия, МРТ.
Серологические исследования ценны в установлении этиологии мезаденита и выборе комплексного лечения заболевания. Целесообразно расширение алгоритма диагностического поиска среди вирусных инфекций, индуцирующих лимфоидную пролиферацию.
Противовирусная терапия рассматривается в остром периоде мезаденита с целью снижения тяжести и сокращения сроков заболевания, а также рекомендуется пациентам при выписке для профилактики рецидива при доказанной персистирующей инфекции.
Только для зарегистрированных пользователей