Медикаментозное прерывание малых сроков беременности
Одной из наиболее важных проблем современного здравоохранения является сохранение репродуктивного здоровья женщин. Столь пристальное внимание к этой проблеме связано, в первую очередь, с демографической ситуацией, сложившейся в России. Предпринимаемые ме
Одной из наиболее важных проблем современного здравоохранения является сохранение репродуктивного здоровья женщин. Столь пристальное внимание к этой проблеме связано, в первую очередь, с демографической ситуацией, сложившейся в России. Предпринимаемые меры, к сожалению, не повышают рождаемость в нашей стране на должный уровень. Основным путем решения проблемы сохранения детородной функции женщин являются уменьшение числа медицинских и криминальных абортов, профилактика нежелательной беременности.
В Российской Федерации аборт продолжает оставаться распространенным методом регулирования рождаемости и планирования семьи (В. И. Кулаков, 1993). По данным медицинской статистики, ежегодно около 15—20 тыс. женщин прерывают беременность. До последнего десятилетия применялись хирургические методы прерывания беременности, такие, как вакуум-кюретаж, вакуум-аспирация («мини-аборт») и традиционный кюретаж.
Вакуум-кюретаж — наиболее распространенный метод искусственного прерывания беременности во многих странах мира, в том числе и в России. Преимуществами этой процедуры являются простота и непродолжительность процедуры полной эвакуации содержимого полости матки через небольшое расширение шейки матки. Операция легко выполнима под местной анестезией в амбулаторных условиях.
При применении указанного метода прерывания беременности возможны аллергические реакции на используемые лекарственные препараты, перфорация или атония матки, судороги или остановка сердца и т. д.
Искусственное прерывание беременности методом вакуум-аспирации в целях регулирования рождаемости приобрело большое распространение во многих странах мира. Широкое применение этого метода обусловлено тем, что проведение операции возможно в амбулаторных условиях при помощи относительно простой медицинской техники, при соблюдении правил асептики и антисептики, без применения местной анестезии. После операции пациенты возвращаются к обычной жизнедеятельности через 1 ч. Несмотря на преимущество данного метода, некоторую сложность представляют диагностирование начальных сроков беременности и исключение внематочной беременности.
Традиционный кюретаж представляет собой операцию искусственного прерывания беременности, которая в настоящее время используется все реже. Медицинский аборт часто приводит к серьезным осложнениям в раннем послеоперационном периоде (кровотечение, инфекция, остатки плодного яйца и т. д.). В более поздние сроки развиваются воспалительные заболевания женских половых органов, невынашивание беременности, бесплодие, внематочная беременность. Осложненное течение последующей беременности, родов и послеродового периода (В. И. Кулаков и соавт., 1991; Т. Н. Мельник и соавт., 2001) неблагоприятно влияет на состояние плода и новорожденного (Т. С. Чередниченко, 2001).
Среди современных щадящих способов прерывания незапланированной беременности можно упомянуть медикаментозный метод. Его разработка началась еще в 70-е гг. ХХ столетия. В этот период во Франции была реализована программа создания стероидов с антигормональным действием. В 1980 г. появился мифепристон, представляющий собой синтетический стероидный препарат для перорального применения и являющийся антагонистом прогестерона и глюкокортикоидов.
Медикаментозный метод прерывания незапланированной беременности с помощью препарата мифепристон (мифегин, пенкрофтон) применяется за рубежом с 1980 г., а в России — с 1998 г. (Е. Н. Караева и соавт., 1999).
Мифепристон (мифегин, пенкрофтон, мифепрекс) — синтетическое стероидное антипрогестогенное средство (блокирует действие прогестерона на уровне рецепторов). Механизм действия препарата основан на взаимодействии с гормонсвязывающим доменом рецептора клеток-мишеней, что вызывает «неэффективную» конформацию и блокаду эффектов природного стероида.
Мифепристон повышает сократительную способность миометрия, стимулируя высвобождение интерлей- кина-8 в хориодецидуальных клетках, повышая чувствительность миометрия к простагландинам (для усиления эффекта применяется в сочетании с синтетическими аналогами простагландинов (Е. Н. Караева и соавт., 1999)). В результате действия препарата происходят десквамация децидуальной оболочки и выведение плодного яйца.
После однократного приема внутрь 600 мг мифепристона максимальная концентрация достигается через 1,5 ч. Абсолютная биодоступность препарата составляет 69%. В плазме крови мифепристон на 98% связывается с белками: альбумином и кислым альфа-1-гликопротеином. После фазы распределения выведение сначала происходит медленно, концентрация уменьшается в 2 раза между 12—72 ч, затем процесс выведения ускоряется. Период полувыведения составляет 18 ч.
При патоморфологическом исследовании материала выкидышей (Т. Н. Мельник и соавт., 2001) после применения мифепристона обнаружили, что линия отторжения формирующейся плаценты проходила по терминальным окончаниям якорных ворсин и остаточным фрагментам базальной оболочки, состоящей из пластов цитотрофобласта и децидуальных клеток. В полости эмбрионального мешка обнаруживались сохраненные фрагменты эмбриона, амниотической оболочки и желточного мешка. Отмечалось полное соответствие строения ворсин, а также стенки эмбрионального мешка, что объяснялось небольшим сроком от момента приема препарата до отторжения эмбрионального мешка. Непосредственный механизм отторжения заключался в формировании гематомы в толще базальной пластинки с переходом ее в близлежащее межворсинчатое пространство. Местный характер геморрагических нарушений (на границе эндо- и миометрия), их острое возникновение и кратковременность процесса не создавали предпосылок для выброса тромбопластических масс и, следовательно, для изменения гемостазиологических параметров крови, что подтверждалось исследованием свертывающей системы крови.
Показанием к применению мифепристона (мифегина, пенкрофтона) в настоящее время является прерывание маточной беременности на ранних сроках (42 дня аменореи). Однако имеются исследования (Р. А. Хетчер, 1993; Р. А. Манушарова, Э. И. Черкезова, 2002), в ходе которых эти препараты применяли до 9-недельного срока беременности. Кроме того, данные литературы свидетельствуют об эффективности использования мифепристона для подготовки и индукции родов при доношенной беременности. В настоящее время мифепристон применяется во Франции, США, Швеции, Китае, России, Великобритании, Индии и других странах.
Противопоказаниями к назначению препарата являются: наличие в анамнезе повышенной чувствительности к мифепристону, надпочечниковая недостаточность и длительная глюкокортикостероидная терапия, острая или хроническая почечная и/или печеночная недостаточность, порфирия, миома матки, наличие рубца на матке, анемия, нарушения гемостаза (в том числе в результате предшествующего лечения антикоагулянтами), воспалительные заболевания женских половых органов, наличие тяжелой экстрагенитальной патологии. Нельзя применять мифепристон у курящих женщин старше 35 лет без предварительной консультации терапевта. Кроме того, противопоказаниями к применению препарата с целью прерывания беременности являются подозрение на внематочную беременность; беременность, не подтвержденная клиническими исследованиями; превышающая по сроку 42 дня после прекращения менструации; возникшая на фоне применения внутриматочной контрацепции или после отмены гормональной контрацепции.
С осторожностью следует назначать препарат при хронических обструктивных заболеваниях легких (в том числе при бронхиальной астме), тяжелой артериальной гипертензии, нарушениях ритма сердца и сердечной недостаточности. Пациенткам с искусственными сердечными клапанами или инфекционным эндокардитом при применении мифепристона следует проводить профилактическое лечение антибиотиками.
Грудное вскармливание после приема мифепристона следует прекратить на 14 дней. Применение этого препарата требует проведения всех подготовительных мероприятий, связанных с абортом.
Среди побочных действий, связанных с процедурой прерывания, следует отметить: кровянистые выделения из половых путей, боли в низу живота, обострение воспалительных процессов матки и придатков.
Побочные действия, связанные с приемом мифепристона, — чувство дискомфорта в низу живота, слабость, головная боль, тошнота и рвота, головокружение, гипертермия. Прием мифепристона в дозе до 2 г не вызывает нежелательных реакций. В случаях передозировки препарата может наблюдаться надпочечниковая недостаточность.
При проведении медикаментозного аборта с помощью препарата мифепристон следует избегать назначения нестероидных противовоспалительных средств, так как они ослабляют его эффективность. Если на 10–14-й день эффект от применения препарата отсутствует, беременность обязательно следует прервать иным способом, поскольку возможно формирование врожденных пороков развития у плода.
Исследования, проводившиеся еще в 80-х гг., показали, что эффективность изолированного применения мифепристона составляет 85%. Поэтому впоследствии было предложено мифепристон сочетать с простагландинами. По данным литературы, эффективность указанной комбинации достигает 96—98% (Р. А. Манушарова, Э. И. Черкезова, 2002). Также было показано, что эффективность комбинированного применения мифепристона (в дозе 400 мг) и сайтотека (800 мкг) равна 96%.
Под нашим наблюдением находились 200 женщин в возрасте от 18 до 41 года (36,7+2,3 года). У 37 из них беременность была первой; 28 прерывали вторую беременность (первая закончилась искусственным абортом), остальные имели в анамнезе роды (37) или роды и аборты (98). По данным гинекологического осмотра и УЗИ, гестационный срок в среднем составил 5,2±0,2 недели при среднем диаметре плодного яйца 10,5+0,5 мм.
Гинекологические заболевания имелись у 42,1% пациенток (бессимптомная миома матки небольших размеров — 4,1%; эрозия шейки матки — 20,9%; хронические аднекситы — 15%; параовариальная киста — 4%; дисфункции яичников — 5%; генитальный эндометриоз — 3,1%).
Мифегин назначали однократно в виде таблеток в дозе 600 мг (3 табл. по 200 мг), а через 36—48 ч пациентки принимали простагландин — мизопростол (сайтотек) в дозе 400 мкг (2 табл. по 200 мкг) и спустя 3 ч — еще 400 мкг (2 табл.). Препараты принимались в присутствии врача после получения согласия пациентки. Наблюдение осуществлялось в течение 2-3 ч, после чего женщины могли покинуть лечебное учреждение, получив необходимые рекомендации. Трудоспособность при этом сохранялась полностью.
Эффективность метода оценивалась на основании констатации положительного исхода, подтвержденного данными объективного исследования, бимануального исследования, УЗИ (отсутствие плодного яйца, а также его элементов в полости матки на 10—14-й день).
Экспульсия плодного яйца у 180 из 200 женщин произошла после комбинированного применения мифегина и сайтотека, у 11 пациенток — без дополнительного приема сайтотека. У 9 пациенток со сроком беременности 8,5-9 нед. через 12—24 ч после приема мифегина наблюдалось кровотечение из половых путей, по поводу чего они были госпитализированы и было произведено выскабливание слизистой полости матки. Экспульсия плодного яйца произошла в первые сутки после приема сайтотека — у 95,3%, на вторые сутки — у 4,7% женщин. Клинически это проявлялось кровянистыми выделениями из половых путей (скудных или умеренной интенсивности) в первые сутки после приема мифегина — у 38% женщин; у 62% пациенток в первые сутки после приема мифегина не отмечено появления кровянистых выделений из половых путей. Спустя 40–55 мин после приема сайтотека кровянистые выделения из половых путей усиливались у подавляющего большинства женщин и в 60% случаев сопровождались схваткообразными болями в низу живота и экспульсией плодного яйца.
Продолжительность кровянистых выделений составляла в большинстве случаев от 7 до 14 дней. У 4 пациенток наблюдались скудные кровянистые выделения до 15—17 дней. Кровотечения, потребовавшие проведения консервативной терапии в течение 1-2 дней (дицинон, аскорутин, викасол), были отмечены у 3 пациенток. Хирургического вмешательства с целью гемостаза не потребовалось ни в одном наблюдении. Следует отметить, что выраженные схваткообразные боли в низу живота наблюдались у нерожавших женщин, а у рожавших пациенток они были выражены слабо или отсутствовали. Купировали схваткообразные боли в низу живота пероральным приемом или парентеральным введением спазмолитических (но-шпа) или анальгетических (анальгин, баралгин) средств.
Положительного результата приема после мифегина нам не удалось добиться в 3 случаях. По данным УЗИ, было зафиксировано наличие остатков плодного яйца в полости матки, по поводу чего пациенткам было проведено диагностическое выскабливание. Следует отметить, что у этих женщин в анамнезе имелся эндометрит. По-видимому, отсутствие достаточного эффекта в данных случаях обусловлено нарушением сократительной способности матки.
Переносимость мифегина была хорошей. При приеме сайтотека у 8 женщин отмечены побочные эффекты(в виде тошноты, рвоты, головокружения, головной боли), которые продолжались в течение 30—45 мин от начала приема препарата и проходили самостоятельно.
Контрольные УЗИ, выполненные на 10—14-е сутки после экспульсии плодного яйца, показали нормальное состояние эндометрия у 187 женщин. У 3 пациенток отмечалось расширение М-ЭХО при наличии гипоэхогенного содержимого. В одном наблюдении выявлены неоднородность М-ЭХО и эхонегативные включения. Этим женщинам дополнительно назначался дюфастон в дозе 10 мг 2 раза в сутки в течение 10 дней и после очередной менструации проводилось дополнительное УЗИ. Во всех случаях было установлено нормальное состояние М-ЭХО при контрольном УЗИ.
Таким образом, результаты проведенного исследования свидетельствуют о том, что комбинированное применение препаратов мифегин (мифепристон) и сайтотек является высокоэффективным средством для прерывания нежелательной беременности. При строгом соблюдении всех необходимых требований этот способ хорошо переносится женщинами, не имеет существенных побочных эффектов и может применяться для прерывания беременности на малых сроках (до 7 нед.). Применение мифегина не вызывает нарушения менструального цикла, вероятность влияния на репродуктивную функцию практически равна нулю.
Медикаментозное прерывание беременности почти полностью исключает риск возникновения восходящей инфекции и связанных с ней осложнений. Кроме того, при данном методе прерывания беременности отсутствует психогенная травма, чаще всего сопровождающая традиционный артифициальный аборт, что повышает качество жизни женщины.
По вопросам литературы обращайтесь в редакцию.
Р. А. Манушарова, доктор медицинских наук, профессор
Э. И. Черкезова
РМАПО, Клиника андрологии, Москва
Без антибиотиков здесь не обойтись. Инфекционные осложнения при искусственном прерывании беременности — вызов современной медицине
Опубликовано в :
Status Praesens. Гинекология, акушерство, бесплодный брак / №5 [16]
Галина Борисовна Дикке, докт. мед. наук,
проф. кафедры акушерства, гинекологии и репродуктивной медицины ФПК МР РУДН (Москва)
Оцифрованная опасность
Другой хирургический | АБОРТЫ В МИРЕ И В РОССИИ (НА 1000 ЖЕНЩИН ФЕРТИЛЬНОГО ВОЗРАСТА) 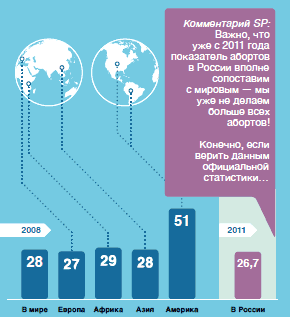 |
Prognosis pessima: летальность
Резюмируя, важно отметить, что уровень летальности при безопасных абортах (выполненных в медицинских учреждениях) существенно ниже, чем при небезопасных (внебольничных и криминальных). Даже при самом низком уровне небезопасных абортов (Восточная Европа) материнская смертность после аборта составляет 30 случаев, что в 40 раз выше, чем в США.
При увеличении срока беременности на каждые 2 нед риск материнской смертности увеличивается в 2 раза независимо от метода. | ИНФЕКЦИОННОЕ ОСЛОЖНЕНИЕ АБОРТА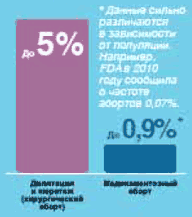 |
Засланные агенты
Табл. Лихорадка при медикаментозном аборте: дифдиагноз
| Симптомы | Побочное действие мизопростола | Инфекция |
| Время возникновения | В течение первых часов после приёма | Через 8 ч и более после приёма мизопростола |
| Продолжительность | 2-3 ч | Постоянная на протяжении нескольких дней |
| Степень гипертермии | Субфебрильная (37,0-37,8°С) | 38°С и выше |
| Купирование | Самостоятельно без использования лекарственных препаратов | |
| Необходимы медикаменты | Частота 4-37% | 0,09-0,5% |
Таким образом, можно сделать вывод о том, что перед осуществлением аборта крайне важно диагностировать уже имеющуюся инфекцию и провести соответствующие профилактические мероприятия.
| Умерла от сепсиса после медаборта В официальной структуре материнской смертности о летальных исходах после медикаментозного прерывания беременности сообщений нет1. И всё же один клинический случай, наступивший в подобных условиях, известен (в статистике отнесён на счёт сепсиса). Ретроспективно было выяснено, что в период между днём приёма мизопростола и поступлением в стационар больная отмечала наличие субфебрильной температуры тела, слабости, недомогания и связывала это состояние с ОРВИ, которым она «заразилась» от своего ребёнка. Дальнейший анализ документации показал, что развитие септического состояния у пациентки Ш. могло произойти вследствие гематогенного инфицирования из очагов хронической инфекции (хронический пиелонефрит, хронический тонзиллит), вызванной стафилококком и гемолитическим стрептококком, на фоне сниженного иммунитета и общих защитных сил организма (указание на наличие аллергической реакции и, возможно, влияние вирусной инфекции от контакта с больным ребёнком). Скорее всего данный случай следует рассматривать как трагическое стечение обстоятельств: совокупности клинических особенностей соматического статуса пациентки (наличие очагов хронической инфекции и снижение защитных сил организма) и внешних факторов, приведших к инфицированию матки и дальнейшему прогрессированию инфекционного процесса, имеющего молниеносный характер течения. Однако видны и ошибки. В частности, лечащий врач не назначил пациентке антибиотикопрофилактику, хотя анамнез требовал особого внимания к этому вопросу. Кроме того, женщина не была информирована о необходимости срочного обращения к врачу при появлении «тревожных» симптомов, свидетельствующих о развитии инфекционного процесса. Подводные камни диагностики Инфекционные осложнения после аборта, выполненного любым методом, обычно диагностируют на основании клинической картины. Среди симптомов выделяют следующие: боль в области малого таза, кровотечение, лихорадку, болезненную матку (пальпаторно нормальную или мягковатую), влагалищные выделения с запахом. По данным УЗИ полость матки может быть свободна от тканей гестации или определяют наличие остатков. В связи с тем, что мизопростол, используемый для медикаментозного аборта, повышает температуру тела, необходимо дифференцировать лихорадку, связанную с действием простагландинов, от лихорадки, вызванной инфицированием матки. При первых же признаках пациентку следует госпитализировать в стационар и провести полный комплекс лечения, включающий антибактериальную, трансфузионную и другие виды терапии в соответствии с принципами лечения тазовых инфекций. При инфицировании на фоне остатков тканей гестации показана вакуумная аспирация. Подумать заранее |  |
Что, когда, кому и сколько?
Табл. Профилактика инфекционных осложнений при прерывании беременности, RCOG (2011) 16
| Для женщин, не обследованных на ИППП |
| Азитромицин 1 г внутрь в день аборта, а также метронидазол 1 г ректально или 800 мг внутрь до или во время аборта или |
| Доксициклин 100 мг перорально 2 раза в день в течение 7 дней начиная со дня аборта, а также метронидазол 1 г ректально или 800 мг перорально до или во время аборта |
| Для женщин, у которых не выявлено хламидийной инфекции |
| Метронидазол 1 г ректально или 800 мг внутрь до или во время аборта |
| При баквагинозе, независимо от наличия клинической картины, следует провести санацию, отдавая предпочтение местным антибактериальным средствам. Библиографию см. StatusPraesens на с. 94-95. 1. Основные показатели здоровья матери и ребенка, деятельность службы охраны 2. Tang O.S., Chan C.C., Ng E.H., Lee S.W., Ho P.C. A prospective, randomized, placebo- 3. Ранние сроки беременности. Изд. 2-е, испр. и доп. / под ред. В.Е. Радзинского, 4. Хамошина М.Б., Лебедева М.Г., Руднева О.Д., Архипова М.П., Зулумян Т.Н. 5. Хрянин А.А., Стецюк О.У., Андреева И.В. Хламидийная инфекция в гинекологии и 6. Дикке Г.Б., Яроцкая Е.Л., Ерофеева Л.В. Стратегическая оценка политики, программ 7. Тихомиров А.Л., Батаева А.Е. Лучше поздно, чем никогда // Русский медицинский 8. Infection and ectopic pregnancy in medical abortion. Unpublished data. The Population 9. Prevention of infection after induced abortion. Clinical Guidelines. Release date October 10. Lichtenberg E.S., Paul M. Surgical abortion prior to 7 weeks of gestation // 11. Осложнения при аборте. Руководство по техническим и управленческим 12. Сухих Г.Т., Яроцкая Е.Л. Стратегический подход к решению проблемы 13. Bartlett L.A., Berg C.J., Shulman H.B. et al. Risk factors for legal induced abortion-related 15. Fjerstad M., Trussell J., Sivin I. et al. Rates of serious infection after changes in regimens 16. Royal College of Obstetricians and Gynaecologists (RCOG). The care of women 17. Safe abortion: technical and policy guidance for health systems. Second edition. World 18. World Abortion Policies 2011. United Nations, 2012. — URL: un.org. 19. Shannon C., Brothers L.P., Philip N.M., Winikoff B. Infection after medical abortion: a 20. Gary M.M., Harrison D.J. Analysis of Severe Adverse Events Related to the Use of 21. Henderson J.T., Hwang A.C., Harper C.C. et al. Safety of mifepristone abortions in clinical 22. Achilles S., Reeves M. Prevention of infection after induced abortion // Contraception. 23. Spitz I.M., Grunberg S.M., Chabbert-Buffet N., Lindenberg T., Gelber H., Sitruc-Ware R. 24. Zane S., Guarner J. Gynecologic Clostridial Toxic Shock in Women of Reproductive Age 25. Fisher M., Bhatnagar J., Guamer J., Reagan S., Hacker L.K. et al. Fatal toxic shock 26. О материнской смертности в Российской Федерации в 2009 году. Методическое 28. Российское общество дерматовенерологов. Инфекции, передаваемые половым 29. Lamy C., Malartic C.M. de, Perdriolle E., Gauchotte E., Villeroy-de-Galhau S., Delaporte M.-O., Morel O., Judlin P. Prise en charge des infections du post-abortum // J. de 31. Dempsey A. Serious Infection Associated With Induced Abortion in the United States 32. Russo J.A., Achilles S., DePineres T., Gil L. Controversies in family planning: postabortal 33. Patel A., Rashid S., Godfrey E.M. et al. Prevalence of Chlamydia trachomatis and 34. Van Eyk N., Schalkwyk J. van. Infectious Diseases Committee. Antibiotic prophylaxis in 35. Workowski K.A., Berman S. Centers for Disease Control and Prevention (CDC). Sexually 36. Sobel J.D. Bacterial vaginosis. Literature review current through. Jul 2013. — URL: 37. Фрипту В.Г. Сравнительная оценка эффективности вагинальных суппозиториев |