Металл хкс что это
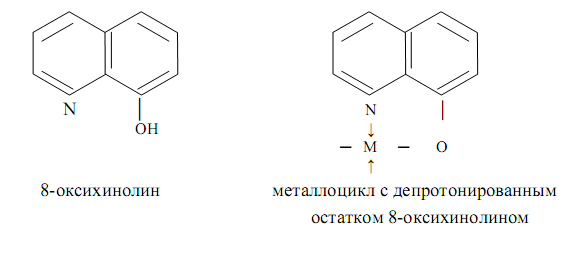
ВКС представляют собой частный случай хелатных комплексных соединений (хелатов) металлов (ХКС), т. е. координационных соединений металлов с одинаковыми или различными отрицательно заряженными или нейтральными полидентатными лигандами (органическими или неорганическими), имеющих один или несколько одинаковых или различных хелатных циклов. Термин «хелат» предложен в 1920 году Морганом и Дрю. Хелаты, в отличии от ВКС, могут быть комплексами катионного, анионного типа или комплексами-неэлектролитами, содержать во внутренней координационной сфере или только полидентатные, или одновременно один или несколько полидентатных и монодентатные лиганды и иметь или не иметь внешнесферные ионы. Различия между ВКС и ХКС иногда (но не всегда) не делается: любые ХКС, содержащие хотя бы один хелатный цикл, нередко называется ВКС. В ХКС один и тот же полидентатный лиганд образует один или несколько хелатных циклов, причём этот лиганд может быть би-, три-, тетра-, пента-, гексадентатным. Так, в комплексах 8-оксихинолином (оксином) реализуются пятичленные металлоциклы:
Примером может служить вышеописанный оксихинолинат цинка или оксихинолинат магния MgL2 (символом HL обозначена молекула 8-оксихолина), осаждающийся из растворов в виде осадка темно-зелёного цвета и используемы для определения магния.
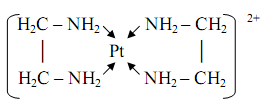
Большую группу хелатных комплексов образует этилендиамин H2NCH2CH2NH2 (часто для краткости обозначаемый En или en), дающий пятичленные металлоциклы, например, в комплексе платины(II)
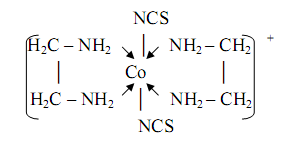
Два идентичных металлоцикла содержаться в комплексе кобальта(III) наряду с двумя монодентатными тиоцианатогруппами:
Этот комплекс применяется для определения серебра(I), висмута(III) в форме соединений [CoEn2(NCS)2][Ag(NCS)2] и [CoEn2(NCS) 2] [BiI4].
К ХКС относятся такие практически важные вещества, как соединения металлов с основаниями Шиффа, комплексонаты, фталоцианины металлов, порфирины, хлорофилл, гемоглобин, цианокобаламин, инсулин, ферритин и многие другие.
Смотрите также
Курсовая работа: Применение органических реагентов в аналитической химии
| Название: Применение органических реагентов в аналитической химии Раздел: Рефераты по химии Тип: курсовая работа Добавлен 14:09:42 27 марта 2010 Похожие работы Просмотров: 2060 Комментариев: 21 Оценило: 5 человек Средний балл: 5 Оценка: неизвестно Скачать | |||
 |  |
Реакция весьма чувствительная: открываемый минимум m=0, 01 мкг. Нитрат-ион NO3 ˉ такой реакции не даёт.
Аналогично протекает реакция также в том случае, если вместо 1-амино-2-нафтола взять β-нафтол: развивается красная окраска.
Вместо сульфаниловой кислоты в этой реакции можно использовать различные другие ароматические амины, которые в щелочной среде с 1-нафтиламином или 1-нафтолом (а также с производными анилина, например, диметиланилином) дают окрашенные азокрасители.
Этакридин (риванол) в кислой среде образует с нитратами диазоэтакридин красного цвета:
 |  |
Реакция специфична для нитратов.
Реакция образования окрашенных соединений с органическими реагентами используются для определения подлинности многих лекарственных препаратов или открытия входящих в них групп, например, органических кислот; соединений, содержащих гидроксильные, альдегидные, кетонные, эфирные, имидные группы, аминогруппы, фенильные радикалы; алкалоидов, гликозидов сердечного действия, витаминов, гормонов и их синтетических аналогов, антибиотиков и других веществ.
3.2 Образование органических соединений, обладающих специфическими свойствами
Летучие сложные эфиры борной кислоты окрашивают пламя в зелёный цвет. В присутствии серной кислоты и этанола борат-ионы образуют сложные эфиры:
При поднесении пламени к чашке или тиглю, в которых протекает эта реакция, продукты сгорания окрашивают пламя в зелёный цвет. Реакция – фармакопейная.
4. ИСПОЛЬЗОВАНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В КАЧЕСТВЕ ИНДИКАТОРОВ В ТИТРИМЕТРИЧЕСКИХ МЕТОДАХ КОЛИЧЕСТВЕННОГО АНАЛИЗА
4.1. Теории кислотно-основных индикаторов
Кроме использования органических соединений для образования металлокомплексов, образования окрашенных соединений органические реагенты используются очень широко в аналитической химии в качестве индикаторов методов кислотно-основного титрования. Индикатор – это вещество, которое проявляет видимое изменение в точке эквивалентности или вблизи её. Кислотно-основные индикаторы в кислых и щелочных растворах имеют различную окраску. Иак, лакмус в кислой среде (рН 7) – в синий; фенолфталеин в кислой – бесцветен, в щелочной – имеет красную или малиновую окраску.
Для объяснения природы изменения окраски индикаторов было предложено несколько теорий. Ионная теория кислотно-основных индикаторов предполагает наличие в растворе двух форм молекулы индикатора – кислой формы, имеющей один цвет, и основной формы, имеющей другой цвет. В зависимости от рН раствора и соответственно от преобладания той или иной формы, происходит окрашивание раствора в соответствующий форме молекулы индикатора цвет.
Хромофорная теория кислотно-основных индикаторов объясняет наличие окраски индикаторов, являющихся органическими соединениями, присутствием в молекулах индикаторов хромофорных групп. В роли хромофорных групп могут выступать такие группировки атомов и связей, как
хиноидные структуры и некоторые другие.
Далее предполагается, что индикаторы в растворе могут присутствовать в разных таутомерных формах, находящихся в равновесии. В кислой среде доминирует одна таутомерная форма индикатора с какой-то, а в щелочной – другая таутомерная форма с иной хромофорной группой. Примером сказанного может послужить индикатор фенолфталеин, который в кислой среде бесцветен, а в щелочной окрашен в красный цвет. Согласно хромофорной теории предполагается, что в водном растворе фенолфталеина устанавливается равновесие:
Таутомерная форма I не имеет хромофорной группы и поэтому бесцветна, а форма II обладает хиноидным хромофором и поэтому окрашена в красный цвет. Другой пример виден у индикатора метиловый оранжевый, который является натриевой солью диметиламиноазобензол-сульфокислоты (CH3 ) 2 N – C6 H4 – N=N – C6 H4 – SO3 Na. В водном растворе анион этой кислоты присоединяет протон и переходит в кислоту, которая подвергается превращению по схеме:
Таутомерная форма I имеет хромофор ─N=N─, придающий индикатору жёлтый цвет, а таутомерная форма II имеет другую хромофорную группу, придающую индикатору красный цвет.
Ионно-хромофорная теория, которая объединила представление ионной и хромофорной теорий.
В рамках этой теории принимается, что кислотно-основные индикаторы представляют собой слабые кислоты и основания, причём нейтральная молекула индикатора и её ионизированная форма содержат разные хромофорные группы.
Допустим, индикатор представляет собой слабую одноосновную кислоту HInd. В соответствии с ионно-хромофорной теорией в водном растворе индикатора устанавливается равновесии:
HInd = H + + Indˉ = H + + IndˉB
кислая форма Iосновная форма II
Кислая форма представляет собой нейтральную молекулу слабой кислоты HIndв какой-то таутомерной форме, основная форма IndˉB – это анион кислотной формы, которая является слабой кислотой в другой таутомерной форме. Хромофорные группы обеих таутомерных форм HInd и IndˉB неодинаковы, поэтому и окраска этих двух форм различна.
При изменении рН растворов, а именно при подкислении равновесие смещается влево – в сторону кислой формы и после понижения рН до такого значения рН1, когда в растворе доминирует эта форма, раствор принимает окраску формы I. При уменьшении концентрации ионов водорода равновесие смещается вправо – в сторону основной формы II. В случае индикатора фенолфталеина схему можно упрощённо представить следующим образом:
4.2 Индикаторы группы азосоединений
4.3 Трифенилметановые индикаторы
Трифенилметановые индикаторы. Индикаторы этой группы также часто применяются в кислотно-основном титровании. Все они формально могут рассматриваться как производные трифенилметана. Из индикаторов этой группы распространены фенолфталеины, сульфофталеины, анилинсульфофталеины, бензеины, собственно трифенилметановые красители. Характер таутомерных превращений фталеинов аналогичен описанным выше для фенолфталеина. К фталеинам относятся α-нафтолфталеин, фенолфталеин, тимолфталеин и др. К сульфофталеинам, содержащим сульфогруппу –SO3 Hв качестве заместителя в ароматических ядрах, принадлежат брокрезоловый зелёный, бромкрезоловый пурпуровый, брофеноловый синий, хлорфеноловый красный и др. Сульфогруппа играет роль ауксохрома. Сульфофталеины обладают интенсивной окраской и резким её изменением при переходе от одной формы индикатора к другой. Различные индикаторы этой группы можно рассматривать в качестве производных фенолового красного
Предполагается, что в растворе феноловый красный претерпевает в зависимости от рН раствора превращения по схеме:
Интервал перехода окраски индикатора наблюдается в пределах рН от
8, 4 (красная). К собственно трифенилметановым красителям относятся кристаллический фиолетовый, малахитовый зелёный, метиловый фиолетовый, пентаметоксикрасный, гексаметоксикрасный. Одним из индикаторов данной группы является кристаллический фиолетовый (кристаллвиолет):
В водных растворах кристаллический фиолетовый протонируется: к атомам азота двух ароматических диметиламиногрупп последовательно присоединяются один или два протона в зависимости от кислотности раствора с образованием зелёной, желтовато-зелёной и оранжевой форм. Интервал перехода лежит в пределах изменения рН раствора от
0,8 (зелёная окраска) до
2, 6 (синяя окраска). Изменение окраски индикаторов этой группы в водных растворах не очень резкое; они чаще применяются при кислотно-основном титровании в неводных средах.
Нитроиндикаторы представляют собой ароматические нитропроизводные, например, паранитрофенол, который в растворе претерпевает превращения:
Интервал перехода лежит в пределах рН от 5, 6 (бесцветный) до 7, 6 (жёлтый). К этой группе индикаторов относятся также мета- и ортонит-рофенолы, динитрофенолы и некоторые другие.
4.5 Индикаторы других структурных групп
Таким образом, как показано выше, в аналитической химии немалую роль играет применение органических реагентов в качественном, количественном анализах, кислотно-основном титровании и других случаях. Качественный анализ имеет большое значение, поскольку частные химические реакции на многие катионы и анионы применяются постоянно в фармацевтическом анализе, фармакопейном анализе для контроля подлинности лекарственных субстанций и компонентов лекарственных форм.
1. Основы аналитической химии. В 2-х книгах под ред. академика РАН Ю.А. Золотова. М.: «Высшая школа», 1996г.
2. Аналитическая химия. В 2-х частях. В.Д. Пономарев. М.: «Высшая школа», 1982г.
3. Аналитическая химия. В 2-х книгах. Ю.Я. Харитонов. М.: «Высшая школа», 2001г.
4. Аналитическая химия. А.Я. Логинов, А.Г. Воскресенский, И.С. Солодкин. М.: «Просвещение», 1973г.
5. Крешков. А.П. Основы аналитической химии, II. т. 1-3, Москва, 1977г.
6. В.Г. Беликов. Фармацевтическая химия. Пятигорск. 1996 г.
7. В.Д. Шаповалова. Фармацевтический анализ лекарственных средств. Харьков, 1995 г.
8. Ф.Б. Коган. Методы идентификации лекарственных препаратов. Киев, 1978 г.
9. Н.Н. Глущенко, Т.В. Плетнёва, В.А. Попков. Фармацевтическая химия. Москва, 2004 г.