Метаболизм костной ткани что это
Физиология паратгормона настолько сильно связана с витамином D и метаболизмом костной ткани, что рассматривать эти вопросы по отдельности, не потеряв их сути, невозможно. Графически взаимоотношения представлена на рисунке ниже. Паратгормон в первую очередь регулирует содержание ионов кальция в межклеточном пространстве. Витамин D контролирует всасывание кальция из пищи, а также косвенно отвечает за минерализацию костной ткани, которая содержит в себе 99% всего кальция организма.
«Можно ли считать кость органом?» Да! Поскольку костная ткань проявляется очень высокую метаболическую активность, а также содержит большие запасы кальция, она напрямую включена в процессы регуляции содержания кальция в межклеточном пространстве и плазме крови. Нормальная концентрация кальция в межклеточном пространстве необходима для выполнения множества клеточных функций, среди которых передача сигнала между клетками, секреция гормонов, нормальная работа мышц и нервов, поэтому необходимо строгое ее сохранение в определенных пределах.
Гипокальциемия ведет к нервно-мышечной гипервозбудимости; умеренное снижение уровня кальция проявляется гиперестезиями с положительными симптомами Хвостека и Труссо; тяжелая гипокальциемия ведет к развитию тетании, судорог и смерти. Гиперкальциемия проявляется летаргией, слабостью, комой и, наконец, смертью. Около 50% внеклеточного кальция находится в ионизированной форме, но точное соотношение зависит от pH. Содержание кальция внутри клеток на порядки меньше, чем вне ее, но некоторые органеллы, например, митохондрии, содержат в себе повышенные концентрации кальция. Колебания уровня внеклеточного ионизированного кальция обычно не превышают ± 10%.
а) Физиология обмена паратгормона. Паратгормон (паратиреоидный гормон, ПТГ, РТН) по химическому строению является 84-аминокислотным полипептидом; было выяснено, что за биологическую активность гормона ответственны первые 34 аминокислотных остатка паратгормона, именно они используются в клинической практике, например, в лечении остеопороза. Определение последовательности классического рецептора ПТГ показало его связь с G-белком и наличие семи трансмембранных сегментов, проявляющих одинаковое сродство как с паратгормоном, так и с ПТГ-родственным пептидом (ПТГ-рП).
Но ПТГ-рП не обладает таким же активирующим действием на 1-гидроксилазы почек, как сам ПТГ.
Наибольшее количество рецепторов к ПТГ находится в костной ткани и в почках, хотя в других органах они также присутствуют в меньших количествах. Недавно был обнаружен новый подвид ПТГ-рецептора, который связывается с карбоксильным остатком паратгормона. Ранее считалось, что данные рецепторы находятся в неактивном состоянии. Этот недавно обнаруженный рецептор не связывается с ПТГ-рП. Неизвестно, играет ли он какую-либо роль в метаболизме костной ткани или имеет какие-либо другие функции.
Клетки паращитовидных желез также экспрессируют рецепторы, чувствительные к кальцию. И они являются рецепторами, связанными с G-белками, и имеют в своем составе семь трансмембранных доменов. Данные рецепторы могут соединяться с различными катионами, но физиологически подходящими для них являются только двухвалентные катионы кальция и магния. Снижение уровня ионизированного кальция ведет к повышению секреции ПТГ, повышение уровня ионизированного кальция ведет к снижению секреции ПТГ.
Таким образом, и концентрация ионизированного кальция, и концентрация ПТГ в плазме крови колеблются лишь в узких пределах. Были описаны различные мутации данных рецепторов, некоторые из них приводят к повышению их активности, другие — к понижению. Данные мутации являются ключом к пониманию семейной гипокальциурической гиперкальциемии и некоторых гипокальциемических синдромов, например, семейного гипопаратиреоидизма.
Паратгормон (ПТГ) повышает резорбцию кальция в почках, усиливает резорбцию костной ткани, повышает активность D1-гидроксилазы почек. Эти механизмы помогают восстановить уровень кальция в плазме крови.
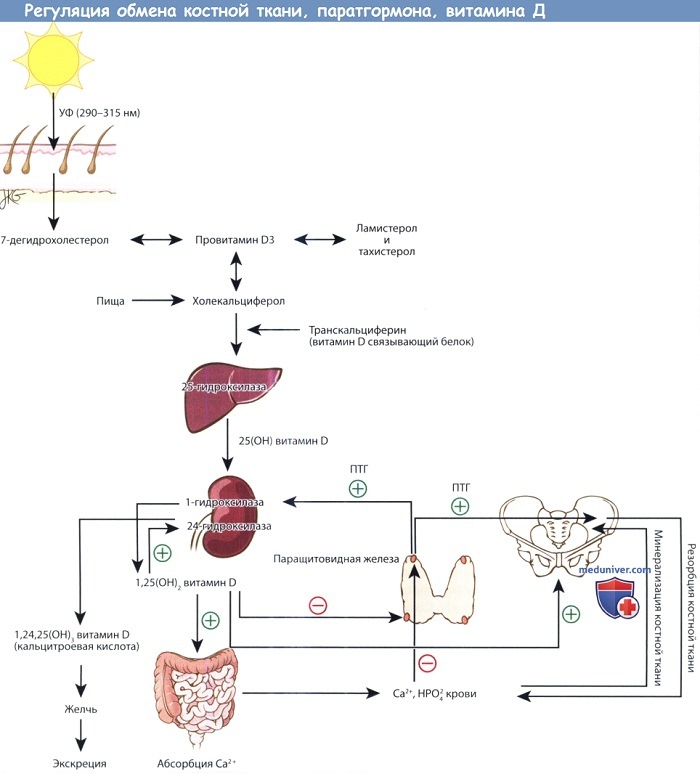
Предшественники витамина D синтезируются в коже под действием ультрафиолета. Превращение 25-ОН витамина D, депонированной формы витамина, в активную форму,
т.е. 1,25-(ОН)2 витамин D, регулируется паратгормоном. 1,25-(ОН)2 витамин D повышает всасывание кальция в желудочно-кишечном тракте.
Кальций и фосфор плазмы крови регулируют содержание паратгормона крови, а также участвуют в минерализации новообразованного костного матрикса.
При повышении уровня паратгормона усиливается резорбция костной ткани, поскольку это необходимо для поддержания необходимого уровня кальция в плазме,
а также стимулируется синтез 1,25-(ОН)2 витамина D почками.
б) Физиология обмена витамина Д. Синтез провитамина D (холекальциферола) происходит в коже из 7-дегидрохолестерола в результате фотокатализа под действием ультрафиолетовых лучей с длиной волны 290-315 нм. Ультрафиолетовые лучи именно с такой длиной волны могут преодолеть атмосферу, поэтому у жителей возвышенностей синтез провитамина D подвержен сезонным колебаниям. Синтез предшественников провитамина D тоже зависит от воздействия солнечных лучей, поэтому избыточное пребывание на солнце не приводит к гипервитаминозу.
Возможности получения витамина D с пищей очень ограничены, лишь крайне малое число продуктов содержит в себе витамин D. Молоко и молочные продукты, производимые в США и Европе, дополнительно обогащаются витамином D. Одна их порция содержит около 100 ME витамина. К сожалению, необогащенные молочные продукты и человеческое грудное молоко содержат крайне малое количество витамина. В желтке яйца содержится около 20 ME витамина D, в белке витамина D нет. Рыба является источником, богатым витамином D.
Витамин D представляет из себя провитамин, активной формой которого является 1-25-(ОН)2 витамин D (кальцитриол). В норме кальцитриол продуцируется почками из витамина D, кальцидиола, в результате реакции 1-гидроксилирования. Активность 1-гидроксилазы почек контролируется ПТГ, поэтому уровень 1-25-(ОН)2 витамина D напрямую коррелирует с уровнем ПТГ. Высокий уровень ПТГ, как правило при гипокальциемии, стимулирует образование 1-25-(ОН)2 витамина D. В результате происходит повышение абсорбции кальция в кишечнике и нормализация его уровня в плазме крови.
При определенных патологических состояниях некоторые другие ткани также могут проявлять 1-гидроксилазную активность, иногда независимо от действия ПТГ.

в) Метаболизм минеральных веществ в костной ткани. Мы часто воспринимаем кости лишь как опорные структуры, но на самом деле костная ткань играет важную роль в метаболизме, выступая в качестве депо кальция, фосфатов и карбонатов, также она участвует в поддержании кислотно-щелочного равновесия. Матриксом кости является частично минерализованная ткань и специфические костные клетки. Костную систему человека разделяют на осевой скелет, к которому относят череп, позвоночный столб, грудину, ребра и таз, и на скелет конечностей, от их проксимальных отделов до кончиков пальцев.
Также костная ткань подразделяется на губчатую (трабекулярную), которая обладает высокой метаболической активностью, и кортикальную, которая имеет большую плотность и меньшую метаболическую активность. Изменения в кортикальной костной ткани наступают при тяжелых или длительно текущих заболеваниях. В осевом скелете преобладает содержание трабекулярной кости, в скелете конечностей — кортикальной.
К костным клеткам относят остеобласты, остеокласты и остеоциты. Остеобласты происходит из мезенхимальных стволовых клеток, они образуют соединительнотканный матрикс кости, который затем минерализуется, формируя новую костную ткань. Большинство остеобластов подвергаются апоптозу, но часть из них остается включенной в костный матрикс и превращается в остеоциты, а другая часть остается на поверхности кости, формируя надкостницу.
Трансформируясь в остеоциты, эти клетки образуют длинные отростки, которыми они создают щелевой контакт с соседними клетками и с клетками надкостницы. Остеоциты воспринимают механическое давление, оказываемое на кость, и играют важную роль в моделировании костной ткани. Остеокласты представляют собой крупные многоядерные клетки, происходящие из одноядерных макрофагов. Процесс дифференцировки клеток в остеокласты происходит под контролем ядер-ного фактора кВ (каппа-Б, RANKL), продуцирующего в ходе апоптоза остеобластов, и под контролем колониестимулирующего фактора макрофагов.
Остеокласты участвуют в резорбции костной ткани, разрушая минеральный компонент и коллагеновый матрикс костной ткани посредством протеолиза.
В норме костная ткань постоянно разрушается остеокластами и одновременно заново синтезируется остеобластами. Этот процесс получил название ремоделирования костной ткани. В здоровом организме процессы разрушения и синтеза костной ткани находятся в равновесии. Ремоделирование костной ткани крайне важно для поддержания структурной целостности (прочности) скелета, т. к. с ее помощью постоянно восстанавливаются микропереломы костей, возникающие от каждодневных физических нагрузок.
г) Кальций-чувствительные рецепторы. Как уже упоминалось выше, паращитовидные клетки экспрессируют кальций-чувствительные рецепторы. Первоначально данные рецепторы были выделены из паращитовидных клеток крупного рогатого скота, затем их наличие было подтверждено и у человека. Кроме паращитовидных желез, где они и были впервые обнаружены, данные рецепторы экспрессируются в почках, костях, желудке, легких, головном мозге и других тканях.
Как мутации, так и приобретенные дисфункции данных рецепторов могут стать причиной появления различных заболеваний, связанных как с повышением, так и с понижением кальция крови. Более подробно эти заболевания будут рассмотрены ниже.
Учебное видео расшифровки биохимического анализа крови
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Научная электронная библиотека
1.1. Особенности метаболизма костной ткани
В филогенетическом аспекте кость является самой молодой тканью. Она до сих пор находится в периоде адаптации к существованию в условиях гравитации. Кроме того, скелет человека подвержен воздействию такого фактора, как прямохождение, а в последние столетия претерпевает изменения, связанные с гипокинезией и различными вынужденными положениями.
В морфофункциональном отношении кость является одной из наиболее сложных и биологически активных тканей. По многим показателям она превосходит другие системы организма и является наиболее массивной, многофункциональной, обладает высокой метаболической и репаративной активностью. Костная ткань в разных участках на 20–25 % состоит из органического матрикса. Около 60–65 % массы сухого деминерализованного матрикса приходится на коллаген и 17–18 % на неколлагеновые белки, по своей структуре, являющиеся гликопротеинами. В состав стромы костного мозга входят недифференцированные стволовые мезенхимальные клетки – ретикулярные, соединительнотканные, эндостальные фибробластоподобные, эндотелиальные клетки, адипоциты, дифференцированные костные клетки (остеобласты, остеокласты, остеоциты), межклеточное вещество, клетки эндоста и периоста, костный мозг, сосудистые, лимфатические и нервные образования, интимно связанные с окружающими мягкими тканями [13, 28, 36, 52].
В костной ткани постоянно протекают два противоположно направленных процесса – резорбция и новообразование. Соотношение этих процессов зависит от различных факторов, в том числе от физических нагрузок на кость и возраста. Считается, что остеогенез происходит за счет клеток эндоста, периоста и костного мозга. Процесс физиологического ремоделирования губчатой костной ткани проходит несколько фаз, в каждую из которых ведущую роль выполняют те или иные клетки. Первоначально участок костной ткани, подлежащий резорбции, «помечается» остеоцитами при помощи специфических цитокинов (активация), разрушается протективный слой на костном матриксе. К оголенной поверхности кости мигрируют предшественники остеокластов и сливаются в многоядерную структуру – симпласт – зрелый остеокласт. Затем остеокласт деминерализует костный матрикс (резорбция), уступает место макрофагам, которые завершают разрушение органической матрицы межклеточного вещества кости и подготавливают поверхность к адгезии остеобластов (реверсия). На последнем этапе в зону разрушения прибывают предшественники, дифференцирующиеся в остеобласты, они синтезируют и минерализуют матрикс в соответствии с новыми условиями статической и динамической нагрузки на кость (формирование) [9, 14, 19, 45].
Регуляция остеогенеза имеет три уровня: локальный (местный), системный и генетический. Это обстоятельство в конечном итоге обеспечивает высокий уровень метаболизма костной ткани.
Локальную регуляцию осуществляет микроокружение посредством различных цитокинов, большим количеством факторов роста, рядом полипептидов, ферментов, межклеточных контактов.
Системная нейроэндокринная регуляция осуществляется гормонами и веществами с гормоноподобным действием. Наиболее изученными являются паратиреоидный гормон, половые гормоны, метаболиты вит. D, кальцитонин, глюкокортикоиды, тиреоидные гормоны [9, 52]. Морфофункциональная связь остеогенеза и кровообращения осуществляются не только анатомически, но и тесно функционально. Это подтверждено многочисленными исследованиями связей внутрикостной и внекостной системы артериального, венозного, лимфатического русла, нервной регуляции с остеорецепцией.
Красный костный мозг является депо крови, органом кроветворения, высокочувствительной рефлексогенной зоной, центральным звеном иммунной системы. Красный костный мозг – это источник практически неистощаемого пула мезенхимальных стволовых фибробластоподобных клеток – предшественников остеобластов, способных не только потенцировать остеогенез, но и строить кроветворное микроокружение и регулировать собственно кроветворение [49].
Нарушение процесса остеогенеза приводит к патологии. Исследования В.М. Чепоя (1978) с применением радиоактивного пирофосфата технеция показали, что при межпозвонковом остеохондрозе в телах позвонков отмечается значительное ослабление фибробластических процессов и усиление остеокластических изменений. Кость становится разреженной и хрупкой, как в старческом возрасте, т.е. развивается остеопороз. По мнению McMahon et al. (2002) дефицит в остеогенезе карбоангидразы-2 приводит к появлению симптомов остеосклероза.
По данным С.В. Либенсона (1989) при гипокинезии происходят существенные изменения в системе регуляции остеогенеза, выражающиеся в гипокальцемии, увеличении содержания паратгормина и кальцитонина в крови, гиперэкскреции с мочой минеральных и органических компонентов, участвующих в остеогенезе. Подобные же изменения автор наблюдал и при хроническом болевом синдроме.
Репаративная регенерация – это восстановление ткани после повреждения. Механизмы физиологической и репаративной регенерации костной ткани качественно едины, осуществляются на основе общих закономерностей. Репаративная регенерация – есть в той или иной мере усиленная физиологическая [34]. Одними из индукторов репаративной регенерации костной ткани и усиления метаболизма являются ее травматическое повреждение [10, 34], а также метод аутотрансплантации красного костного мозга, как источника мезенхимальных стволовых клеток – предшественников фибробластов.
Многие исследователи указывают на возможность локально возбуждать репаративную регенерацию костной ткани, тем самым изменять ее метаболизм, методом остеотомии, трепанации, туннелизации или перфорации в необходимых участках кости. Локализованная и дозированная альтерация костной ткани применяется, как средство терапевтического воздействия и приводит к купированию дегенеративно-дистрофических нарушений. Лечебный эффект проявляется местно в зоне стимуляции и регионарно в сегментарных областях за счет интенсификации гемоциркуляции [10, 32, 34].
Микротравматическое повреждение костной ткани приводит к возникновению остеоиндуктивного сигнала, который осуществляется морфогенетическим белком-2, при этом, как в костной ткани, так и в кровеносной системе, происходит стремительная активация ростовых факторов (инсулиноподобного фактора роста, фактора роста фибробластов, колониестимулирующего фактора, фактора некроза опухоли-α и т.д.) [6].
Индуцированный фактор некроза опухоли человека (hTNF)-α стимулирует образование одноядерных преостеокластоподобных клеток (POCs), увеличивает число мРНК рецепторов кальцитонина (CTR) в POCs, формирует образование колонийстимулирующего фактора макрофагов (M-CSF) и экспрессирует образование мРНК активатора ядерного фактора Каппа В лиганда (RANKL). Совместное влияние стволовых клеток красного костного мозга и hTNF-α с растворимым RANKL увеличивают образование многоядерных остеокластоподобных клеток (MNC-s) из макрофагов, осуществляя лизис и резорбцию перелома. RANKL не только участвует в сигнальной трансдукции преостеокластов и остеокластов, но и в резорбтивной функции и выживании зрелых остеокластов [50]. Сигнальные механизмы RANKL распространяются и на активируемые митогенами протеинкиназы – нейроэндокринный уровень регуляции [50]. HTNF-α, простагландин Е2 (PGE2), паратгормон (PNG), 1, 25 (ОН) 2 витамин D3 индуцируют образование интерлейкина 11 (IL-11), интерлейкина 11R (IL-11R) и гликопротеина (gp 130) остеобластами за счет мРНК.
Основной фактор роста фибробластов (bFGF) увеличивает в ККМ количество остеобластов и стимулирует образование белкового матрикса, ускоряя минерализацию и снижая уровень свободного фосфата.
При повреждении кости в красном костном мозге, так же экспрессируется мРНК фактора роста эндотелия сосудов (VEGF) с рецепторами. Ангиобласты способствуют окружению поврежденной зоны капиллярами. Действие механического повреждения может быть потенцировано введением аутологичных стволовых клеток костного мозга [36].
Особый интерес вызывают работы о применении внутрикостной трансплантации аллогенного костного мозга для лечения экспериментального сенильного остеопороза. В этом случае остеоиндуктивный сигнал осуществляется морфогенетическим белком-2 и макрофагами [25, 50]. Аденозинтрифосфат (АТФ) так же участвует в передаче сигналов факторов роста ККМ за счет повышения активности протеинкиназ. Таким образом, существенно усиливается метаболическая активность костной ткани.
Янковский Г.А. (1982) привел результаты лечения 135 больных пояснично-крестцовым радикулитом методом введения 1 мл изотонического раствора натрия хлорида в остистые отростки нижних поясничных позвонков. У 122 пациентов автор отметил значительный регресс неврологической симптоматики и в течение последующих 2-х лет у этих больных поясничные боли не отмечались. При рентгенденситометрии у данных пациентов было выявлено увеличении плотности костной ткани. Автор сделал вывод, что внутрикостная пункция остистого отростка вследствие общности кровообращения обуславливает улучшение трофики тела позвонка и, соответственно, межпозвонкового диска.
При гистологическом исследовании костной ткани И.Н. Атясовым (2000) после проведения внутрикостного введения 10 мл различных жидкостей или крови в 1 сутки определялось разрушение костных трабекул, повреждение стромы и паренхимы костномозговой ткани, нарушение кровообращения в очаге деструкции, что являлось следствием механического повреждения в момент внедрения иглы в кость.
Через 3 суток на месте внутрикостного вливания 10 мл жидкости наблюдалось разрастание нежноволокнистой ткани и гиперплазия эндостальных элементов в виде окружения близлежащих к очагу деструкции костных трабекул остеобластами, а в некоторых опытах (после внутрикостного введения лекарственных жидкостей вместе с аутологичным костным мозгом) – уже было видно образование и разрастание остеоидных балочек.
Через 5 суток разросшаяся нежноволокнистая ткань почти полностью замещала очаг кровоизлияний, определялась резко выраженная гиперплазия соединительнотканных и эндостальных элементов в виде разрастания множества остеоидных балочек и напластования остеоидных масс на окружающие зрелые костные балки.
По истечении 7 суток в месте введения жидкости определялась нежно-волокнистая ткань, полностью замещающая очаг кровоизлияний.
Через 15 суток в нежно-волокнистой соединительной ткани определялись скопления лимфоидных и жировых клеток, множество зрелых костных балок с явлениями активной перестройки с помощью остеобластов и остеокластов.
На 18–20 сутки определялись участки фиброза.
В последующие 30–60 суток в месте введения иглы в кость отмечалась разросшаяся фибринозная ткань неравномерной плотности, окруженная костными балками, находящимися в стадии дальнейшей перестройки.
К 60 суткам костная и костномозговая ткани полностью восстанавливали свою клеточную структуру [2, 3].
Костная ткань – это главное депо минеральных солей в организме, по своей химической структуре представляет собой кристаллы гидроксиапатита, поэтому обладает физическими свойствами пьезоэлектрика. При одноостных сжатиях, изгибах или кручениях постоянно изменяется пьезоэлектрический потенциал как всей кости, так и отдельных ее составляющих элементов. В основополагающих работах Фукады и Ясуды (1957) было показано, что поляризация линейно связана с механическим напряжением и деформацией. В состоянии покоя на поверхности кости нет связанных поляризационных зарядов, вызванных собственными механическими напряжениями, т.к. они компенсируются ионами электролита. Механическая деформация кости определенным образом изменяет пьезоэлектрические потенциалы.
Так, на вогнутой поверхности образуется отрицательный, а на выпуклой – положительный заряд. Сочетание положительных и отрицательных потенциалов так же существенно влияет на процессы активации остеокластов, остеобластов и других клеток кости и костного мозга, на движение ионов и заряженных молекул по кровеносным сосудам.
На вогнутой поверхности стимулируется костеобразование, а на выпуклой – резорбция кости. Кроме того, кровотоком создается электрохимический потенциал. Совокупность электропотенциалов распределена в кости таким образом, что венулы заряжены преимущественно положительно, что, по-видимому, является биологически оправданным механизмом предотвращения зарастания костных каналов, в которых они проходят.
Однако при недостаточных механических нагрузках на кость, незначительном внутрикостном кровотоке, венозном застое изменяется соотношение разнополярных потенциалов. Положительный заряд венул уменьшается или превращается в отрицательный. Это способствует костеобразованию в месте их выхода. Уменьшается диаметр отверстия, в котором проходит венула, что ограничивает возможности резервного оттока, усиливает отек, замедляет отток крови от кости. Таким образом, замыкается патологический круг.
Терапия нарушений метаболизма костной ткани
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Остеопороз (ОП) – прогрессирующее системное заболевание скелета, характеризующееся снижением костной массы и нарушением микроархитектоники (качества) костной ткани, что приводит к хрупкости костей и повышению риска перелома. Важно подчеркнуть, что заболевание протекает асимптомно до тех пор, пока не случится низкоэнергетический перелом. Он – самое распространенное заболевание костной ткани: остеопоротические переломы отмечается у половины всех женщин, находящихся в периоде постменопаузы, а также у мужчин старших возрастных групп [1]. По данным Российской ассоциации по ОП, каждые 5 минут в России происходит перелом шейки бедра, вызванный ОП, а в год в нашей стране из–за него происходит 9 млн переломов периферического скелета и более 3 млн случаев переломов позвонков (www.osteoporoz.ru). Пациенты, перенесшие один остеопоротический перелом, имеют высокий риск повторных переломов. Следовательно, наиболее важной целью лечения ОП является предотвращение переломов [1].
Костная ткань является разновидностью соединительной и вместе с хрящевой образует скелет. Для выполнения своих функций (движение, защита внутренних органов, костного мозга и нервной системы) скелет должен быть прочным, а, следовательно, жестким и гибким одновременно. Жесткость кости придают минералы (кальций, фосфор), а гибкость – органический матрикс (коллаген I типа и неколлагеновые белки: остеокальцин, остеонектин, остеопонтин и др.). В течение всей жизни человека, начиная с рождения и дальше, с возрастом, и жесткость, и гибкость кости снижаются, поскольку происходят потеря минералов и повреждение матрикса. Для того чтобы противостоять этим проявлениям старения, в кости существует процесс постоянного обмена (ремоделирования), обеспечивающий обновление всего скелета 3–4 раза за жизнь. Способность костной ткани к самостоятельному ремоделированию способствует не только адаптации и обновлению, но и заживляет переломы, трещины, а также микропереломы. Таким образом, ремоделирование кости – это процесс, работающий в течение всей жизни и направленный на восстановление и сохранение скелета как структурного и функционального органа.
Ремоделирование выполняется двумя основными клетками костной ткани: остеокластами, резорбирующими кость, и остеобластами, формирующими новую кость. Остеокласты – многоядерные гигантские клетки, происходящие из мононуклеарных фагоцитов, продуцируемых гематопоэтической системой. Прикрепившись к кости, остеокласты начинают продуцировать множество протеолитических ферментов, разрушающих матрикс кости, а также ионы водорода, рассасывающие кристаллы гидроксиапатита. Весь процесс резорбции кости занимает обычно несколько дней.
Процесс костеобразования, продолжающийся несколько недель, выполняется остеобластами. Последние происходят из предшественников – мезенхимальных или стромальных стволовых клеток. Остеобласты значительно меньше размером, чем остеокласты, и имеют одно ядро. Они синтезируют остеоид, органический матрикс кости, и ответственны за дальнейшую его минерализацию. Примерно один из десяти остеобластов при образовании нового костного матрикса остается замурованным внутри и превращается в остеоцит. Остеоциты соединены друг с другом и с покровными клетками длинными отростками, позволяющими функционировать целой коммуникационной системе внутри кости. Благодаря этому остеоциты служат системой «быстрого реагирования» на любые внутренние и внешние стимулы и регулируют процессы резорбции и костеобразования.
Костное ремоделирование – гомеостатический процесс, вовлекающий повторные циклы резорбции и депозиции новой кости. В норме ежедневно в различных частях скелета работают от 2 до 5 млн единиц (мест) костного ремоделирования, каждая состоящая из нескольких остеокластов и множества остеобластов. Важно понимать, что их активности тесно связаны друг с другом: костная резорбция предшествует костеобразованию и связана с целым рядом сложнейших метаболических изменений. Предшественники остеобластов вырабатывают ряд веществ, способных связываться с рецепторами остеокластов и, как это ни парадоксально, усиливают дифференцировку и активацию остеокластов. Ведущую роль из них играют макрофаг–колониестимулирующий фактор (М–КСФ) и лиганд RANK (рецептора активации фактора NF–KB). Мононуклеары обеспечивают условия для работы новых остеобластов, синтезирующих компоненты органического матрикса для восстановления дефекта кости. Активация одних клеток приводит к активации других, так что количество резорбированной ткани соответствует количеству вновь образованной кости. Затем наступает период относительного покоя, сменяющийся периодом незначительной активности клеток, далее проходит новый цикл ремоделирования. Постоянный костный обмен важен для здоровья костной ткани, он предупреждает накопление старой, «усталой» кости, способствует репарации микропереломов и изменению костной архитектоники в ответ на повторные нагрузки. Не надо забывать, что кость является резервуаром кальция в организме и ремоделирование обеспечивает процесс гомеостаза кальция.
Дефицит эстрогенов после наступления менопаузы приводит к увеличению скорости костного ремоделирования, при этом увеличивается количество резорбированной кости и снижается объем вновь образованной, что приводит к потере массы кости и ее структурным нарушениям. Постменопаузальный ОП характеризуется гиперактивностью остеокластов, приводящей к столь высокой скорости потери кости, что для компенсации последствий работы нескольких аномально активированных остеокластов требуется несколько месяцев деятельности многочисленных остеобластов. В связи с указанным процессом за первые 10 лет от наступления менопаузы женщина теряет 20–30% трабекулярной и 5–10% кортикальной кости. Одновременно ухудшается качество кости: уменьшается ее объем и толщина трабекул, снижается их количество. Чрезмерная резорбция костной ткани, не компенсируемая костеобразованием, лежит в основе и других костных заболеваний, таких как болезнь Педжета, метастазирование опухолей и др.
Возможности медикаментозного воздействия на костную ткань в мировой медицинской литературе обсуждаются с 60–х годов XX столетия. В 1962 г. Н. Fleisch и S. Bisaz впервые высказали предположение о влиянии пирофосфата на физиологическую регуляцию процесса обмена кальция, что привело в дальнейшем к внедрению в клиническую практику целой группы фармакологических препаратов, получивших название бисфосфонатов. Они были синтезированы как устойчивые аналоги встречающихся в природе соединений пирофосфата, имеющие высокое сродство к гидроксиапатиту и селективно присоединяющиеся к костной ткани, влияя на процессы ремоделирования за счет снижения активности остеокластов, что подвело основу для использования их в качестве антирезорбтивных средств. В отличие от множества других лекарственных препаратов бисфосфонаты прикрепляются к активным участкам костного ремоделирования и именно там проявляют свой эффект [2].
Первенцем на этом пути стал этидронат. Синтезированный около 100 лет назад, он нашел применение как ингибитор коррозии или комплексный агент в различных отраслях промышленности при изготовлении тканей, минеральных удобрений, нефтепереработке. Первое описание медицинского применения бисфосфонатов опубликовано в 1969 г. в журнале «Ланцет», когда 16–месячного ребенка с оссифицирующим миозитом успешно лечили этидронатом с целью подавления внекостной оссификации. В 1972 г. была опубликована первая статья об эффективности этидроната при болезни Педжета [2].
В последующем было синтезировано второе поколение бисфосфонатов, содержащих атом азота, антирезорбтивная активность которых была существенно выше. Сейчас известно, что азотсодержащие бисфосфонаты подавляют метаболизм мевалоната и пренилирование белков, что приводит к структурным изменениям внутри остеокласта и нарушению его функции. Благодаря этому костный обмен возвращается к физиологическому уровню, наблюдавшемуся до менопаузы, и предупреждаются дальнейшая деструкция микроархитектоники и потеря кости. Обмен кости остается стабильным на протяжении длительного приема алендроната, по крайней мере в течение 10 лет. Это доказывает, что аккумуляция препарата в кости не приводит к гиперсупрессии ремоделирования.
В настоящее время бисфосфонаты являются признанным методом профилактики и лечения ОП у мужчин и у женщин. Исследования, успешно проведенные на десятках тысяч пациентов, показали, что бисфосфонаты безопасны, хорошо переносятся, имеют мало побочных эффектов, подавляют костную резорбцию, способствуют повышению МПК и снижают риск переломов.
В настоящее время в клинической практике используется несколько бисфосфонатов (алендронат, ризедронат, ибандронат, золедроновая кислота) с различными путями и режимами введения (таблетка 1 раз/нед. или 1 раз/мес., внутривенные введения раз в 3 месяца или раз в год).
Первое место по продолжительности изучения, количеству проведенных исследований и наличию серьезной и разнообразной доказательной базы эффективности и переносимости в клинической практике занимает алендронат. Лечение алендронатом эффективно уже к концу года приема у 95% пациентов [3].
Наиболее весомый вклад в проблему изучения эффективности алендроната внесли исследования FOSIT (Fosamax International Trial) и FIT (Fracture Intervention Trial), из которых известно, что МПК в области позвоночника уже к 3–му мес. лечения увеличивается на 3%. К концу 12–го мес. приема алендроната отмечено повышение МПК в поясничном отделе позвоночника на 13,7% и проксимальном отделе бедра на 5,4%. Риск новых переломов позвонков снизился на 47%, частота прогрессирования деформации позвонков – на 64%, риск болезненных переломов позвонков – на 55%. Продолжением исследования FIT послужило исследование FLEX по 10– либо 5–летнему приему алендроната с переводом на плацебо, показавшее снижение общего риска периферических переломов на фоне непрерывного 10–летнего лечения (частота составила 5,3% для плацебо и 2,4% для алендроната).
К настоящему времени доказано, что алендронат снижает риск не только переломов позвонков, но также других типов остеопоротических переломов, включая переломы предплечья и проксимального отдела бедра. По данным мета–анализов результатов рандомизированных контролируемых испытаний, алендронат снижает относительный риск новых переломов позвонков на 48%, внепозвоночных переломов – на 49%, перелома шейки бедра – на 55%. Кроме того, алендронат эффективен при первичной профилактике переломов позвонков. Исследование FIT продемонстрировало также уменьшение боли и повышение мобильности больных постменопаузальным ОП, принимающих алендронат. Сходные результаты были обнаружены у мужчин и пациентов со стероидным ОП.
Особенности метаболизма бисфосфонатов и их прочное длительное соединение с костной тканью позволили предположить, а затем и доказать эффективность более редкого приема. Так, алендронат, принимаемый в дозе 70 мг 1 раз/нед., так же эффективен, как принимаемый ежедневно в дозе 10 мг/сут., но при этом сопровождается лучшей приверженностью пациента проводимому лечению.
В целом бисфосфонаты хорошо переносятся и побочные эффекты встречаются редко. Тем не менее пациенты должны быть проинформированы о возможных осложнениях лечения. Началу лечения должно предшествовать обследование пациента, направленное на поиск возможных противопоказаний: состояние полости рта, функциональные пробы почек и печени, общий клинический анализ крови, уровень кальция, магния, фосфора и щелочной фосфатазы в сыворотке крови.
При приеме бисфосфонатов возможна транзиторная гипокальциемя, обычно протекающая бессимптомно. Клинически значимая гипокальциемия регистрировалась при слишком быстрой внутривенной инфузии бисфосфоната и при одновременном лечении аминогликозидами. Индуцированная бисфосфонатами гипокальциемия также наблюдается при дефиците витамина D, поэтому для ее предупреждения лечение этими препаратами всегда сопровождается назначением холекальциферола или альфакальцидола.
При пероральном приеме бисфосфонатов отмечены случаи раздражения пищевода, обычно связанные с нарушениями инструкции по приему препарата (принимать таблетку утром с полным стаканом воды, после чего 30 мин. не принимать пищу и не ложиться). Крупное рандомизированное контролируемое испытание с участием более 20 000 пациентов продемонстрировало отсутствие разницы в частоте любых побочных эффектов, включая гастроинтестинальные, между ежедневным, еженедельным приемом алендроната и плацебо.
После внутривенной инфузии бисфосфоната у 20–40% больных регистрируется лихорадка и другие проявления гриппоподобного синдрома (головная боль, миалгии и т.д.). Обычно эта реакция начинается 10 ч спустя после инфузии и продолжается 1–2 дня. Возможно назначение симптоматической терапии, которая, однако, в большинстве случаев не требуется. В целом острофазовая реакция наблюдается практически только на первую инфузию и крайне редко наблюдается при повторных вливаниях.
У больных с инфекцией полости рта, а также у пациентов после иплантации, экстракции зуба или другого вмешательства в полости рта возможно развитие остеонекроза челюсти на лечении бисфосфонатами, наблюдающееся крайне редко. В подавляющем большинстве описанные в литературе случаи касались пациентов с онкологическими заболеваниями, получавших длительно большие дозы внутривенных бисфосфонатов по поводу костных метастазов.
Оптимальной продолжительностью лечения бисфосфонатами считается 3–5 лет. Выделяются 3 фазы лечения: до 12 мес. – фаза репарации, от 6 до 36 мес. – фаза восстановления, 24–60 мес. – фаза поддержки костной ткани [2]. Лечение бисфосфонатами должно проводиться в непрерывном режиме на протяжении ряда лет, и это необходимо объяснять каждому пациенту, который начинает лечение. Наибольшая скорость повышения МПК наблюдается в течение первых 12 мес. лечения, когда лакуны резорбции начинают репарироваться и заполняются костной тканью. Во время последующих фаз повышение МПК не столь заметно, поскольку в этот период восстанавливаются структура трабекулярной ткани и ширина трабекул. Общепринято, что выраженное снижение риска перелома в течение первого года терапии бисфосфонатами обусловлено восстановлением трабекулярной сети и повышением МПК.
К настоящему времени опубликованы результаты длительных (7–10–летних) исследований по применению алендроната при постменопаузальном ОП, показавшие постоянное увеличение МПК примерно на 0,7% в год. Таким образом, за 10–летний период плотности кости в области позвоночника увеличивается на 13,7%, в области шейки бедра – на 6,7%. Это свидетельствует о том, что позитивный баланс при костном ремоделировании сохраняется на всем протяжении длительного лечения. При этом показано отсутствие значимых нарушений минерализации скелета. Биопсии костной ткани, проведенные через 7 лет после начала терапии, показали, что строение трабекул не нарушается, микропереломы не обнаруживаются, а количество нормальных кристаллов гидроксиапатита увеличивается, свидетельствуя о том, что кость становится более устойчивой к компрессии.
Показателем эффективности применения бисфосфонатов является снижение концентрации маркеров костной резорбции в сыворотке крови пациента, наблюдаемое уже через 3–6 нед. лечения. Если к концу 2–3–го мес. терапии не произошло снижения маркеров на 30–40%, следует задуматься, принимает ли пациент препарат и правильно ли он это делает. Денситометрия при приеме бисфосфонатов проводится раз в год. Интересно, что в крупных многоцентровых исследованиях бисфосфонатов было показано снижение риска переломов даже в отсутствие повышения МПК.
В последние годы на рынке появились дженерики бисфосфонатов, в частности алендроната. Для широкого внедрения в клиническую практику важно знать, были ли проведены исследования на биоэквивалентность дженерического препарата и оригинального средства.
В 2003 г. было проведено исследование биоэквивалентности Теваната оригинальному препарату, целью которого является сравнение фармакокинетических параметров Теваната и оригинального препарата (Фосамакс). На 120 здоровых добровольцах было проведено тройное перекрестное рандомизированное исследование кинетики накопления препаратов в моче, которая изучалась в течение 36 ч после однократного приема внутрь 70 мг, отмывочный период между приемами препаратов составлял 7 дней. Результаты исследования показали отсутствие достоверных различий по фармакокинетическим параметрам: максимальной концентрации в моче Rmax, времени достижения максимальной концентрации в моче Тmax, общему количеству экскретируемого неизмененного препарата в моче в течение 36 часов Тае(0–36). Другими словами, Теванат 70 мг полностью биоэквивалентен оригинальному препарату [4]. Следовательно, появление дженерического препарата алендроновой кислоты компании Teva позволяет применять Теванат для увеличения минеральной плотности кости и снижения риска переломов (в качестве первичной и вторичной профилактики), лечения ОП у мужчин, стероидного ОП. Необходимо помнить о достаточном поступлении кальция и витамина холекальциферола в комбинации с пероральными препаратами для лечения ОП.
Таким образом, хорошо изученный механизм действия бисфосфонатов наряду с опытом длительного лечения тысяч пациентов с ОП в контролируемых испытаниях свидетельствуют об их положительном влиянии на здоровье костной ткани. Они снижают скорость обмена костной ткани и повышают МПК. Эти изменения ассоциируются с достоверным статистически значимым снижением риска переломов позвонков и переломов периферического скелета. Данные клинических испытаний продолжительностью до 10 лет продемонстрировали сохраняющуюся эффективность и хорошую переносимость алендроната. Более редкий режим приема обеспечивает больных более удобной формой приема при сохраненной эффективности.
Азотсодержащие бисфосфонаты включены во все зарубежные клинические рекомендации по ОП, а также наряду со стронция ранелатом названы препаратами первой линии в лечении постменопаузального ОП в «Российских клинических рекомендациях по диагностике и лечению ОП» [5]. Алендронат также эффективен при ОП у мужчин, стероидном ОП и в качестве средства первичной профилактики ОП.