Антибиотики: вред и польза
Антибиотики (от анти… и греческого bios — жизнь) – это специфические химические вещества, образуемые микроорганизмами и способные в малых количествах оказывать избирательное токсическое действие на другие микроорганизмы и на клетки злокачественных опухолей.
Первый эффективный для клинического применения антибиотик (пенициллин) открыт А. Флемингом в 1929, термин «антибиотики» предложил в 1942 3. Ваксман.
Описано свыше 4 тыс. антибиотиков, но применяются лишь около 60.
Классификация антибиотиков.
По химической природе антибиотики принадлежат к различным группам соединений.
Антибиотики разделяются на:
По молекулярному механизму действия различают антибиотики, нарушающие:
Антибактериальные антибиотики широкого спектра действия подавляют рост как грамположительных, так и грамотрицательных бактерий (тетрациклины, аминогликозиды, полусинтетические пенициллины, цефалоспорины и др.). Антибиотики узкого спектра действия активны в основном в отношении грамположительных микробов (пенициллины, макролиды, рифампицин и др.)
Мнения, насчёт применения антибактериальных препаратов разделились: кто-то считает, что антибактериальные препараты – современные средства, помогающие успешно противостоять инфекционным заболеваниям, другие уверены, что антибиотики сами по себе вызывают серьезные нарушения в человеческом организме, поэтому их прием представляет значительную опасность. Некоторые страны Европы призывают отказаться от лекарств в легких случаях недомогания. В Британии медики призывают лечить воспалённое горло медом и горячим чаем, чтобы снизить неоправданный прием лекарств. А в Нидерландах кашель вообще не считают заболеванием, и не выписывают лекарства. Некоторые страны просвещают жителей на тему приема препаратов, где-т о просто вводят на них жесткие ограничения.
Несмотря на резкую критику антибиотиков, они, тем не менее, считаются одним из значимых открытий в истории человечества. Если до их изобретения люди умирали от обычной простуды, то сегодня антибактериальные препараты способны справиться с тяжелыми заболеваниями, ранее считавшимися неизлечимыми.
Пневмония, туберкулез, желудочно-кишечные инфекции, венерические заболевания, заражения крови и послеоперационные осложнения – правильно и своевременно назначенные противомикробные средства помогут справиться с серьезными состояниями, по возможности сведя к минимуму риск развития осложнений.
Кроме того, современные антибиотики, относящиеся к группе синтетических, создаются на основе новейших разработок: их прием относительно безопасен, а концентрация активных антибактериальных компонентов в одной дозе препарата рассчитывается с максимально возможной точностью.
К сожалению, антибиотики способны вызывать побочные действия такие, как:
Таким образом, становится понятным, почему врачи настаивают на том, чтобы никогда и ни при каких условиях пациенты не занимались самолечением, тем более самолечением антибиотиками. Однако есть состояния, когда прием антибиотиков однозначно не нужен. Это следующие патологии: вирусные заболевания, включая грипп, которые врачи
Антибиотики – мощное и действенное лекарство, чье влияние на организм полностью зависит от того, насколько правильно оно используется.
Информация на сайт подготовлена сотрудником отдела ГОиВ Бабиченко Г.Г. с использованием материалов медицинских журналов и газет, медицинских Интернет-ресурсов, а также информации пресс-служб Роспотребнадзора РФ.
Мем антибиотик что происходит
Информация о доставке будет отображаться для региона:
Москва Да, выбрать Нет, выбрать другой город

Информация о доставке будет отображаться для региона:
Москва Да, выбрать Нет, выбрать другой город
О пользе и вреде антибиотиков ведется немало разговоров, и многие уже давно знают, что у них очень много побочных действий. Они подавляют иммунитет, на фоне их приема может возникнуть аллергическая реакция и развиться дисбактериоз, они вредны для слизистой внутренних органов – и это далеко не полный список. Да, многие знают, что применять их можно и нужно только в случаях тяжелых инфекций. Но применяются они, зачастую, без необходимости и без ведома врача. И этому виной их широкое распространение и легкая доступность, они есть практически в каждом доме.
Сейчас ими принято лечить любую болезнь, начиная от банального насморка и заканчивая золотухой. Не врачами, конечно же, а «обычными смертными», хотя и врачи этим грешат, назначая их, когда нужно и не нужно. Однако же стоит знать самые грубые ошибки в применении антибиотиков, а так же случаи, когда они могут применяться, но не являются обязательными.
Итак, самая серьезная ошибка – применение антибиотиков в случаях острой респираторной вирусной инфекции. Современные антибиотики совершенно никак не действуют на вирус, поэтому их назначение теряет всякий здравый смысл. А если учесть прямое действие антибиотика (снижение естественного иммунитета), то его применение может нанести еще больший вред организму и запустить более тяжелую форму имеющейся болезни. Антибиотики назначаются только при серьезных микробных инфекциях, и только после выявления природы инфекции. А для этого, как минимум, нужно сдать анализы в больничной лаборатории.
Следующая распространенная ошибка – самостоятельное удлинение курса приема антибиотиков. Некоторые люди считают, что если пить антибиотики дольше, то организм станет еще здоровее. Но это далеко не так, антибиотик необходим для борьбы с инфекцией, а не для замещения нормальных (природных) функций организма. Если применение антибиотика в течении 3-4 дней является успешным и состояние человека стабилизируется, то курс следует сократить, а не увеличить.
Многие думают, что антибиотики можно пить для профилактики инфекционных болезней. И это еще одна грубая ошибка обычного человека. Антибиотик предназначен для борьбы с микробной средой в организме. Если он ее не обнаруживает, то начинает разрушаться и от действия продуктов распада страдают внутренние органы человека.
Вопреки распространенному заблуждению, антибиотик не понижает температуру тела и не имеет обезболивающего действия. Для этого есть другие препараты, которые не так вредны для организма. Так же, антибиотик не применяется при расстройствах желудочных функций, если речь не идет об инфекции. Но даже, если это и инфекция, то применение антибиотика находится под вопросом, ответ на который может дать только соответствующий специалист и только после проведения обследования. Кроме того, расстройство может носить вирусный характер, быть проявлением аллергии или отравления, дисбактериозом и многое другое. И в таких случаях, антибиотик просто противопоказан.
Нельзя часто употреблять один и тот же антибиотик. Организм привыкает к его действию и вырабатывается устойчивость, в следующий раз придется выбирать более сильнодействующий препарат.
Ошибочно употреблять какой-то конкретный антибиотик только потому, что он помог в лечении другому человеку. Каждый случай индивидуален и назначение антибиотика должно происходить после проведения обследования.
Об этих ошибках должен знать каждый человек. Только зная, он может защитить свою семью и себя самого от нанесения вреда организму. Да, антибиотики важны и нужны, но только как крайний случай, а не норма при любой болезни.
Мем антибиотик что происходит
Изображение носит иллюстративный характер
Основные ошибки приема антибиотиков в домашних условиях.
О пользе и вреде антибиотиков ведется немало разговоров, и многие уже давно знают, что у них очень много побочных действий. Они подавляют иммунитет, на фоне их приема может возникнуть аллергическая реакция и развиться дисбактериоз, они вредны для слизистой внутренних органов – и это далеко не полный список. Да, многие знают, что применять их можно и нужно только в случаях тяжелых инфекций. Но применяются они, зачастую, без необходимости и без ведома врача. И этому виной их широкое распространение и легкая доступность, они есть практически в каждом доме.
Сейчас ими принято лечить любую болезнь, начиная от банального насморка и заканчивая золотухой. Не врачами, конечно же, а «обычными смертными», хотя и врачи этим грешат, назначая их, когда нужно и не нужно. Однако же стоит знать самые грубые ошибки в применении антибиотиков, а так же случаи, когда они могут применяться, но не являются обязательными.
Итак, самая серьезная ошибка – применение антибиотиков в случаях острой респираторной вирусной инфекции. Современные антибиотики совершенно никак не действуют на вирус, поэтому их назначение теряет всякий здравый смысл. А если учесть прямое действие антибиотика (снижение естественного иммунитета), то его применение может нанести еще больший вред организму и запустить более тяжелую форму имеющейся болезни. Антибиотики назначаются только при серьезных микробных инфекциях, и только после выявления природы инфекции. А для этого, как минимум, нужно сдать анализы в больничной лаборатории.
Следующая распространенная ошибка – самостоятельное удлинение курса приема антибиотиков. Некоторые люди считают, что если пить антибиотики дольше, то организм станет еще здоровее. Но это далеко не так, антибиотик необходим для борьбы с инфекцией, а не для замещения нормальных (природных) функций организма. Если применение антибиотика в течении 3-4 дней является успешным и состояние человека стабилизируется, то курс следует сократить, а не увеличить.
Многие думают, что антибиотики можно пить для профилактики инфекционных болезней. И это еще одна грубая ошибка обычного человека. Антибиотик предназначен для борьбы с микробной средой в организме. Если он ее не обнаруживает, то начинает разрушаться и от действия продуктов распада страдают внутренние органы человека.
Вопреки распространенному заблуждению, антибиотик не понижает температуру тела и не имеет обезболивающего действия. Для этого есть другие препараты, которые не так вредны для организма. Так же, антибиотик не применяется при расстройствах желудочных функций, если речь не идет об инфекции. Но даже, если это и инфекция, то применение антибиотика находится под вопросом, ответ на который может дать только соответствующий специалист и только после проведения обследования. Кроме того, расстройство может носить вирусный характер, быть проявлением аллергии или отравления, дисбактериозом и многое другое. И в таких случаях, антибиотик просто противопоказан.
Нельзя часто употреблять один и тот же антибиотик. Организм привыкает к его действию и вырабатывается устойчивость, в следующий раз придется выбирать более сильнодействующий препарат.
Ошибочно употреблять какой-то конкретный антибиотик только потому, что он помог в лечении другому человеку. Каждый случай индивидуален и назначение антибиотика должно происходить после проведения обследования.
Об этих ошибках должен знать каждый человек. Только зная, он может защитить свою семью и себя самого от нанесения вреда организму. Да, антибиотики важны и нужны, но только как крайний случай, а не норма при любой болезни.
Вывод
Беспечное отношение ведёт к возникновению суперустойчивых микробов, появление которых фармакологическим компаниям пока что удаётся контролировать, изобретая новые препараты. Однако, за последние два десятилетия было изобретено только два вида антибиотиков нового класса. И если в ближайшем будущем ситуация кардинально не изменится, неэффективное применение существующих антибиотиков при первых симптомах респираторного заболевания неизбежно приведёт к проигрышу человечества в борьбе с резистентными микробами.
Как бактерии развивают устойчивость к антибиотикам и почему это так важно
Врачи предупреждают, что если не принимать меры, к 2050 году 10 000 000 человек в мире будут умирать от бактерий, которые стали устойчивыми к антибиотикам.
Именно по этой причине ВОЗ призывает все страны участвовать в борьбе с ростом резистентности к антибиотикам. Что касается России, то у нас уже разработан план мероприятий на 2019–2024 годы, в котором предусмотрены соответствующие шаги.
Но что еще важно знать о проблеме? «Аргументы и Факты» пригласили известных врачей, экспертов и ученых для обсуждения — и вот к каким выводам они пришли.
Как бактерии становятся устойчивыми
Заведующий кафедрой фармакологии Института клинической медицины Первого МГМУ им. И. М. Сеченова, доктор медицинских наук Владимир Фисенко рассказал, что бактерии, как и любые микроорганизмы, стремятся избежать гибели, используя разные механизмы для этого.
Создание новых антибиотиков направлено во многом на преодоление этих механизмов защиты бактерий.
С чего все началось
Генеральный секретарь Российского научного медицинского общества терапевтов, заместитель начальника управления науки ГБОУ ВПО «МГМСУ им. А. И. Евдокимова» Минздрава России, главный внештатный специалист-пульмонолог Министерства здравоохранения РФ по ЦФО Андрей Малявин заострил внимание на двух проблемах, которые привели к существенному росту антибиотикорезистентности.
Например, во Франции из-за этого синтетические антибактериальные средства – фторхинолоны — стали неэффективны при лечении пневмонии (воспаление легких). В России при этой инфекции активно использовали антибиотики из группы макролидов, и к ним пневмококки стали устойчивы. В новых рекомендациях для врачей по лечению пневмонии, снова советуем начинать лечение с пенициллинов, они сохранили свою эффективность.
Какие меры будут предпринимать
«Проблема устойчивости к антибиотикам имеет глобальное значение, — подчеркнула представитель ВОЗ в РФ, доктор Мелита Вуйнович. — Это очень важные и полезные лекарства, но только тогда, когда применяются рационально и по назначению. Сегодня в мире каждый год из-за инфекций, вызванных микроорганизмами, резистентными к антибиотикам, погибает 700 тысяч человек.
Важно, что стратегия «Единого здоровья» — единственно возможная мера для сохранения эффективности антибиотиков. Она охватывает сферы защиты здоровья людей, животных и окружающей среды, и разработана ВОЗ, FAO (Продовольственная организация ООН) и OIE (Всемирная организация по охране здоровья животных).
Один из эффективных способов защиты человека от резкого роста устойчивых бактерий, запрет на использование антибиотиков в качестве стимуляторов роста в животноводстве и применение их для лечения в сельском хозяйстве только в исключительных случаях. Конечно, необходимо правильное и рациональное использование антибиотиков в лечении человека».
Эволюция наперегонки, или Почему антибиотики перестают работать
Энтеробактерии (Enterobacteriaceae), обработанные карбапенемом. В правой чашке Петри — колонии, устойчивые к антибиотику.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Начиная ещё со времён открытия пенициллина, человечество постоянно ведёт своеобразную «гонку вооружений» с миром бактерий, которые научились оперативно адаптироваться вслед за появлением новых антибиотиков. И, увы, на сегодняшний день в этой гонке мы начали постепенно отставать от противника. Перед лицом угрозы остаться беспомощными, когда появятся новые, «пуленепробиваемые» инфекции, учёные запасаются своим козырями в рукаве. Проблема стоит крайне остро — или успеть найти оптимальную замену антибиотикам в ближайшее десятилетие, или погрузиться в новое Средневековье, каждодневно рискуя умереть от самой ничтожной царапины.
Конкурс «био/мол/текст»-2014
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2014 в номинации «Лучший обзор».
Главный спонсор конкурса — дальновидная компания «Генотек».
Конкурс поддержан ОАО «РВК».
Спонсором номинации «Биоинформатика» является Институт биоинформатики.
Спонсором приза зрительских симпатий выступила фирма Helicon.
Свой приз также вручает Фонд поддержки передовых биотехнологий.
Благодаря естественному отбору мы развили в себе способность к сопротивлению; мы не уступаем ни одной бактерии без упорной борьбы.
Герберт Уэллс. Война миров
«Порой находишь то, чего вовсе не ищешь»
Сэр Александер Флемминг
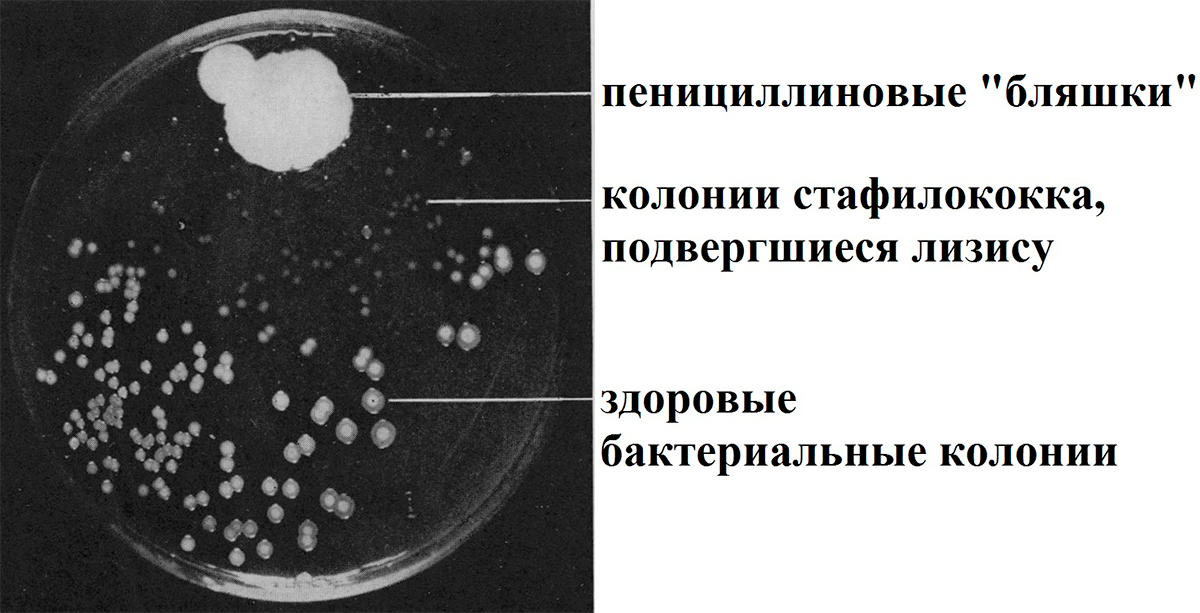
Слава и мировое признание в науке — штука капризная и непредсказуемая. Многие слышали историю об открытии Александром Флемингом первого из антибиотиков — пенициллина, — в которой, казалось бы, пустяковая случайность сыграла ключевую роль. В 1928 году в чашку для культивации бактерий, забытую на столе в его лаборатории, случайно попал плесневый гриб рода Penicillium, и Флеминг обратил внимание, что колонии микроба гибнут (лизируются) рядом с бляшкой плесени.
Кстати, достаточно много Нобелевских лауреатов, к числу которых относится и Флеминг, работали в научных подразделениях фармацевтических компаний: «Кузница нобелевских кадров» [1]. — Ред.
Однако далеко не все знают, что до Флеминга пенициллин открывали ещё несколько раз, правда, с меньшим успехом. За 60 лет до описываемых событий английский физиолог и по совместительству офицер медицинской службы баронет сэр Джон Бардон Сандерсон в своем докладе Кабинету Министров Великобритании упоминал о грибковой плесени, подавлявшей распространение «микрозимов» (так он называл бактерии) в тканях и жидкостях живых организмов. Но доклад — это совсем не то, что публикация в научном журнале. Поэтому полученные им данные так и не стали достоянием широкой общественности.
Рисунок 1. Фото чашки Петри из знаменитой статьи Александра Флеминга. Хорошо видна «мертвая зона» между бляшкой плесневого грибка и колониями бактерий.
Спустя год, вдохновленный успехами своего коллеги, Джозеф Листер — профессор клинической хирургии Эдинбургского университета — посчитал, что Penicillium glaucum (та самая голубая плесень, хорошо знакомая любителям сыров) может неплохо послужить ему в качестве антисептика при проведении операций. И даже испробовал его на пациентке; тогда на вопросы этичности подобных вещей смотрели несколько проще. Пациентка выжила, однако Листер по какой-то причине тоже не потрудился опубликовать результаты своего эксперимента, и научный мир ничего не узнал о нём.
С тех пор пенициллиум ещё не раз попадал в поле зрения учёных, систематически наблюдавших и описывавших его способность угнетать рост бактерий. Тем не менее именно Флемингу с его настойчивостью удалось довести дело до конца [2].
На следующем этапе необходимо было выделить из культуры грибка активное вещество в чистом виде и научиться правильно им пользоваться. Первые попытки применить его на практике напоминали игру в рулетку, поскольку было неясно, кого первым убьет лекарство — возбудителя болезни или самого пациента. Позднее эту проблему удалось решить Говарду Флори и Эрнсту Чейну из Оксфордского университета. Определение безопасной дозы и расшифровка химической структуры позволили наладить массовое производство пенициллина уже к середине второй мировой войны, что оказалось как нельзя более вовремя [3].
Начиная с середины ХХ века, новые антибиотики начали появляться один за другим, и сперва на них возлагали большие надежды. Однако спустя некоторое время стало понятно, что быстрой и окончательной победы над инфекционными заболеваниями с их помощью, скорее всего, ждать не следует.
Что такое «антибиотик»?
Во-первых, сам термин «антибиотик» обозначает совершенно не то, что под ним часто подразумевают. При буквальном переводе слова можно подумать, что это нечто вроде ДДТ — «уничтожающее все живое». На самом же деле в фармакологии антибиотиками называют препараты природного или полусинтетического происхождения, воздействующие на бактерии, и только на них. Не говоря уже о том, что в природе антибиотики чаще всего используются вообще не для убийства. Микроорганизмы вроде плесневого грибка продуцируют их, чтобы отпугивать конкурентов за экологическую нишу, то есть функция у антибиотиков примерно такая же, как у репеллента от комаров. Подобная же путаница, кстати, получилась и со словом «микроб», которому часто придают негативный оттенок, считая синонимом «болезнетворной бактерии». Хотя вообще-то микроб — это просто микроскопический (условно: невидимый невооруженным глазом) организм, необязательно конфликтующий с человеком.
«В пятидесяти случаях из ста даже лучшие из них не знают, как вас лечить»
Агата Кристи
Фокус в том, что инфекция может быть действительно вызвана злыми бактериями, а может и чем-то другим — например, археями, грибами или даже протистами. И против всего этого великолепия антибиотики едва ли будут эффективны. С вирусами — ещё хуже. Вылечить антибиотиком какой-нибудь грипп или ОРВИ у вас не будет вообще ни единого шанса. В отличие от бактерии — клеточной структуры, обладающей собственным геномом, белоксинтезирующим аппаратом, ферментами метаболизма и проч., — вирус из всего вышеперечисленного имеет только геном. Фактически это всего лишь молекула ДНК или РНК, упакованная в белковый капсид, которая реплицируется внутри зараженной клетки хозяина, используя ее же ресурс. Этакий саботажник, проникший на чужую фабрику со своими чертежами и штампующий на фабричном станке копии самого себя. Ну не ломать же, в самом деле, ради того, чтобы остановить нарушителя, собственное оборудование!
Согласно данным статьи, недавно вышедшей в журнале Американской медицинской ассоциации [4], в США из десяти пациентов, обратившихся к врачу с жалобами на боль в горле, шестерым прописывают антибиотики. Препаратом выбора по-прежнему остается пенициллин из-за невысокой цены и хорошей переносимости. Между тем эффективен он, только когда инфекция вызвана стрептококком группы А, а это всего лишь один случай из десяти [5]. Выходит, что врач, прописывающий вам антибиотик при болях в горле, чаще всего либо не уверен в диагнозе, либо банально перестраховывается.
Более того, даже если причина инфекции в бактерии, это вовсе не гарантия, что конкретный антибиотик на нее подействует. Все зависит от того, с каким видом или даже штаммом приходится иметь дело. С одной стороны, это и хорошо, ведь в здоровом организме всегда присутствует своя микрофлора, которая живет с ним в благополучном симбиозе и которую лучше не трогать. С другой стороны, именно по этой же причине не существует универсальных препаратов, которые одинаково хорошо помогали бы от всего сразу. Чтобы не действовать наугад, перед тем как назначить лечение, обычно делают посев культуры из образца, взятого у больного, и поочередно проверяют ее на устойчивость к целому пулу антибиотиков, после чего выбирают наиболее подходящий. К несчастью, процедура эта требует как минимум нескольких дней и наличия микробиологической лаборатории под рукой, а инфекционный процесс часто протекает куда стремительней. И может статься так, что когда придут результаты анализов. лечить будет уже поздно.
Конечно же, исследователи ищут и другие способы диагностики инфекций на ранних стадиях, например, Алан Джармуш из Универистета Пурду предложил использовать для этих целей масс-спектральный анализ [6]. Большие надежды возлагают и на ДНК-диагностику возбудителей, хотя до широкого применения этих методов на практике пока ещё далеко.
Как это всё работает?
Этот список не полон, существуют и другие группы антибиотиков. Так или иначе, почти всегда их мишень — это белок, будь то бактериальный фермент, метаболит, элемент цитоскелета, протонный насос или что-то еще [9]. Даже чтобы просто попасть внутрь клетки, антибиотику сперва необходимо пройти сквозь ее клеточную стенку и мембрану по каналам, которые тоже состоят из белков (поринов) [10], [11]. И тут есть два немаловажных момента. Во-первых, белков чудовищно много, и они очень разнообразны, отсюда и разнообразие антибиотиков. Каждый из них поражает «свой» белок — и безвреден для всех микроорганизмов, у которых такого белка нет. Но куда страшнее то, что белки легче и быстрее, чем другие соединения (углеводы, фосфолипиды и т. д.), подвержены адаптивным изменениям. Именно это лежит в основе масштабной проблемы, которая пока не проявляет себя в полную силу, но уже маячит на горизонте и в скорой перспективе грозит обернуться нешуточной катастрофой. Речь идет об умении бактерий достаточно быстро — за считанные месяцы — вырабатывать устойчивость (резистентность) к любому антибиотику [12].
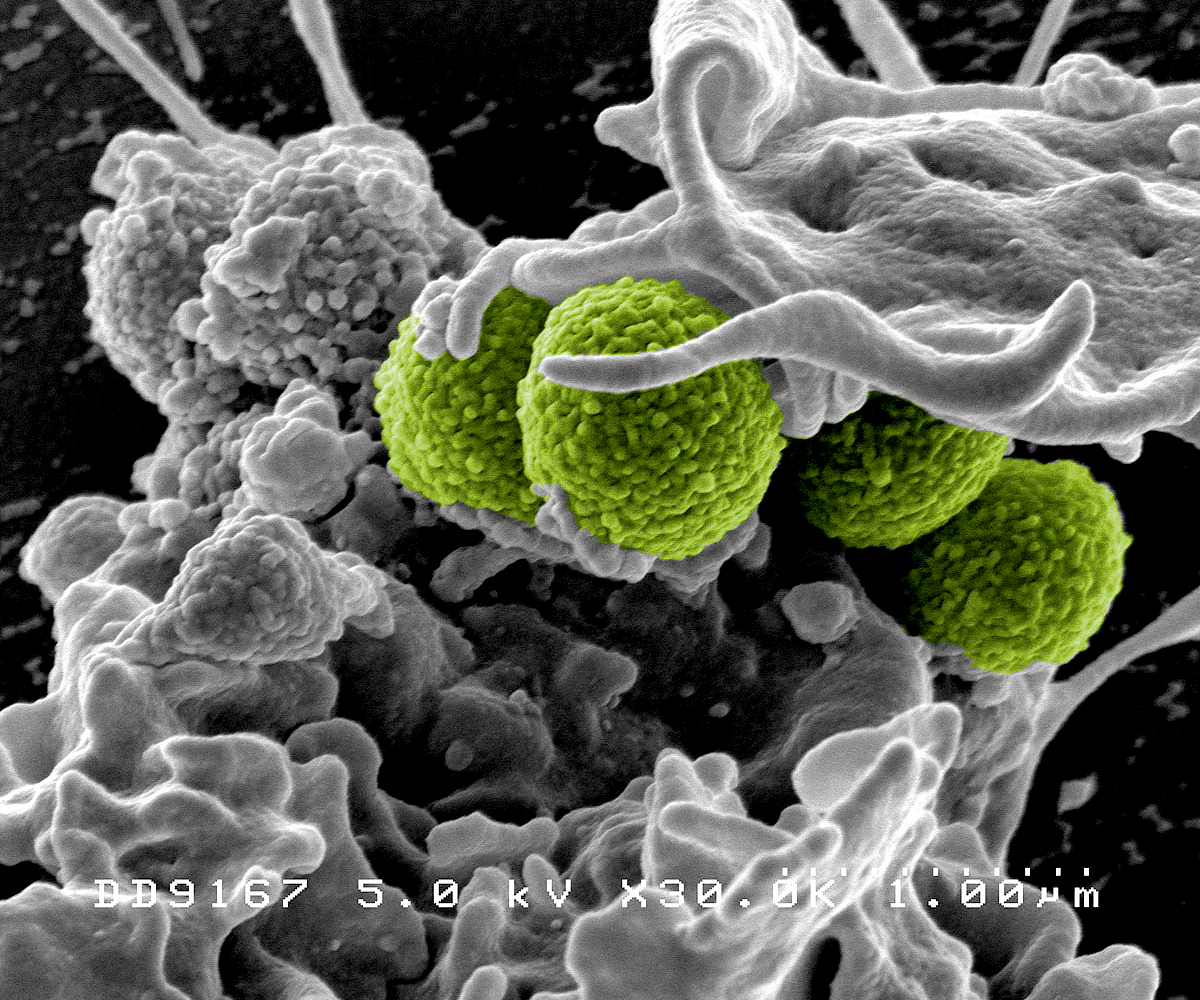
Рисунок 2. Взаимодействие метициллин-устойчивого золотистого стафилококка (жёлтый) и лейкоцита человека. Штамм MRSA252 является одной из наиболее частых причин госпитальных инфекций в США и Великобритании.
«Выживает сильнейший»
Чарльз Дарвин
Очевидно, что чем проще устроен механизм, тем легче его и починить «на коленке», и улучшить технические характеристики, не затрачивая слишком много времени. Бактерии — весьма простые устройства. Когда у тебя всего одна клетка, нет необходимости то и дело разбирать ядро и распаковывать хромосомы, геном не перегружен множеством регуляторных элементов, и весь генетический материал экономно используется для поддержания лишь самых необходимых жизненных функций, то и адаптировать его под изменившиеся условия куда проще. Жизнь у бактерии короткая — минут 20–30. Но если ей ничто не помешает, то заканчивается она обычно делением. Иными словами, через каждые полчаса на месте одной клетки будут уже две, а к концу суток успеет смениться около семидесяти поколений. Поэтому с эволюционной с точки зрения, время для бактерий течёт быстрее, чем для нас, а значит, и естественный отбор работает тоже быстрее. Каким бы мощным ни был антибиотик, всегда есть шанс, что среди миллиарда его жертв найдется хотя бы одна, которая устоит благодаря случайно приобретенной мутации. А сумев выжить, получит эксклюзивную возможность размножиться и передаст эту способность выживать дочерним клеткам, а те, в свою очередь — своим. Из потомков уцелевших бактерий рано или поздно сформируется популяция, совершенно невосприимчивая к старому антибиотику — в точности по Дарвину [13].
Рисунок 3. Лекарства составляют основу современной медицины
Сходным образом приспосабливаются и высшие организмы, находящиеся под постоянным прессингом. Насекомые, вредящие сельскохозяйственным культурам, вырабатывают устойчивость к пестицидам, разве что у них это занимает гораздо больше времени. Бактерии же, мало того, что размножаются быстро, но и умеют «по-соседски» обмениваться генами непосредственно друг с другом (это называется «горизонтальный перенос генов»). Всё это только ещё больше ускоряет их адаптацию к новым условиям.
«Мир стоит на пороге пост-антибиотиковой эры»
Маргарет Чан, глава Всемирной организации здравоохранения
В результате после запуска любого антибиотика в продажу его эффективность начинает со временем снижаться, стремясь к нулю. Некоторых бактерий сегодня не берет уже практически ничего. В англоязычной прессе для обозначения штаммов, устойчивых к нескольким антибиотикам сразу, был даже придуман термин — «superbugs». Так, согласно результатам исследования, опубликованного в январе 2014 года [14], до половины случаев заражения туберкулезной палочкой на территории РФ приходится именно на них.
Однажды начав масштабное применение антибиотиков в клинической практике, человечество вступило в гонку вооружений с миром прокариот, и продолжает вести ее по сей день. Микробиологам, химикам, занимающимся органическим синтезом, и фармакологам приходится постоянно подыскивать новые молекулы с более сильными бактерицидными свойствами или менять что-то в структуре уже имеющихся. Конечно, методы молекулярного дизайна [15] позволяют подобрать молекулу, которая будет длиннее или короче исходной, изменить её пространственную структуру и число возможных конформаций, увеличить либо уменьшить гидрофобность и суммарный заряд, свернуть в кольцо или просто случайным образом перетасовать структурные блоки. С помощью компьютерного моделирования (in silico [16]) или искусственных модельных систем можно даже попытаться просчитать ее поведение при взаимодействии с бактериальной мембраной и предугадать, в каком направлении следует искать [17]. Однако человеческая фантазия далеко не безгранична, и вовремя поспевать за обновлениями у соперника уже сейчас получается с немалым трудом. Дальше будет только сложнее, и в какой-то момент разработка новых антибиотиков просто закончится инновационным кризисом (некоторые данные, впрочем, позволяют предположить, что он уже наступил).
Рисунок 4. Устойчивость бактерий к антибиотикам — одна из серьезнейших проблем в фармакологии
Ухищрения, предпринимаемые ВИЧом для обхода барьеров нашей иммунной системы, невероятны [18], однако в некоторых случаях и ему можно подставить подножку [19]. — Ред.
Аналогичная история произошла в 1918 году с «обычным» гриппом, когда он совершил прыжок со своего природного носителя — птиц — на человека. Потери человечества тогда составили десятки миллионов человек: «Объяснена различная вирулентность вирусов гриппа — возбудителей „испанки“» [20]. — Ред.
Единственное, что обнадеживает, — в случае глобальной пандемии, угрожающей человечеству вымиранием, естественный отбор начнет работать уже в нашу пользу, по принципу маятника. Те из особей Homo sapiens, которым повезет остаться в живых, наверняка передадут своим потомкам собственный иммунитет к инфекции, и начнется новый виток затяжной войны. Но «победа» в ней будет стоить слишком дорого.
Новейшие виды оружия
Можем ли мы выиграть эту гонку, в которой у бактерий столь явное преимущество? На самом деле альтернативы антибиотикам существуют. Некоторые из этих средств находятся на стадии изучения, другие — на стадии клинических испытаний. Третьи вообще не требуют медицинского вмешательства и основываются исключительно на здравом смысле.
SOS-репарация бактерий
Разумеется, самой простой и логичной идеей было бы если не помешать бактериям эволюционировать, то хотя бы искусственно притормозить этот процесс [22]. Как это осуществить на практике, впервые продемонстрировала группа Флойда Ромсберга [23]. Задача, которую исследователи поставили перед собой, заключалась в том, чтобы научиться управлять системой бактериального SOS-ответа, или SOS-репарации. Это явление хорошо известно микробиологам и было описано в научной литературе еще лет тридцать тому назад [24].
В обычных условиях репликация генома проходит с довольно высокой точностью, несмотря на неизбежные ошибки. В основном благодаря тому, что фермент, копирующий ДНК (у бактерий это ДНК-полимераза III), обладает, помимо прочего, еще и (3′, 5′)-экзонуклеазной активностью. Это значит, что если в растущую смысловую цепь случайно попадёт нуклеотид, не комплиментарный своему партнёру на матрице, он тут же будет вырезан и заменен на «правильный». Однако когда дела у клетки начинают идти хуже некуда (например, при высокой концентрации антибиотика в среде), и в ее хромосоме накапливается слишком много повреждений, становится ясно, что тот геном, который есть на текущий момент, вообще не годится для выживания. Тогда, чтобы хоть как-то спастись, клетка идет ва-банк и включает механизм SOS-репарации. Вместо «аккуратной» ДНК полимеразы III, исправляющей за собой ошибки, начинают работать совсем другие белки, которые просто подставляют в поврежденные участки что попало в расчете на слепое везение. Шансы на успех такого предприятия мизерны, и чаще всего клетка погибает оттого, что ее жизненно важные гены оказываются безнадежно испорченными. Но если это вдруг сработает, то из обычной бактерии может получиться нечто совсем непохожее на «предков», и возможно, крайне живучее [25].
Контролируют SOS-систему два белка — RecA и LexA. Первый играет роль активатора; второй — репрессора. Пока все спокойно, LexA постоянно сидит на операторной области SOS-генов (SOS-боксе), не давая их прочесть и запустить — до тех пор, пока в распоряжении его оппонента не попадает фрагмент одноцепочечной ДНК. Связавшись с ней, RecA образует что-то вроде длинной нити (филамента), которая заставляет репрессор отсоединиться от операторной области и запускает SOS-репарацию. Как только запасы однонитевых фрагментов ДНК иссякают (т. е. когда все отремонтировано), LexA снова садится на свое место, и процесс прекращается.
Целью работы Ромсберга и его коллег был поиск низкомолекулярных соединений, которые не давали бы репрессору покинуть оператор ни при каких условиях, тем самым постоянно держа гены SOS-ответа выключенными. Им удалось отобрать несколько таких ингибиторов, способных работать в клетках E. coli в присутствии антибиотиков ципрофлоксацина и рифампицина, однако до клинических испытаний препарата дело так и не дошло.
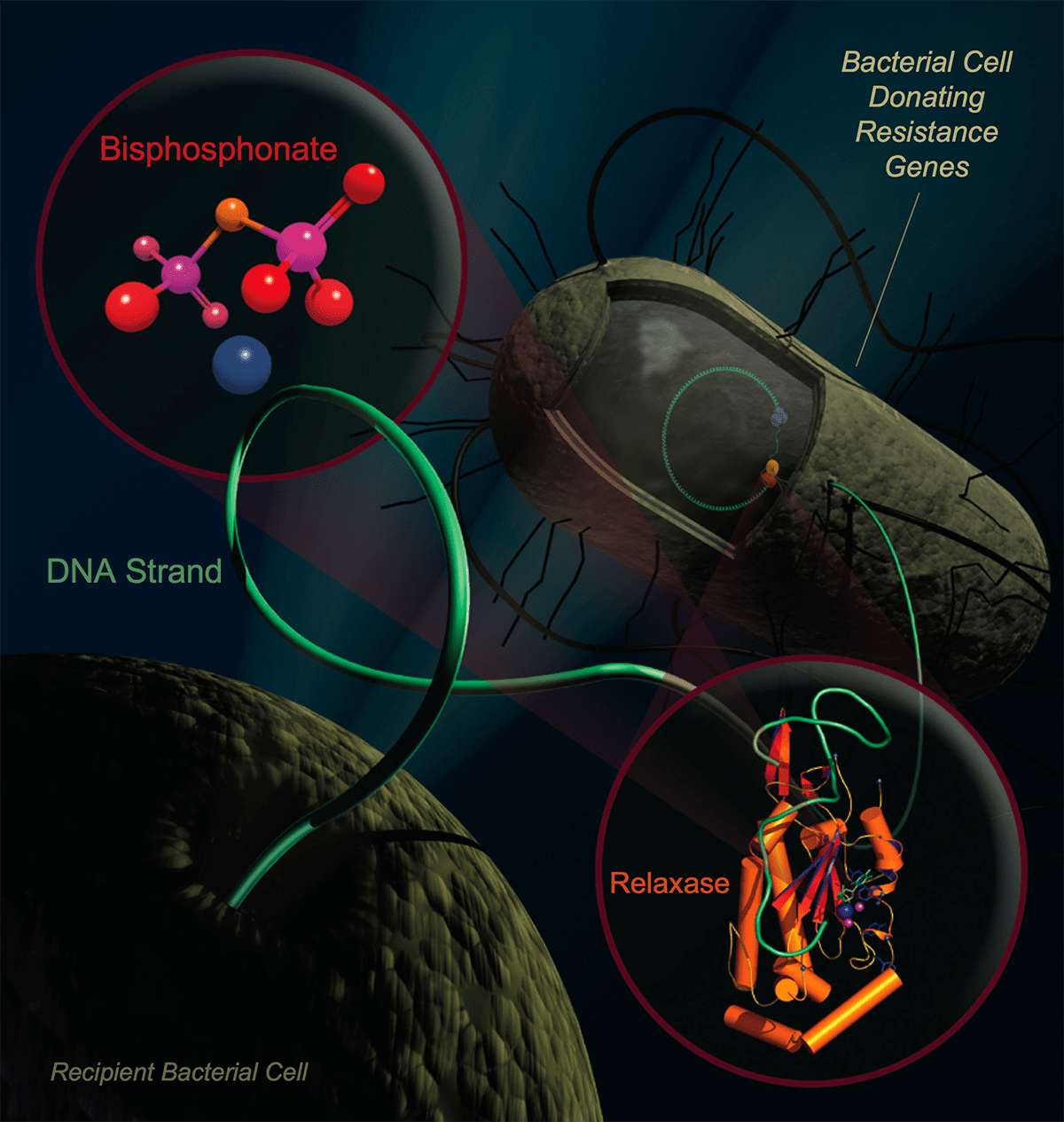
Рисунок 5. Горизонтальный перенос генов у бактерий
Бактериофаги
Другой подход к решению проблемы — использовать против возбудителей инфекций их природных врагов. Бактериофаги — вирусы бактерий — сами способны эволюционировать не хуже своих жертв и за счет этого обходить механизмы их резистентности [26]. Одна из причин, по которой фаговая терапия пока мало представлена на рынке, не в том, что это сложно осуществить технически, а, скорее, в запутанном патентном законодательстве. До сих пор нет единого мнения, считать ли вирус живым. Если да, то право на его использование в коммерческих целях становится намного сложнее получить, поэтому все усилия фармацевтических компаний сводятся к тому, чтобы юридически признать бактериофаг чем-то вроде вакцины или вектора для генетического клонирования [27]. В любом случае, и работать с таким высокоспецифичным и изменчивым лекарством, и писать к нему инструкцию — непростое дело. Есть и другие спорные моменты — например, не до конца ясно, как себя поведет тот или иной фаг, столкнувшись с иммунной системой человека. Да и вообще нет никакой гарантии, что, проникнув в клетку возбудителя, он ее тут же уничтожит. Вместо этого многие фаги предпочитают встроиться в бактериальную хромосому и законспирироваться там на неопределенное время.
Антимикробные пептиды
Куда более «интеллектуальной» мишенью для антибиотиков в мембранах бактерий являются уникальные именно для микроорганизмов молекулы липида-II — вещества, являющегося важным промежуточным звеном синтеза клеточной стенки. На него действуют бактерицидные вещества, называемые лантибиотиками, и данная мишень рассматривается как крайне перспективная для разработки нового класса антибактериальных веществ, не подверженных бремени развития резистентности: «Компьютерное моделирование мембран, липид-II и покрывало Пенелопы» [17]. — Ред.
Понятно, что бактерия погибнет, если целостность ее мембраны будет нарушена. Именно это и делает большая часть антимикробных пептидов (хотя и не все). Молекула, способная проделать дыру в мембране, должна, во-первых, быть небольшой и компактной, чтобы беспрепятственно проскочить сквозь наружную пептидогликановую оболочку, во-вторых, иметь суммарный положительный заряд, достаточный для электростатического притяжения к поверхности мембраны. (Остатки фосфорной кислоты в составе фосфолипидов заряжены отрицательно, что и придает отрицательный заряд мембране бактерии с наружной стороны. А вот внешняя сторона наших с вами клеток по сравнению с бактерией отрицательного заряда практически не несет.) И самое главное — одна половина этой молекулы должна быть гидрофобной, а другая гидрофильной.
Рисунок 6. Фаги атакуют клетку Escherichia coli
“We need public education: not every ill needs a pill”
«Необходимо донести до общественности, что не для каждой болезни нужна таблетка»
Питер Суиниард, председатель Ассоциации семейных врачей Великобритании
Наконец, самая дешевая и общедоступная, но оттого не менее важная мера: здравый смысл и выполнение простых правил. Так уж получилось, что между врачами в мире нет единой договоренности, которая ограничивала бы использование антибиотиков и оставляла бы некоторые из них про запас. В тех странах, где антибиотики можно приобрести без рецепта, их часто держат в домашней аптечке «на всякий случай» и начинают принимать при первых признаках недомогания. Самолечение вместе с незнанием правильных дозировок создают бактериям отличные условия для выработки устойчивости. Лучше приберечь антибиотики на крайний случай, предоставив иммунной системе возможность выполнить свою работу. Но если уж пришлось их принимать, соблюдайте предписания врача — пропейте курс до конца, а не бросайте при первых признаках улучшения.
Как ни удивительно, эпическое сражение бактерий и антибиотиков с неясной концовкой предсказал еще сам Флеминг, выступая с нобелевской речью в 1945 году. Ему же приписывается довольно-таки философская фраза о том, что «пенициллин, конечно, помогает, но зато вино делает счастливей». И надо сказать, в чем-то он здесь неуловимо прав.
Первоначальная версия статьи опубликована в «Химии и жизни» [31].