Что показывает анализ крови на онкомаркеры
Чтобы узнать, что показывает анализ крови на онкомаркеры, необходимо правильно подготовиться и сдать его в первой половине дня. Сделать это можно в лаборатории как при клинике, так и в частном независимом медицинском учреждении с хорошей репутацией. Отметим, что цена анализа крови на онкомаркеры зависит от того, какой маркер нужно проверить, сколько всего таких тестов назначено и надежности выбранной лаборатории.
О чем говорят результаты анализа на онкомаркеры
Онкомаркеры – специфические белковые соединения, которые продуцируются патологическими образованиями в организме либо здоровыми клетками с целью защитить организм от зловредных процессов. В зависимости от этого есть маркеры, которые постоянно присутствуют в организме в минимальном количестве, и есть те, которые появляются только при наличии опухоли. Таким образом, необходимо знать, что показывает анализ крови на онкомаркеры группе риска и тем, кто однажды сталкивался с онкологией.
Данный анализ не назначается в случае отсутствия симптомов, генетической предрасположенности к раку. Лишь в исключительных случаях может быть показан лицам старше 50 лет, которые заняты на вредных производствах.
Результаты тестирования в данном случае могут показать наличие патологического уплотнения на ранней стадии (в зависимости от онкомаркера за 3-5 месяцев до проявления первых симптомов рака), воспалительного заболевания, доброкачественного новообразования, риск патологии у плода. Все это говорит о важности анализа на онкомаркеры в современной диагностике опухолей и патологий развития эмбриона.
Когда нужно сдавать кровь на маркеры и как подготовиться
Сразу отметим то, что показывает анализ крови на онкомаркеры, не является диагнозом. Это лишь первый шаг, который может нести до 95% отображения происходящего в организме. Поэтому проверке нормы онкобелка всегда сопутствуют другие способы обследования, в частности, магниторезонансная и компьютерная томография, ультразвуковое исследование, рентгенография.
Основными показаниями к анализу являются:
| Диагностика раннего определения ракового уплотнения. |
| Проверка наличия метастазов на фоне отсутствия каких-либо симптомов. |
| Составление максимально подходящей и эффективной лечебной программы онкоболезни, подбор лекарственных препараторов и их дозировки. |
| Контроль и оценка результативности выбранной программы лечения и эффективности применяемых препаратов. |
Проверка нормы онкомаркеров назначается группе риска и лицам после 50 лет, так как с возрастом продукция этих веществ увеличивается.
Отметим, что анализ крови на онкомаркеры у женщин и мужчин берется только на каждый вид отдельно, согласно назначению доктора. В зависимости от предположительной локации опухоли для ее выявления может быть достаточно проверить только один маркер. Но чаще всего полную картину дает группа, которая наилучшим образом сочетается между собой.
Подготовка в большинстве случаев не требует особых действий, и она практически аналогична требованиям к анализу на биохимию крови:
| Отказ от пищи за 4-12 часов до начала процедуры. Также следует исключить кофе, чай и соки. Допустима только негазированная вода, в том числе и в день сбора крови. |
| Прекратить употребление лекарственных средств по согласованию с врачом. Если это невозможно, следует обязательно предупредить лаборанта об этом. |
| Исключить алкоголь и курение за 12 часов до начала (это касается и кальяна, курения различных ароматических табаков и электронных сигарет). |
| Постараться не посещать массажиста, не подвергаться диагностическим манипуляциям за несколько часов до тестирования. |
| Снизить физическую активность. Достаточно неспешных прогулок. |
Также по возможности необходимо предупредить стрессовые ситуации и не нервничать. Помните, что соблюдение данных требований позволит получить качественный и достоверный результат.
Женщинам планировать анализ нужно исходя из периода менструального цикла. Выбрать подходящий день, когда гормональный фон оптимален, поможет соответствующий специалист.
Техника проведения проверки крови на онкобелки

Перед началом пациента усаживают на кушетку (в некоторых случаях нужно занять лежачее положение), затем берут кровь из вены традиционным способом при помощи шприца и переносят материал в пробирку с крышкой.
Полученная кровь проходит обработку в специальном оборудовании, где отделяется сыворотка от плазмы. Полученная сыворотка – это и есть образец, в который вводят антитела и наблюдают за взаимодействием. Полученная реакция – это результат анализа крови на онкомаркеры, и то, что он показывает, вносится в карточку пациента.
Нормы и расшифровка 10 самых информативных маркеров
Всего в медицине известно более 200 различных онкомаркеров. Но только около 20 признаны наиболее информативными.
Таким образом, имея показания либо предрасположенность к опухолям, необходимо срочно сдать анализ крови на онкомаркеры в инвитро по цене, которая в любом случае будет ниже, чем вероятное лечение.
Онкомаркеры: что показывают, где сдать кровь на онкомаркеры бесплатно
Онкологические заболевания занимают второе место после сердечно-сосудистых патологий среди причин смерти пациентов в России. Негативная статистика связана с поздним обнаружением патологии. По мнению специалистов, с помощью ранней диагностики выживаемость онкопациентов можно увеличить в два раза. Методов для этого предостаточно.
В числе самых распространенных методов ранней диагностики рака – анализ крови на специфические химические соединения – онкомаркеры. По его результатам нельзя точно установить, болен человек раком или нет. Диагностическая ценность исследования состоит в возможности заподозрить начальную стадию заболевания, продолжив исследование клиническими методами.
Что такое онкомаркеры
Онкомаркеры – это специфические биомолекулы, продуцируемые патологически измененными раковыми клетками. Чаще они представляют собой белковые соединения, но могут иметь иную природу: ферментарную, гормональную либо рецепторную. Большинство таких маркеров синтезируют и здоровые клетки организма, но в гораздо меньших количествах.
Впервые термин «онкомаркер» был введен в 60-х годах прошлого века отечественными учеными Гарри Абелевым и Львом Зильбером. Проводя исследования, они обнаружили, что повышение белка АФП, вырабатываемого плацентой во время беременности, характерно для злокачественных новообразований печени. Этот маркер стал первым включенным в клиническую практику опухолевых исследований.
Сегодня выявлены более двух сотен видов специфических соединений, но анализу подлежат только около двадцати.
Маркеры обнаруживаются в различных биожидкостях на начальных стадиях образования злокачественных клеток, в доклинической (бессимптомной) стадии формирования опухоли. Соединения подразделяются на два вида. Маркеры высокой специфичности с большой долей вероятности выявляют определенное заболевание, низкой специфичности — характерны для ряда различных патологий.
По вероятной локализации опухоли специалисты выделяют онкомаркеры:
Врачи неоднозначно относятся к такой классификации. Это связано с тем, что идеального маркера к настоящему моменту не выявлено. Ни один из них не обладает 100% специфичностью, позволяющей однозначно вычленять рак конкретного органа.
Для чего проводят исследование крови на онкомаркеры
Анализ на онкомаркеры чаще используют как оценочный, для определения положительной (либо отрицательной) динамики в терапии рака. Основываясь на его результатах, можно предотвратить развитие рецидива.
В качестве самостоятельной диагностики исследование не рекомендовано из-за большого количества ложноположительных (ложноотрицательных) результатов. Но, в сочетании с другими методиками помогает выявить онкологическое заболевание на раннем этапе.
О чем говорит отклонение от нормы
В онкологии по количеству специфических белков диагностируют стадию заболевания, по их разновидности — вероятное место локализации новообразования.
Кроме рака соединения обнаруживаются при наличии в организме кист, инфицирований, воспалительных процессов, иных доброкачественных патологий.
Внимание: в небольшом количество онкомаркеры присутствуют в крови здоровых людей.
Приведем данные о норме содержания подобных веществ в организме и предполагаемых проблемах при обнаружении отклонений от нее.
| онкомаркер | максимальное нормативное значение | вероятное расположение опухоли | возможные прочие заболевания |
| ПСА | 4 нг/мл | предстательная железа | инфекционный простатит; аденома. |
| СА-125 | 30 МЕ/мл | женская репродуктивная система; поджелудочная железа; ЖКТ; дыхательные органы (редко). | эндометриоз; адемомиоз; воспаления половых органов; заболевания печени. |
| ХГЧ | для мужчин — 2,5 МЕ/мл; 5 МЕ/мл — для женщин | плацента; яичники; яички. | |
| СА-242 | 30 МЕ/мл | поджелудочная железа; прямая и толстая кишки. | воспаления ЖКТ; панкреатит. |
| РЭА | 5 нг/мл | предстательная, щитовидная либо молочная железы; желудок; печень; костная ткань; репродуктивная система; желудок. | патологии печени; полипоз кишечника; патологии поджелудочной железы; болезнь Крона; туберкулез; пневмония; муковисцидоз. |
| Cyfra 21-1 | 3,3 нг/л | мочевой пузырь; бронхи; лёгкие; средостение. | воспаления почек или печени; фиброзы тканей легких. |
| СА-19-9 | 30 МЕ/мл | печень; желчный пузырь; желудок; мочевой пузырь; половая система. | холецистит; холангит, желчнокаменная болезнь; муковисцидоз. |
| СА-15-3 | 38 МЕ/мл | молочная железа; ЖКТ; печень; женские половые органы (поздняя стадия). | цирроз; доброкачественная опухоль груди; аутоиммунные процессы. |
| Б-2-МГ | от 670 до 2140 нг/мл | система кроветворения | аутоиммунные патологии; воспалительные процессы; печёночные заболевания; почечная недостаточность. |
| CA 72-4 | 6,9 Ед/мл | желудок; яичники; матка; поджелудочная или молочная железы. | гинекологические воспаления; кисты; цирроз; аутоиммунные отклонения. |
Отдельно следует отметить маркер АФП. В гинекологии он применяется для оценки состояния течения беременности. В онкологии — сигнализирует о возможном развитии рака печени, яичников, молочной железы, бронхов и легких, ЖКТ.
Для беременных норма АФП по неделям следующая:
Внимание: превышение указанных показателей может свидетельствовать о патологиях в развитии плода.
Кроме того, повышенный АФП — признак гепатита или цирроза.
На основании данных, приведенных в таблице можно сделать вывод, что отклонения в показателях того или иного онкомаркера говорит о вероятности развития ряда различных заболеваний. Основываясь только на содержании в крови специфических белков поставить диагноз не представляется возможным. Чтобы подтвердить (либо опровергнуть) наличие раковой опухоли в организме потребуются дополнительные диагностические процедуры.
Степень достоверности маркеров в онкологии
Анализ содержания данных веществ очень информативен для оценки назначенного терапевтического курса при онкологическом заболевании. В первичной диагностике ни один из них не используется самостоятельно. Это связано с недостаточной специфичностью маркеров.
Достоверность показаний специфических белков можно рассмотреть на примере самых распространенных из них. К таковым относится тест ПСА. Этот онкомаркер нужно сдавать мужчинам для своевременного обнаружения рака простаты. При злокачественных опухолях железы данный показатель действительно превышает норму. Но, он также возрастает, если в простате формируется новообразование доброкачественного характера. Как показывает врачебная практика, у большинства мужчин с повышенным уровнем ПСА рак предстательной железы не подтверждался.
Внимание: бывают случаи, когда недобросовестные доктора в сомнительных клиниках назначают ненужные терапевтические манипуляции. Они не только требуют серьезных финансовых вложений, но и способны спровоцировать серьезные осложнения!
Еще один показательный маркер — CA-125. Он растет в крови женщин, у которых обнаружен рак яичников, но может повышаться при большом количестве иных патологий, не связанных с онкологией.
Медицине известны случаи, когда на поздних стадиях формирования злокачественных новообразований в яичниках, анализ крови не показывал отклонений в результатах ни по одному из 28 специфических для данного заболевания белковых соединений.
СА-125 не рекомендовано исследовать на начальных стадиях болезни при отсутствии характерной симптоматики. Для анализа течения диагностированной патологии его рассматривают совместно с иными белками, а также результатами УЗИ.
В составе комплексного обследования сдавать онкомаркеры каждые полгода нужно женщинам с плохой наследственностью либо генными мутациями.
В целом, вопрос о том, насколько можно доверять онкомаркерам, на сегодняшний день остается открытым. При расшифровке результатов исследования следует обращать внимание на ряд факторов, способных исказить данные:
Это наиболее распространенные нюансы, но могут быть и другие «тонкости». Разобраться в них способен только квалифицированный врач, который сможет грамотно расшифровать результаты.
Показания к анализу на онкомаркеры
Ткани раковой опухоли в период активного роста поглощают питательные вещества и выделяют продукты распада, многие из которых токсичны. Эти процессы отражаются на здоровье человека, вызывая характерную симптоматику.
Любой сбор анамнеза начинается с опроса пациента. Доктора могут насторожить следующие изменения в самочувствии:
Отражается онкологическая патология и на результатах стандартных исследований крови. Общий анализ может выявить рост СОЭ, падение лейкоцитов либо гемоглобина. Негативные изменения отмечаются также в «биохимии» крови.
Для злокачественных новообразований характерно понижение содержания белков, ускорение свертываемости крови, повышение СОЭ.
Подобные результаты исследований сами по себе не говорят о росте патологически измененных клеток, но выступают поводом для дополнительного обследования. В том числе, сдачи анализов на онкомаркеры.
Исключения составляют люди из групп риска, которым эту процедуру рекомендовано проводить регулярно.
К таковым относят пациентов:
Мужчинам после 50 лет тест на ПСА желательно делать ежегодно, для своевременного обнаружения изменений в деятельности предстательной железы. Также анализ показан тем, у кого рак уже диагностирован. Исследования назначают не только пациентам, проходящим лечение, но и успешно излечившимся. Это позволяет купировать возможные рецидивы болезни. Повышает вероятность получения точного результата предварительная подготовка человека к анализу.
Как правильно сдавать кровь на онкомаркеры
Конкретные рекомендации по ограничениям перед забором крови должен дать лечащий врач. Они зависят от того, какой конкретно белок будет исследоваться.
Общие правила следующие:
Может потребоваться соблюдение иных требований. Так, при подозрениях на опухоль простаты желательно 7 дней воздерживаться от половых контактов, на онкомаркеры женской репродуктивной системы кровь лучше не исследовать в период менструации.
Где можно сдать анализ на онкомаркеры
Сдать анализ на онкомаркеры бесплатно (по полису ОМС и направлению терапевта либо онколога) можно в поликлинике. Результат обычно готов уже через день. Однако не во всех медицинских учреждениях есть необходимое оборудование.
Пройти обследование можно в диагностических центрах либо частных клиниках, но самостоятельно принимать решение о его необходимости не стоит. Сдавать кровь надо исключительно по назначению лечащего врача. Специалист даст адекватную оценку состоянию больного, подберет наиболее специфичные соединения для конкретного случая. Исследование на все группы онкомаркеров лишено смысла. К тому стоит не дешево. Цены колеблются в диапазоне от 300 до 2000 рублей за каждое вещество в зависимости от региона и клиники.
Онкомаркеры – эффективные показатели отслеживания опухолевого ответа на проводимую пациенту терапию. В качестве способа первоначального выявления онкологических патологий, точного результата они не гарантируют. С помощью анализа специфических белков можно заподозрить наличие раковых клеток, другие опасные заболевания. Расшифровкой полученных данных должен заниматься врач-онколог. Самодиагностика часто приводит к ошибочным выводам, неправильному лечению и наступлению тяжких последствий для здоровья.
Мáркеры для клеток: как ученые «раскрашивают» клетки, чтобы отличить одну от другой
Выделить все важное и отличить от других — вот задача клеточных мáркеров.
Автор
Редакторы
Статья на конкурс «био/мол/текст»: В этой статье рассказывается о том, как ученые научились в широком смысле «раскрашивать» клетки — выделять из общей смеси только те, которые им интересны, а остальные отсеивать. Речь пойдет как о естественных поверхностных и внутриклеточных мáркерах и способах их выявления, так и о более изощренных генетических способах маркировать клетки. Читателя ждет открытие, что штрих-коды бывают не только в магазинах, но и в клетках, а вирус иммунодефицита человека превратился в послушный инструмент.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

Что первое приходит на ум неискушенному в науке человеку при слове «мáркер»? Бьюсь об заклад, что добрая половина представляет себе желтый широкий фломастер для выделения текста. Другая половина, наверняка, представляет себе черный нестираемый маркер, которым одно время были исписаны все трубы, заборы и веранды. Начертания «Маша + Саша = Любовь» скрепляли чувства подростков навечно, а менее романтичные, но выразительные фразы надолго свидетельствовали о личной неприязни. Встречались даже стихи. Однако предлагаю уважаемым читателям узнать еще одно значение этого слова — очень научное и так нужное всей современной биологии и биомедицине. В научном понимании и конкретно в клеточной биологии, слово «маркер» в широком смысле означает что-то, что отличает одну живую клетку (или группу клеток) от других. Это может быть молекула на поверхности клеточной мембраны, или какой-нибудь внутриклеточный белок, или вещество, которое синтезируется/накапливается только в этом конкретном виде клеток, или генетическая особенность, присущая только данному типу клеток. Условно все маркеры можно разделить на естественные, которые существуют сами по себе, и искусственные — введенные намеренно. Давайте разберемся с ними по порядку.
Естественные клеточные маркеры и способы их рассмотреть
В многоклеточных организмах существует клеточная специализация. Несмотря на то, что клетки содержат одинаковую ДНК, они отличаются друг от друга: клетки мышц умеют сокращаться, нейроны — проводить нервные импульсы, и так далее. Это происходит из-за того, что в каждом виде клеток работает только определенный набор генов из всего их разнообразия, содержащегося в ДНК. Именно поэтому маркером клеток может служить любой ген, который экспрессируется избирательно — только в каком-нибудь конкретном виде клеток. Особенно удобно, когда такой отличительный ген кодирует белок, располагающийся на поверхности клетки.
Раковые маркеры
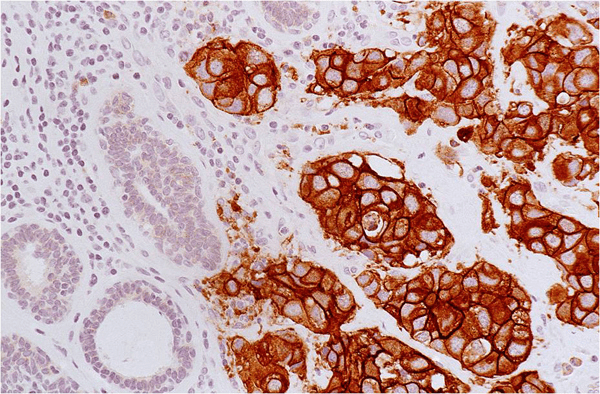
Часто можно слышать слово — «онкомáркер». Это классический пример клеточных маркеров: молекул на поверхности опухолевых клеток, которые или не встречается совсем, или присутствуют в гораздо меньшем количестве на поверхности здоровых клеток. Одним из ярких примеров онкомаркеров является HER2-антиген на поверхности клеток рака груди (рис. 1) [1]. HER2 — рецептор эпидермального ростового фактора. В результате аномального увеличения количества копий гена этого рецептора в опухолевых клетках нарушается регуляция клеточного цикла, и опухоль начинает быстро расти. HER2+-варианты рака груди — очень агрессивны [2].
В этом случае у ученых есть целый набор методов, как можно «увидеть» клетки, несущие такой маркер, отличить их от остальных клеток и даже отсортировать: в одну пробирку — клетки с поверхностным маркером (или с несколькими маркерами), в другую — остальные. Эти методы основаны на использовании антител.
Антитела — специальные белки, которые могут распознавать молекулы за счет пространственного взаимодействия. Именно антитела играют важную роль в нашем иммунитете — они связываются с белками или другими молекулами на поверхности бактерий и вирусов, что и запускает иммунную реакцию. Современная наука научилась делать антитела против практически любых белков — в том числе и против поверхностных клеточных маркеров. Чтобы использовать антитела для определения маркеров, ученые прибегают к еще одной хитрости. Они присоединяют к антителу еще один белок: или фермент, или флуоресцирующий (светящийся) белок. Тогда, если к исследуемым клеткам добавить антитела против поверхностного маркера, связанные с ферментом, потом отмыть лишние антитела и добавить субстрат для фермента, который при расщеплении приобретает какой-нибудь цвет, то клетки, несущие на своей поверхности нужный маркер, окажутся окрашенными, а остальные клетки — останутся бесцветными (рис. 1).
Рисунок 1. Пример выявления онкомаркера HER2 с помощью антител (иммуногистохимия). Коричневые клетки несут на своей поверхности HER2.
Такая модификация выявления маркера называется иммуногистохимией («иммуно» — из-за того, что используют иммунные антитела, «химия» — потому что в методе присутствует химическая реакция расщепления субстрата ферментом, «гисто» — потому что чаще всего такой метод применяют к гистологическим срезам — тонким слайсам исследуемой ткани, которые закреплены на стеклянной подложке).
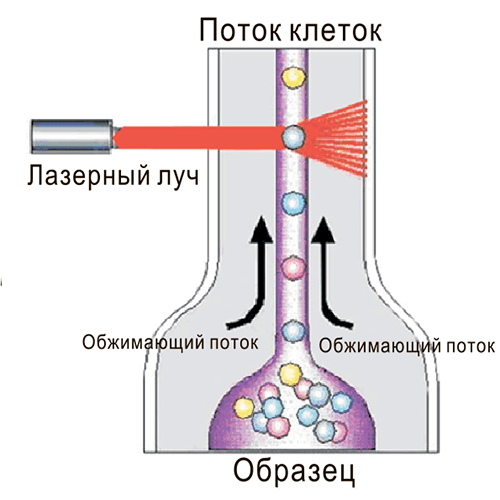
Другой метод, позволяющий выявлять поверхностные маркеры, называется проточной цитофлуориметрией (fluorescence-activated cell sorting, FACS) [3]. Здесь исследуемые клетки (в виде одноклеточной взвеси) смешивают с антителами, к которым присоединены флуоресцирующие белки. Антитела связываются со своими маркерами-мишенями, a не связавшиеся антитела удаляют. Далее клетки загружают в прибор. Он создает тонкую струю из клеточной суспензии, проходящую через свет лазера буквально по одной клетке. Если на поверхности клетки есть искомые маркеры, то вместе с клеткой в луч лазера попадают и антитела, связавшиеся с маркерами. Происходит возбуждение флуорофора на антителе, и он испускает на своей длине волны свет, который и регистрируется детектором (рис. 2).
Рисунок 2. Общий принцип проточной цитофлуориметрии.
После этого прибор может отклонить эту клетку из струи или в одну сторону, или в другую. Таким образом можно разделить клетки на две группы: с маркером и без. Получается, что прибор «знает», есть ли искомые маркеры на каждой из исследуемых клеток, сколько таких клеток, умеет сортировать нужные и ненужные клетки.
Описанные способы позволяют выявлять естественные маркеры — молекулы, которые и до начала исследования присутствовали на поверхности или внутри клеток. Эти методы сильно помогли ученым разобраться в том, чем опухолевые клетки отличаются от нормальных, стволовые клетки — от более зрелых и дифференцированных, и разные ткани — друг от друга.
Искусственные маркеры: внедрить и распознать
У описанных выше методов есть один существенный недостаток: они не позволяют установить родственные связи между клетками. Вот, предположим, у нас есть 100 клеток, и у 12 из них есть маркер А на поверхности. Все эти клетки А для нас будут на одно лицо, как близнецы (рис. 3).
Рисунок 3. Братья-близнецы из фильма «Приключения Электроника».
Мы не сможем сказать, произошли ли все эти 12 клеток от одной материнской и являются ли «близкими родственниками». Или, скажем, можно предположить, что они получились после деления нескольких клеток с исследуемым маркером и являются друг другу двоюродными, троюродными братьями и сестрами, а может быть и вовсе седьмой водой на киселе. Чтобы исследовать родственные связи в клеточной популяции (еще говорят — «исследовать клональный состав популяции» [4]) и следить за тем, как ведет себя потомство отдельных клеток, ученые научились вводить искусственные генетические маркеры в клетки. Делают это несколькими способами. Один из самых продвинутых способов на сегодняшний день — использование специальных вирусов.
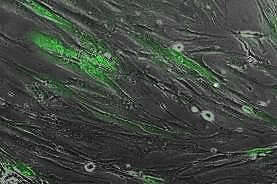
Рисунок 4. Мультипотентные мезенхимальные стромальные клетки (ММСК) человека, маркированные лентивирусом с зеленым флуоресцентным белком GFP.
собственные данные автора статьи, [4]
Современная генная инженерия достигла таких невиданных высот, что специалисты научились конструировать вирусы с заранее известными, тщательно отобранными для целей исследователей свойствами. Например, можно создать вирус, который способен заражать клетку — проникать через ее оболочку в ядро, — встраиваться в ДНК зараженной клетки, и больше ничего не делать: не создавать новые вирусные частицы, не копировать себя в геноме зараженной клетки, не экспрессировать ни один из вирусных генов. Вместо этого ученые смогли заставить вирус, который встроился в ДНК клетки, экспрессировать нужные белки (например, на этом принципе основана генотерапия). В частности, можно сделать так, что с ДНК вируса экспрессируется флуоресцентный белок [5], и зараженная клетка начинает светиться во флуоресцентном микроскопе (рис. 4).
Вирусы, которые способны направленно доставлять гены в ДНК клетки, стали называть вирусными векторами.
Как ВИЧ помогает ученым
На заметку: именно к этому семейству принадлежит вирус иммунодефицита человека (ВИЧ). На его основе придуманы многие генетические векторы. Так что, в руках ученых ВИЧ из возбудителя страшной болезни превратился в послушный инструмент исследования.
Введение вектора в клетки для исследования их клонального состава принято называть маркированием клеток. Вы здесь совершенно справедливо спросите: «Позвольте, а где же здесь маркирование? Ну, ввели мы ДНК вируса в ДНК клетки, но дальше-то что?». А я Вам отвечу, что здесь-то и начинается самое интересное! Введенная ДНК действительно может выступать в роли маркера. Здесь есть два варианта: 1) маркером может служить не сама вирусная ДНК, а то место, куда она встроилась; 2) маркер может содержаться в самой вирусной ДНК.
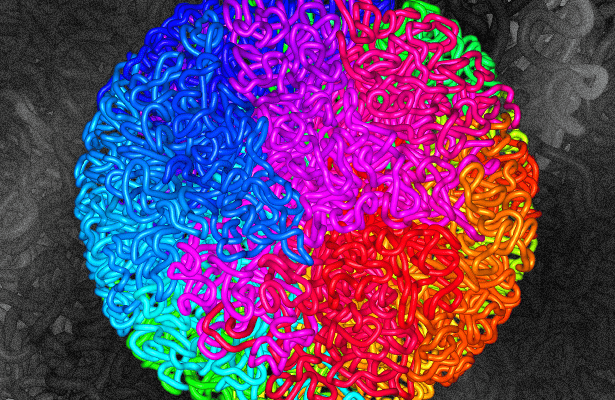
Про то, каким удивительным образом в одном клеточном ядре величиной в несколько микрометров упаковываются молекулы ДНК, длина которых измеряется в метрах, читайте увлекательную статью на «Биомолекуле»: «Организовать геном: запутанная история гипотез и экспериментов» [6].
Рисунок 5. Модель фрактально-глобулярной структуры ДНК. Цветом здесь условно обозначены разные хромосомы.
Соответственно, у одного маленького вируса много возможностей, куда встроиться. В идеале — их бесконечно много, и поэтому найти две клетки, в которых бы вирусы встроились в абсолютно одинаковом месте, — довольно сложно. Еще один важный момент заключается в том, что если зараженная клетка решит поделиться, то обе ее дочерние клетки будут содержать провирус (так называется вирус, который встроился в геномную ДНК) в одном и том же месте генома! Другими словами, генетический маркер — наследуемый признак. Если научиться определять, в какое же именно место генома попал вирус в разных клетках, то можно было бы отличать потомство одной зараженной клетки от другой! И ученые умеют это! Существует несколько методов, позволяющих это сделать, главные из которых — метод саузерн-блоттинга и полимеразная цепная реакция, опосредованная лигированием [7], [8].
Про принцип гибридизации по Саузерну я отсылаю тебя, дорогой читатель, к другой замечательной статье, посвященной описанию важнейших методов молекулярной биологии: «Важнейшие методы молекулярной биологии и генной инженерии» [9]. А о полимеразной цепной реакции расскажет статья «12 методов в картинках: полимеразная цепная реакция» [10].
Оба метода основаны на том, что вследствие случайного характера интеграции вируса в геномную ДНК расстояние от провируса до ближайшего сайта рестрикции будет разным в двух независимо зараженных клетках. Соответственно, если из зараженных клеток выделить ДНК и разрезать ее одной из рестриктаз, то длина фрагмента, содержащего провирус, будет разной у потомства двух разных зараженных клеток, и будет одинаковой у всех клеток, которые произошли в результате деления одной зараженной клетки. Если после рестрикции разделить фрагменты гель-электрофорезом [11], перенести на нитроцеллюлозную мембрану и гибридизовать с короткой последовательностью дезоксирибонуклотидов, комплементарной провирусу (такие олигонуклеотиды принято называть зондами), то на фотобумаге проявится набор полос, который будет одинаковым для клеточного потомства одной клетки и разным — для клеточного потомства нескольких зараженных клеток (рис. 6).
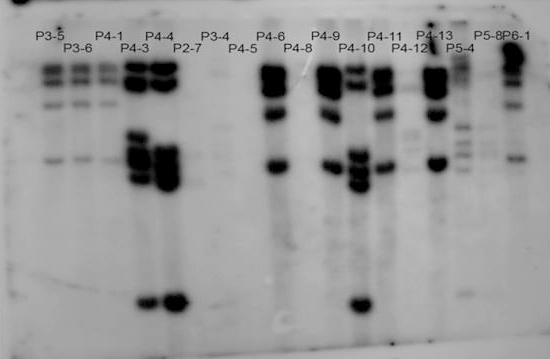
Рисунок 6. Саузерн-блот клеточных клонов, полученных из популяции, зараженной лентивирусным вектором. Каждая дорожка — результат саузерн-блоттинга ДНК из клеточного клона (клеточного потомства одной зараженной клетки). Набор полос в каждой дорожке соответствует продукту гибридизации зонда, комплементарного провирусу, с фрагментами расщепленной ДНК, содержащими провирус. Фрагменты разделены по длине с помощью гель-электрофореза.
собственные данные автора статьи, [4]
Из картинки видно, что на первых трех (и некоторых других дорожках — предлагаю читателю размяться и подсчитать их!) паттерн полос идентичен. Это говорит о том, что ДНК, проанализированная в этих образцах, получена из клеток, произошедших от одной исходно зараженной материнской клетки. Легко также заметить, что дорожка с таинственным названием Р5-4 содержит совершенно другой набор полос. Это означает, что ДНК, использованная здесь, принадлежала другой зараженной клетке. Недостаток такого метода в том, что он не позволяет в явном виде идентифицировать сайт интеграции провируса. Метод позволяет только сравнивать между собой клеточные клоны и судить об их родстве.
Другой метод, который позволяет анализировать сайты интеграции провирусов, — полимеразная цепная реакция, опосредованная лигированием [8]. Это достаточно сложный и многостадийный метод, который включает в себя рестрикцию ДНК, присоединение (лигирование) адаптеров, использование магнитных микрочастиц, ПЦР, электрофорез и секвенирование и заслуживает отдельной статьи. Прошу тебя, мой читатель, поверить мне на слово — этот метод позволяет с точностью до нуклеотида определить место в ДНК, в которое произошла интеграция провируса. С помощью этой методики можно не только различить потомство зараженных клеток между собой, но также судить о том, сколько вирусов проникло в ДНК зараженной клетки, в какие гены произошла интеграция, и не произошло ли изменение их экспрессии в результате внедрения вируса [12], [13].
Ранее я упомянул о том, что в качестве маркера, кроме места интеграции, можно использовать и саму ДНК провируса. Давайте рассмотрим подробнее, как это можно сделать. Здесь нам поможет химический синтез олигонуклеотидов! Дело в том, что в ДНК вируса можно вводить любую информацию: например, ген, кодирующий флуоресцирующий белок или фермент. Правда, тогда все вирусные частицы ничем не будут отличаться одна от другой и приобретут смысл маркеров только тогда, когда попадут в клетку. А почему бы не сделать сами вирусные частицы уникальными? Для этого ученые конструируют лентивирусные векторы, несущие так называемые генетические штрих-коды [14]. Суть заключается в том, что с помощью химического синтеза получают смесь олигонуклеотидов, где в некоторых позициях случайным образом содержится любой из четырех известных дезоксирибонуклеотидов. Дизайн штрих-кода может быть, например, таким:
ATC NNN GGA NNN TAT NNN CGA NNN ATT NNN GTG NNN
Здесь символы N обозначают любой из известных нуклеотидов (А, Т, C или G). Такой штрих-код ничего не кодирует, но он представляет собой смесь нуклеотидов с разными последовательностями. Приведенный штрих-код — на самом деле смесь из 4 18 (или приблизительно 10 11 после несложных, но утомительных математических преобразований) различных олигонуклеотидов! Такая смесь используется для сборки вирусов. На выходе получаются уже не обезличенные вирусы, похожие друг на друга как две капли воды, но целая библиотека вирусов, где каждая вирусная частица несет какой-то из возможных олигонуклеотидов-штрих-кодов. Клетки заражают такой вирусной библиотекой, и каждая зараженная клетка получает в свою ДНК уникальный стабильный наследуемый маркер в виде генетического штрих-кода. Все дочерние клетки будут нести тот же штрих-код (или набор штрих-кодов), который приобрела материнская клетка при заражении. Клеточное потомство двух разных зараженных материнских клеток будет иметь различные штрих-коды. Подобно тому, как штрих-коды на товарах в обычном продуктовом магазине позволяют однозначно идентифицировать и отличить один товар от другого, так генетические штрих-коды позволяют отличить потомство одной зараженной клетки от другой. Если затем из зараженной популяции клеток выделить ДНК и определить все присутствующие в ней штрих-коды с помощью новых методов секвенирования, то можно однозначно установить клональный состав клеточной популяции, проследить за динамикой клонов и выявить те клоны, которые преобладают над другими. После заражения библиотекой лентивирусов со штрих-кодами клеточная популяция становится как будто раскрашенной маркерами с очень-очень-очень разнообразной палитрой [15], примерно вот так (рис. 7):
Рисунок 7. Как выглядела бы клеточная популяция, если бы каждый генетический штрих-код имел свой цвет.
Рисунок 8. Канцелярские принадлежности.