Другие невоспалительные болезни матки, за исключением шейки матки (N85)
Алфавитные указатели МКБ-10
Внешние причины травм — термины в этом разделе представляют собой не медицинские диагнозы, а описание обстоятельств, при которых произошло событие (Класс XX. Внешние причины заболеваемости и смертности. Коды рубрик V01-Y98).
Лекарственные средства и химические вещества — таблица лекарственных средств и химических веществ, вызвавших отравление или другие неблагоприятные реакции.
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97 г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2022 году.
Сокращения и условные обозначения в Международой классификации болезней 10-го пересмотра
БДУ — без дополнительных уточнений.
НКДР — не классифицированный(ая)(ое) в других рубриках.
† — код основной болезни. Главный код в системе двойного кодирования, содержит информацию основной генерализованной болезни.
* — факультативный код. Дополнительный код в системе двойного кодирования, содержит информацию о проявлении основной генерализованной болезни в отдельном органе или области тела.
Внутриматочные синехии
» data-image-caption=»» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/04/vnutrimatochnye-sinehii-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/04/vnutrimatochnye-sinehii.jpg» title=»Внутриматочные синехии»>
Александр Иванов, хирург-гинеколог
Внутриматочные синехии (синдром Ашермана) – редкое, приобретенное, гинекологическое расстройство, характеризующееся формированием спаек в полости матки. При наличии патологии женщин беспокоит нарушение менструального цикла, сильные боли и спазмы в животе, развивается аменорея и бесплодие.
Рубцевание эндометрия и внутриматочные спайки – синехии – чаще всего возникают после хирургического выскабливания. Но есть и другие причины.
Что такое внутриматочные синехии
Патология впервые была описана в 1948 году доктором Ашерманом, который отметил, что у некоторых женщин, проходивших хирургическое лечение матки, впоследствии отсутствовала менструация. После обследования таких пациенток оказалось, что спайки (рубцовая ткань) внутри матки вызывают слипание стенок органа, что приводит к уменьшению или отсутствию менструального цикла. Иногда патология сопровождается болью.
Рубцовая ткань внутри матки, возникающая непосредственно после инфекции малого таза или хирургического вмешательства – симптом патологических внутриматочных синехий. Это состояние отличается от абляции эндометрия, которая проводится специально, чтобы индуцировать рубцовую ткань в матке и предотвратить тяжелые месячные.
Симптомы при наличии внутриматочных синехий
Патология сопровождается следующими признаками:
В некоторых редких случаях менструальный цикл у женщины может быть нормальным.
Важный момент: вышеперечисленные симптомы не уникальны для синдрома Ашермана и могут остаться незамеченными у женщин, которые не пытаются забеременеть.
Причины развития внутриматочных синехий
Существует множество причин развития спаек в матке, но чаще всего патология развивается после хирургического вмешательства в полость матки, особенно после дилатации и кюретажа (D & C).
Более высокая вероятность развития внутриматочных рубцов существует во время и после беременности, поскольку эндометрий в этот момент тоньше и более подвержен повреждениям. Кроме того, в период беременности очень распространены инфекции органов малого таза. Такие заболевания протекают более тяжело по сравнению с обычным состоянием. Заживление повреждений, как правило, приводит к образованию соединительнотканных изменений.
В результате сильного воспаления слизистой оболочки матки, регенерация заканчивается развитием полос рубцовой ткани, которые соединяют части стенок матки друг с другом, уменьшая объем полости матки.
В развитии патологии определенную роль играют женские половые гормоны. Низкий уровень эстрогена предрасполагает к развитию рубцовой ткани в матке. Гипоэстрогения характерна для беременности и кормления грудью, когда преобладающим гормоном в организме остается прогестерон. Высокий уровень прогестерона и низкий уровень эстрогена создают условия, в которых патология может развиваться с большей вероятностью.
Частой причиной развития внутриматочной синехии служат внутриматочные хирургические операции, которые проводятся с целью прерывания беременности, для удаления миомы или исправления структурных дефектов полости матки.
Более редкие, но возможные предпосылки для формирования маточных спаек:
Почему у некоторых женщин развиваются спайки в матке даже после относительно простых процедур или инфекции, в то время как у других женщин такая патология не возникает, до сих пор точно не известно.
Методы диагностики хронического спаечного процесса
Диагностика внутриматочных спаек проводится с помощью гистеросальпингографии (HSG), УЗИ, включая контрастную соногистерографию (SHG), 3D-УЗИ, гистероскопии и магнитно-резонансной томографии (МРТ).
В отношении внутриматочных синехий очень важна дифференциальная диагностика. Гинеколог должен проверить пациентку на заболевания, имеющие сходные симптомы.
Лечение внутриматочных синехий
Лечение внутриматочного спаечного процесса проводится при помощи хирургического вмешательства. Главные задачи хирурга-гинеколога: восстановление размера и формы полости матки и нормализация репродуктивной функции. Для этого применяется операционная гистероскопия, когда спайки срезаются специальными ножницами. Частота успешного анатомического восстановления матки после первой процедуры колеблется от 57,8% до 97,8%.
Для снижения риска инфицирования с первых дней после гистероскопии назначаются антибиотики. В течение примерно трех недель после лечения применяются эстрогенсодержащие препараты. Это необходимо для естественного восстановления эндометрия и снижения риска формирования рубцовой ткани. В конце трехнедельного периода делается перерыв на одну неделю, затем по показаниям курс эстрогенотерапии продолжают.
Повторную гистероскопию проводят через 4, 8 и 12 недель. При повторных осмотрах врач проверяет состояние полости матки, шейки и яичников и оценивает возможность нормального развития беременности.
Как предупредить развитие внутриматочных синехий
Помогут предотвратить формирование спаечного процесса внутри матки несколько простых советов:
При появлении симптомов внутриматочных синехий нужно срочно обратиться в гинекологию и пройти обследование.
Что такое синехии половых губ? Причины возникновения, диагностику и методы лечения разберем в статье доктора Барковской А. Ю., гинеколога со стажем в 5 лет.
Определение болезни. Причины заболевания
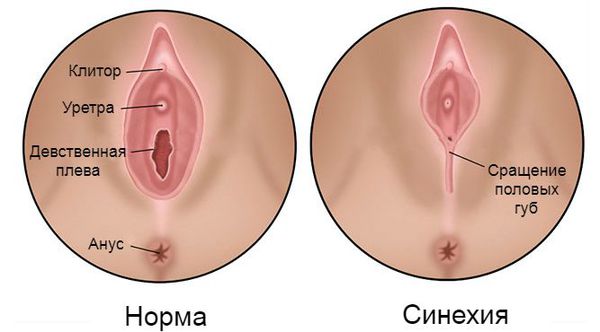
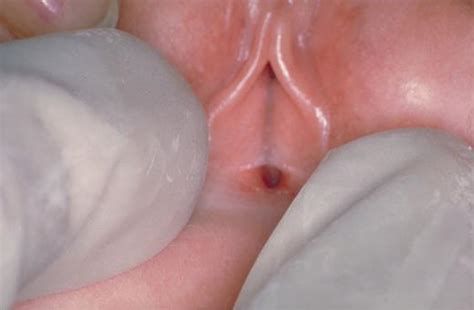
Синехии вульвы — это соединительнотканная мембрана или перемычки, возникшие между малыми половыми губами, которые полностью или частично закрывают преддверие влагалища и уретру.
За последние десятилетия распространённость данной патологии увеличилась. Многие авторы объясняют эту тенденцию активным введением средств гигиены в быт семьи: повсеместное использование подгузников, агрессивных мыльных средств. Также к причинам синехий относится слишком частое ежедневное подмывание наружных половых органов.
Факторы риска развития болезни :
Симптомы синехий половых губ
Клиническая картина появляется тогда, когда сформировавшаяся мембрана нарушает нормальный пассаж мочи. Часто в анатомическом «кармане», образованном синехиями, скапливается моча. В таких случаях родители замечают, что уже после акта мочеиспускания у ребёнка мокнет белье. Также может измениться характер струи: она становится «бьющей» или несформированной.
При полном сращении вульвы возникает острая задержка мочи. Это состояние требует неотложной помощи, так как оно приносит ребёнку выраженные физические страдания.
Патогенез синехий половых губ
Для полного понимания патогенеза синехий малых половых губ необходимо обратиться к обсуждению нормальной анатомии вульвы у детей допубертатного возраста (примерно до 9-12 лет). В норме она представлена такими анатомическими элементами, как большие и малые половые губы, клитор, отверстие уретры, преддверие влагалища и девственная плева.
Большие половые губы с хорошо развитой подкожно-жировой клетчаткой, как правило, прикрывают малые половые губы и преддверие влагалища.
Малые половые губы, в отличие от больших, атрофичны. Они покрыты тонким слоем многослойного плоского эпителия, через который просвечивает богатая капиллярная сеть сосудов. Вот почему покровы этой области имеют ярко красный цвет, что иногда ошибочно трактуется как признак воспаления.
Под передней спайкой малых половых губ расположен атрофичный клитор. Под ним открывается отверстие уретры.
Задняя спайка малых половых губ и мочеиспускательный канал ограничивают преддверие влагалища. Вход в него прикрыт девственной плевой. Слизистая преддверия у девочек также имеет характерный ярко-красный цвет. Это обусловлено тем, что многослойный плоский эпителий у детей состоит из небольшого количества слоёв, клетки которого не созревают и не ороговевают, в них содержится низкое количество гликогена (субстрата для продукции слизи). Сквозь эпителий также просвечивает капиллярная сеть.
При возникновении неблагоприятных факторов (воспаления, аллергической реакции, механической травмы — например, расчёсов) слизистая малых половых губ повреждается. Если в процессе заживления эпителия (пролиферации соединительной ткани) малые половые губы плотно прилегают друг к другу, то между ними могут возникнуть спайки. Формирование синехий может занимать от несколько дней до нескольких месяцев.
Классификация и стадии развития синехий половых губ
Различают полную или частичную форму синехий половых губ.
Частичную форму разделяют на два типа:
Как правило, в обоих случаях частичного сращения наблюдается бессимптомное течение.
Осложнения синехий половых губ
К осложнениям патологии относят инфекционно-воспалительные заболевания органов мочеполовой системы. Их появление связано с нарушением нормального пассажа мочи.
При тотальном или субтотальном сращении малых половых губ происходит острая задержка мочи. Она проявляется болями распирающего характера над лоном (из-за чего ребёнок плачет и кричит), сильными позывами к мочеиспусканию и невозможностью самостоятельно помочиться.
Диагностика синехий половых губ
В целом синехии половых губ видны невооружённым глазом. Дополнительные методы исследования необходимы для выявления осложнений и причины, а также дифференциальной диагностики с пороками развития.
Дифференциальная диагностика
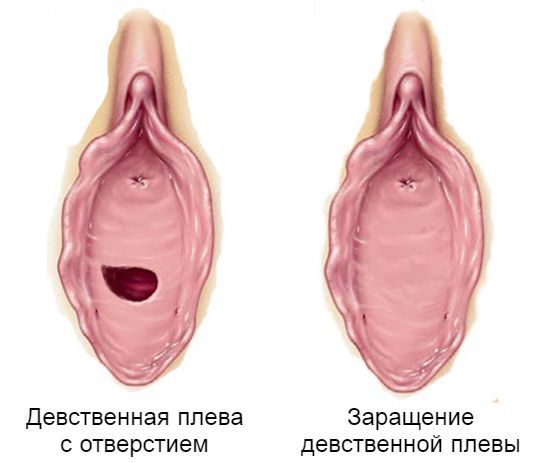
Дифференциальный диагноз должен проводиться с пороками развития мочеполовой системы, такими как атрезия девственной плевы, урогенитальный синус и женский псевдогермафродитизм. Чтобы понять, как возникают данные патологии, вспомним механизм формирования влагалища и мочеполового тракта в эмбриональный период развития.
Для диагностики осложнений синехий половых губ может быть назначен контроль общего анализа мочи, взят мазок и посев на флору с определением чувствительности к антибиотикам и выполнена ПЦР на скрытые инфекции, передаваемые половым путём.
Лечение синехий половых губ
«Золотым стандартом» консервативного лечения является назначение мазей с конъюгированным эстрогеном или эстриолом. Эти препараты являются первой линией терапии. Механизм их действия заключается в увеличении количества железистых клеток и клеток эпителия, усилении восстановления под воздействием экзогенного эстрогена.
Мазь назначается курсом, применяется местно 1 раз в сутки. Побочные эффекты могут проявиться в виде гиперпигментации вульвы, сыпи, нагрубания молочных желёз и кровянистых выделений из половых путей. Данные побочные эффекты требуют отмены препаратов.
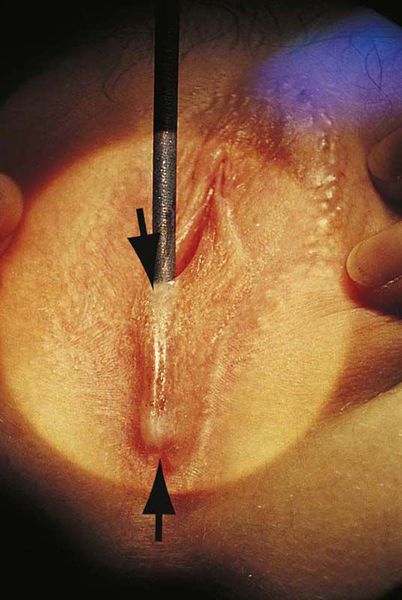
Операция производится в амбулаторных условиях. За 5-10 минут до манипуляции для обезболивания используют аппликационную анестезию с применением мази, содержащей лидокаин. Иногда хирургическому вмешательству предшествует назначение седативных препаратов, чтобы успокоить ребёнка. В ходе операции врач разводит большие половые губы в противоположные стороны и подсекает соединительную мембрану скальпелем или ножницами. В сформировавшееся отверстие вводится желобчатый зонд, по жёлобу которого скальпелем полностью рассекается соединительнотканная мембрана.
При наличии «свежих» тонких синехий зачастую достаточно механического разведения малых половых губ в противоположные стороны без использования режущих инструментов: под воздействием силы натяжения соединительнотканные перемычки разрываются без возникновения болезненных ощущений.
Родители могут самостоятельно устранить «свежие» синехии, не обращаясь к врачу. Для этого рекомендуется половые губы разводить при помощи ватных палочек с использованием эмолентов. Чаще всего такой способ эффективен.
Для снижения риска рецидива на раневую поверхность до заживления рекомендовано наносить мазь с конъюгированным эстрогеном или эстриолом. Как правило, после манипуляции дети не предъявляют жалоб на боль, но иногда могут ощущать дискомфорт во время мочеиспускания в течение первых двух суток.
Прогноз. Профилактика
Прогноз для жизни и здоровья благоприятный, однако возможны рецидивы.
Методом первичной и вторичной профилактики синехий малых половых губ является соблюдение правил интимной гигиены :
Синдром Ашермана – сращение матки
Александр Иванов, хирург-гинеколог
При Синдроме Ашермана внутри маточной полости образуются спайки (синехии), приводящие к нарушениям цикла, невынашиванию, внематочной беременности и бесплодию. Болезнь может зайти столь далеко, что стенки матки срастаются.
Синдром Ашермана отлично диагностируется, причины патологии хорошо изучены, известна и группа риска, однако число женщин с запущенными синехиями не сокращается.
Что такое Синдром Ашермана
Синдром Ашермана – это комплекс репродуктивных проблем, связанный с образованием внутриматочных синехий.
Внутриматочные синехии – основной признак Синдрома Ашермана – представляют собой спайки стенок матки, которые могут частично или полностью перекрывать просвет органа. Такие грубые сращения на слизистой оболочке приводят к деформации органа, изменению его плотности.
Спайки препятствуют нормальному выведению менструальных выделений из матки и снижают вероятность имплантации оплодотворенной яйцеклетки в маточную стенку. В результате женщина, столкнувшаяся с проблемой внутриматочных синехий, страдает нарушениями менструального цикла и различными формами бесплодия.
Почему возникают внутриматочные синехии при Синдроме Ашермана?
Заболевание вызывается травмами и инфекциями матки. В результате ее внутренняя оболочка (эндометрий) грубеет, образуя жесткие выросты, спайки и сращения. Стенки органа «слипаются» друг с другом.
Что чувствует женщина при Синдроме Ашермана – признаки и симптомы при сращении матки
Первое время симптомов нет, но со временем из-за воспаления появляется боль внизу живота. Матка увеличивается в объемах, грубеет, давит на кишечник и мочевой пузырь. Нарушается работа этих органов: женщину мучают запоры, учащенное мочеиспускание, ложные позывы.
Выраженность симптомов зависит от степени патологии:
При внутриматочных синехиях, не пропускающих плодное яйцо, увеличивается риск внематочной трубной или шеечной беременности.
Лечение синдрома Ашермана – хирургическое и медикаментозное
Вначале врач выясняет степень поражения тканей. Простого осмотра на гинекологическом кресле недостаточно, необходима эндоскопия — осмотр полости матки с помощью специального прибора, снабженного подсветкой, оптикой и видеокамерой. Диагностическая эндоскопия показывает строение и тип спаек.
Размеры спаек определяют при трансвагинальном УЗИ, когда датчик помещают внутрь влагалища. Для большей точности исследование проводят несколько раз в течение менструального цикла.
Лечение внутриматочных синехий лучше провести сразу же после их выявления, ведь чем раньше обнаружена проблема — тем больше у врача шансов на быстрое ее решение и восстановление детородной функции пациентки.
Лечат внутриматочные синехии методом гистероскопии под местным или легким внутривенным обезболиванием. Доктор аккуратно рассекает спайки и, чтобы они больше не образовывались, вводит в матку специальный наполнитель (гель) или спираль. Через месяц после вмешательства женщину обследуют повторно, чтобы проверить полноту удаления спаек. Заболевание рецидивирует в 28% случаев, поэтому требуется регулярный врачебный контроль.
После операции пациентка принимает противовоспалительные средства и гормоны, предупреждающие инфекцию и образование соединительной ткани. При выраженных синехиях, спайках и деформациях, сопровождающихся сильным воспалением, матку удаляют.
Профилактика заключается в своевременном лечении «женских» болезней и избегании абортов, особенно проводимых вне клиник, на дому.
Лечение Синдрома Ашермана – вопросы и ответы
Врачи-гинекологи Университетской клиники ответили на распространенные вопросы пациенток относительно лечения внутриматочных спаек, чтобы помочь принять правильное решение и развеять все сомнения о необходимости лечения.
“Подскажите, если я в будущем не планирую иметь детей, нужно ли мне лечить синехии, которые обнаружил врач во время диагностической гистероскопии? Они образовались после аборта, который был три года назад, но все эти годы никак себя не проявляли.”
Внутриматочные спайки могут длительное время не проявляться, но это не значит, что их можно не лечить. Разрастаясь, оболочка, выстилающая матку, заменяется грубой соединительной тканью, которая со временем полностью перекрывает выход для менструальных выделений. В результате развивается состояние, при котором в полости матки скапливается большое количество менструальной крови. Эту патологию называют гематометра и считают опасной для жизни и здоровья пациентки — из-за риска прорыва матки и выхода содержимого в брюшную полость.
Своевременное лечение синехий — залог женского здоровья, особенно если обнаруженные сращения носят множественный характер.
“Можно ли избавиться от синехий без операции, при помощи таблеток или уколов? Я давно хочу ребенка, но боюсь делать операцию, так как подруги говорят, что мне во время процедуры могут повредить матку.”
Лечение Синдрома Ашермана подразумевает разрушение спаек, поэтому без операции не обойтись. Однако страхи и беспокойства по поводу этого вмешательства необоснованны.
Разделение синехий проводится при помощи специального эндоскопического прибора — гистероскопа, благодаря которому врач видит матку изнутри. Прибор, оснащенный оптической и осветительной системами, вводится в полость матки через влагалище. Операцию делают под местным наркозом или в состоянии медикаментозного сна.
Осмотрев матку, гинеколог выбирает наиболее подходящий способ разделить сращения стенок, сохранив при этом функционирование матки. Важно, что каждое движение инструментов врач контролирует визуально — это исключает риск прокола и другого повреждения органа.
“Мне поставили диагноз «Синдром Ашермана» и назначили операцию по удалению внутриматочных синехий. Я так понимаю, что врач разрежет участки сращения стенок скальпелем, или это происходит по-другому?”
Для разделения синехий не всегда используются привычные хирургические инструменты. В тех случаях, когда плотность сращений невелика, а площадь не превышает 25% органа, разделить сросшиеся участки можно, используя корпус самого гистероскопа. Для рассечения плотных и обширных синехий применяют эндоскопические ножницы или щипцы.
В некоторых клиниках применяется также безопасная методика лазерного разделения сращений матки. Лазерный луч испаряет патологические участки тканей, не затрагивая при этом здоровую часть слизистой оболочки. Эта методика еще и бескровна, ведь вместе с тканями синехий коагулируются (запаиваются) и сосуды, что препятствует развитию опасных кровотечений.
“Родственнице делали гистероскопию. После процедуры врач назначил на протяжении 6 месяцев принимать оральные контрацептивы. Скажите, если мне сделают эту же операцию для разделения внутриматочных синехий, мне тоже придется пить противозачаточные?”
После удаления маточных сращений назначается гормональная терапия, но оральные контрацептивы в этом случае не используются. Противозачаточные таблетки вызывают атрофию (отмирание) слизистой оболочки матки (эндометрия), а врач в этом случае преследует противоположные цели. После гистероскопии по поводу синехий назначают гормоны гестагены и эстрогены, которые способствуют восстановлению эндометрия и нормализации менструального цикла.
“У меня ответственная работа, и я не могу себе позволить длительный больничный. Меня интересует, долго ли я пролежу в больнице после гистероскопического удаления внутриматочных сращений?”
Операция по разделению синехий считается малотравматичной, благодаря короткому и простому для пациентки восстановительному периоду. Женщина не госпитализируется, если процедура прошла успешно. При этом пациентка может выполнять любую работу, не связанную с тяжелым физическим трудом.
Получить подробную профессиональную консультацию по лечению Синдрома Ашермана и грамотную медицинскую помощь можно, обратившись в Университетскую клинику. Мы гарантируем современное оборудование, профессионализм и индивидуальный подход к каждому пациенту!
Код по мкб 10 внутриматочные синехии
В настоящее время бездетные браки остаются важной медицинской и социальной проблемой. При этом наиболее актуальной в современном акушерстве является проблема невынашивания беременности. Обусловлено это, прежде всего, тем, что невынашивание беременности является одной из главных составляющих репродуктивных потерь [2,22].
Маточный фактор в структуре нарушений репродуктивной функции женщин составляет 24-62%. [3,17,25]. В Российской Федерации стране в структуре внутриматочной патологии преобладает хронический эндометрит, более чем в 2 раза превышая распространенность других заболеваний. Доля женщин с внутриматочными синехиями варьирует от 3 до 13% [3,36]. В работах В. М. Сидельниковой и Г. Т. Сухих была показана частота встречаемости хронического эндометрита у женщин с невынашиванием беременности до 70% [17]. По данным В.П. Сметник и Л.Г. Тумилович, более 60% женщин с невынашиванием беременности имеют гистологически подтвержденный хронический эндометрит [19].
По данным Рудаковой Е.Б. и соавт. в 54% случаев женское бесплодие сопровождается патологическими изменениями в матке, при этом нарушения функции эндометрия диагностируются у 41% женщин [5]. Поэтому важным при обследовании пациенток с бесплодием и/или привычным невынашиванием беременности является оценка полости матки и эндометрия [1,3,35].
Впервые внутриматочные спайки, или синехии, возникшие после выскабливания полости матки, были описаны Fritsch в 1854 г., но их клиническую значимость доказал Asherman в 1948 г. на примере пациентки с вторичной аменореей после травматичных родов [26]. С этого времени общепринятым термином, обозначающим внутриматочные синехии, стал синдром Ашермана.
В 90% случаев развитие выраженных внутриматочных синехий обусловлено осложненным течением гестации в связи с неполным абортом, замершей беременностью, пузырным заносом, послеродовым кровотечением, остатками плацентарной ткани. Синдром Ашермана чаще всего встречается после неполного аборта (50%), послеродового кровотечения (24%) и артифициального аборта (17,5%) [50]. При необходимости проведения повторного кюретажа полости матки, вероятность развития синехий увеличивается на 8%, и достигает 30% при проведении манипуляции в третий раз. При замершей беременности вероятность возникновения внутриматочных синехий зависит от периода времени, прошедшего между гибелью эмбриона и эвакуацией полости матки, достигая при этом 30,9% [47]. Наложение компрессионных швов при послеродовом кровотечении в последующем также способствует формированию внутриматочных синехий [24].
Наличие синехий способствует увеличению частоты внематочной беременности, привычного невынашивания, преждевременных родов и аномальной локализации плаценты [48].
Есть несколько теорий образования внутриматочных синехии: травматическая, инфекционная, нейровисцеральная [26].
Повреждение базального слоя эндометрия приводит к частичной или полной облитерации полости матки с поверхностью дефектного эндометрия и формированием волокнистых синехий между стенками матки [43]. Пациенты с синдромом Ашерман обычно имеют нарушения менструального цикла, такие как аменорея или гипоменорея, бесплодие или невынашивание беременности [3,17,33,40].
Хроническая активация клеточных и гуморальных провоспалительных реакций сопровождается повышенной выработкой цитокинов и других биологически активных веществ, обусловливающих нарушения микроциркуляции, экссудацию и отложение фибрина в строме эндометрия, что формирует соединительнотканные фибринозные спайки в строме и/или внутриматочные синехии различной степени выраженности [46,50].
Существует несколько классификаций внутриматочных синехий: О. Sugimoto (1978), С. March, R. Izrael (1981). С1995 г. в Европе используется классификация, принятая Европейской ассоциацией гинекологов-эндоскопистов (ESH, 1989), с выделением 5 степеней внутриматочных синехий на основании данных гистерографии и гистероскопии в зависимости от состояния и протяженности синехий, окклюзии устьев маточных труб и степени повреждения эндометрия:
Наиболее удобна и часто используемая классификация внутриматочных синехий по распространенности и степени облитерации полости матки (С. March, R. Izrael; 1981):
По гистологическому строению О. Sugimoto (1978) выделяет 3 типа внутриматочных синехий:
В США в 1988 г. принята классификация Американской ассоциации по бесплодию (ААБ). Эта классификация несколько громоздка, так как ведётся подсчёт баллов по трём разделам: степени вовлечения полости матки, типу синехий и нарушению менструальной функции (в зависимости от выраженности этих показателей). Затем подсчитывают баллы. Различают три стадии: слабую (I), среднюю (II) и тяжёлую (III).
По мнению отечественных исследователей [11,13], основными звеньями патофизиологического механизма преобразования фибринозных сращений в фиброзные спайки являются:
Наиважнейшими клетками, участвующими в данном процессе, являются: полиморфноядерные лейкоциты и макрофаги, мезотелиальные клетки и фибрин. После механического повреждения макрофаги проявляют повышенную фагоцитарную, «дыхательную» и секреторную активность и через 5 дней становятся основными клеточными компонентами популяции лейкоцитов. Макрофаги также способствуют миграции новых мезотелиальных клеток к поврежденной поверхности. Именно эти новые клетки формируют сначала небольшие «островки» на поврежденной поверхности, а затем и тонкие пласты из мезотелиальных клеток. Через 5-7 дней после повреждения реэпителизация заканчивается [15,29].
Длительная стимуляция иммунокомпетентных клеток эндометрия инфекционным возбудителем приводит к декомпенсации регуляторных механизмов локального гомеостаза, что поддерживает персистенцию инфекционного процесса. Хроническая активация клеточных и гуморальных провоспалительных реакций сопровождается повышенной выработкой цитокинов и других биологически активных веществ, обусловливающих нарушения микроциркуляции, экссудацию и отложение фибрина в строме эндометрия. Продолжающаяся депрессия локальной фибринолитической активности под влиянием провоспалительных факторов усиливает ангиогенез в первичных фибринозных сращениях, что усугубляет морфологические изменения в тканях матки, формирует соединительно-тканные фибринозные спайки в строме и/или внутриматочные синехии разной степени выраженности [12,13,22,25].
В настоящее время доказано и подтверждено в экспериментах на животных изменение состояния ангиогенеза, точнее его повышение, или проангиогенный сдвиг, при формировании спаек. Изучено несколько механизмов, объясняющих влияние сосудисто-эндотелиального фактора роста на активацию ангиогенеза путем взаимодействия с его рецептором посредством гипоксией-индуцированного фактора роста [15,27,29]. Большое значение в активации ангиогенеза также играет плацентарный фактор роста, воздействующий на эти процессы посредством ряда механизмов.
Комплексность механизмов формирования спаек, недостаточное понимание патогенеза их образования приводит к тому, что до настоящего времени не существует полноценных способов их профилактики [30].
Для диагностики внутриматочных синехий применяют гистеросальпингографию, ультразвуковую диагностику, гистероскопию.
Рентгенологическая картина при внутриматочных синехиях зависит от характера последних и их распространенности. Обычно синехии проявляются в виде одиночных или множественных дефектов наполнения неправильной формы и различных размеров. Плотные множественные синехии могут разделять полость матки на большое количество камер различного размера, соединенных между собой мелкими протоками. Такую конфигурацию матки не удается определить при гистероскопии; она может дать информацию только о первых нескольких сантиметрах нижнего сегмента полости матки. При гистерографии текучее контрастное вещество может находить пути через сложные лабиринты и необлитерированные пространства. При гистеросальпингографии часто получают ложноположительные результаты из-за обрывков эндометрия, слизи, искривлений полости матки [3,21,28,33,37].
Возможности эхографии в диагностике внутриматочных синехий ограничены. В некоторых случаях визуализируются неровные контуры эндометрия, прерывистое М-эхо, при гематометре определяется анэхогенное содержимое в полости матки [3,33,37].
Магнитно-резонансная томография при необходимости может быть использована для диагностики внутриматочных синехий. Однако высокая стоимость обследования и сложность интерпретации полученных результатов не всегда дают клиницисту возможность применить этот метод в качестве скринингового [44].
Офисная гистероскопия является высокоэффективным доступным в амбулаторных условиях методом диагностики внутриматочной патологии у женщин репродуктивного возраста, не требующим обезболивания [4,7].
Основным методом лечения является операция адгезиолизиса [44]. В настоящее время доступно несколько технологий: 1) тупое разделение нежных спаек тубусом гистероскопа во время гистероскопии, 2) механическое разделение спаек ножницами, введенными в полость матки через операционный канал гистерокопа, 3) воздействие иттрий-алюминивым гранатовым лазером, введенным в полость матки через операционный канал гистерокопа, 4) монополярная или биполярная энергия, 5) гидролаваж, 6) внутриматочный катетер, 7) флюороскопическая техника. Особый интерес представляет использование офисной гистероскопии для диагностики и лечения данной патологии. Общий уровень осложнений достигает 7% и, в основном, представлен перфорациями [39,44].
Результаты лечения индивидуальны и зависят от степени тяжести внутриматочных синехий, этиологии и длительности заболевания, используемых технологий для лечения. Очень важно, чтобы во время адгезиолизиса была восстановлена полость матки в своих нормальных размерах и сохранены островки эндометрия, за счет которых происходит регенерация внутренней поверхности полости матки [4,5].
Использование хирургической микрогистероскопии с микроинструментами и биполярной энергией в соответствии с концепцией «See and treat» [4,39,44] с использованием дополнительного УЗИ-контроля позволяет выполнять диагностику и бережное лечение внутриматочных синехий и синдрома Ашермана.
Эффективность хирургического лечения внутриматочных синехий составляет 85-90%, при этом репродуктивная функция восстанавливается всего у 23-35% женщин. Недавнее исследование показало, что степень выраженности внутриматочных синехий до гистероскопического адгезиолизиса в последующем влияет на вероятность наступления беременности и составляет у пациенток с легкой, средней и тяжелой степенями 64,7%, 53,6% и 32,5% соответственно [34].
Центральной проблемой современной репродуктивной медицины является предотвращение возникновения внутриматочных синехий у пациенток с перенесенными репродуктивными потерями [28].
В послеоперационном периоде для профилактики рецидива образования спаек используются адьювантная терапия эстрогенами в комбинации или без прогестинов, внутриматочные средства, внутриматочные катетеры, противоспаечные барьеры [3,13,31].
Необходимо помнить о возможности возникновения внутриматочных синехий у пациенток с осложненным течением раннего послеродового и послеабортного периода. У больных с подозрением на остатки плодного яйца или плаценты в матке целесообразно выполнять не просто выскабливание слизистой оболочки матки, а осуществлять гистероскопию для уточнения расположения патологического очага и его прицельного удаления без травмирования неизменного эндометрия [5,45].
По данным ряда авторов, краткосрочное размещение в полости матки инородных предметов (шары, катетеры, внутриматочные спирали) препятствует формированию внутриматочных синехий [42]. Так, в результате использования катетера Фолея в послеоперационном периоде у пациенток после миомэктомии при контрольном обследовании через 6 месяцев в 100% случаев синехии отсутствовали, в то время как в группе сравнения данный показатель составил 70% [23]. Катетер Фолея не только безопасен, но и эффективен в восстановлении репродуктивной функции, однако диапазон его использования ограничен в связи с необходимостью госпитализации.
С целью профилактики развития синехий предложено использовать препарат «Суперлимф» в виде внутриматочных орошений после операции и ректальных суппозиториев в течение 10 дневного курса. «Суперлимф» это лекарственная форма интерферона и комплекса природных цитокинов, включающих факторы роста, про- и противовоспалительные цитокины. Важная особенность «Суперлимфа» в том, что он регулирует синтез коллагена и пролиферативную активность фибробластов, стимулирует регенерацию, предупреждает образование грубых рубцов [6].
Для предупреждения возникновения синехий в послеоперационном периоде предложено проведение динамической офисной гистероскопии с использованием инстилляции в полость матки лечебного раствора лидазы 64 ЕД и гидрокортизона 125 мг в 20 мл изотонического раствора [8].
Исследование Назаренко Т.А. и соавт. показало, что эффективно включение ферментного препарата Лонгидаза® в комплекс послеоперационных лечебных мероприятий после разрушения внутриматочных синехий, препарат способствует восстановлению морфофункционального состояния эндометрия [12].
Создание внутриматочной системы с двумя изолированными лекарственными рилизинг-системами, содержащими эстроген, а также цитокины призвано способствовать сохранению не только нормальной анатомии полости матки, но и восстановлению функциональной активности эндометрия за счет оптимизации регенеративных процессов в послеоперационном периоде [41].
В настоящее время перспективным направлением репродуктивной медицины является коррекция внутриматочной патологии с использованием стволовых клеток, которые, как было показано, обладают способностью идентифицироваться в клетки эндометрия в естественных условиях [32].
В результате анализа сравнительной эффективности карбоксиметилцеллюлозы и гиалуроновой кислоты в профилактике возникновения внутриматочных синехий после гистероскопической коррекции была доказана более выраженная эффективность препарата карбоксиметилцеллюлозы [24].
Особое значение в профилактике возникновения синехий принадлежит и способу эвакуации полости матки.
В настоящее время актуальна тенденция к уменьшению инвазивности оперативной гистероскопии. Степень инвазии операции в основном определяется повреждением цервикального канала при введении гистероскопа в полость матки, а также воздействием различных видов энергий на эндометрий и миометрий. До недавнего времени практически любая внутриматочная патология могла быть устранена только путем использования метода оперативной гистероскопии с наружным диаметром гистероскопа более 7 мм или гистерорезектоскопии [3,7,34]. Данные операции считаются малоинвазивными, но требуют общей анестезии, сопровождаются травматизацией шейки матки при расширении её канала, риском серьезных осложнений. Устранение внутриматочной патологии при гистерорезектоскопии основывается на использовании электрической энергии, что обуславливает наличие термического повреждения эндометрия и миометрия.
Так, было показано, что удаление остатков трофобластической ткани под контролем гистероскопа при помощи гистерорезектоскопической петли без использования тока вызывает меньшую травматизацию и, в последующем, в меньшей степени способствует образованию внутриматочных синехий, чем проведение более распространенной в данном случае процедуры дилатации и эвакуации плодного яйца [38]. Неудачное опорожнение матки вне гистероскопической визуализации и полноценной реабилитации травмированного эндометрия формирует сущность хронического эндометрита ятрогенного происхождения [13].
В результате многочисленных исследований выявлено, что включение физических методов в алгоритмы восстановления после гинекологических операций и лечения хронического эндометрита, повышает частоту наступления и вынашивания беременности, оказывает позитивное влияние на состояние рецепторного аппарата эндометрия и маточную гемодинамику [10,16,20].
Индуцированное применением физических методов ремоделирование молекулярных характеристик эндометрия, приводит к восстановлению его рецептивности: регрессу воспаления и фиброза, регуляции процессов ангиогенеза, регенерации и рецепции половых стероидов [18].
Актуальной проблемой в современных условиях является необходимость сохранения и восстановления репродуктивного здоровья пациенток после потери беременности, поскольку частота таковых предопределяет рост уровня хронического эндометрита и развитие внутриматочной патологии.
В настоящее время ни один из существующих методов профилактики формирования внутриматочных синехий не является достаточно эффективным, что требует проведения дальнейших исследований для повышения эффективности мероприятий с учетом данных о роли патофизиологической регуляции формирования синехий, в том числе и ангиогенеза.
Рецензенты:
Рогожина Ирина Евгеньевна, доктор медицинских наук, доцент, заведующий кафедрой Акушерства и гинекологии ФПКиППС ГБОУ ВПО «Саратовский ГМУ им. В.И.Разумовского» Минздравсоцразвития РФ, г.Саратов.
Буров Юрий Александрович, доктор медицинских наук, заведующий отделением сосудистой хирургии МУЗ «1-я Городская клиническая больница им. Ю.Я. Гордеева», г.Саратов.