Электронная и электронно-графическая формула
Что такое электронная и электронно-графическая формула
Наиболее часто электронные формулы записывают для атомов в основном или возбужденном состоянии и для ионов.
Существует несколько правил, которые необходимо учитывать при составлении электронной формулы атома химического элемента. Это принцип Паули, правила Клечковского или правило Хунда.
Составление электронной и электронно-графической формулы
При составление электронной формулы следует учитывать, что номер периода химического элемента определяет число энергетических уровней (оболочек) в атоме, а его порядковый номер количество электронов.
Согласно правилу Клечковского, заполнение энергетических уровней происходит в порядке возрастания суммы главного и орбитального квантовых чисел (n + l), а при равных значениях этой суммы – в порядке возрастания n:
При заполнение электронами энергетических подуровней также необходимо соблюдать правило Хунда: в данном подуровне электроны стремятся занять энергетические состояния таким образом, чтобы суммарный спин был максимальным, что наиболее наглядно отражается при составлении электронно-графических формул.
Электронно-графические формулы обычно изображают для валентных электронов. В такой формуле все электроны помечаются стрелочками, а ячейками (квадратиками) – орбитали. В одной ячейке не может находиться более двух электронов. Рассмотрим на примере ванадия. Сначала записываем электронную формулу и определяем валентные электроны:
Внешний энергетический уровень атома вольфрама содержит 6 электронов, которые являются валентными. Энергетическая диаграмма основного состояния принимает следующий вид:
Примеры решения задач
| Задание | Изобразите электронную и электронно-графическую формулу химического элемента алюминия. |
| Ответ | Алюминий имеет порядковый номер 13 и расположен в третьем периоде Периодической системы Д.И. Менделеева, следовательно, атом этого химического элемента состоит из положительно заряженного ядра, внутри которого находится 13 протонов, а вокруг ядра имеется три оболочки, по которым движутся 13 электронов. |
Электронная формула алюминия выглядит следующим образом:
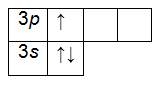
На внешнем энергетическом уровне алюминия находится три электрона, все электроны 3-го подуровня. Электронно-графическая формула имеет следующий вид:
| Задание | Изобразите электронную и электронно-графическую формулу химического элемента хлора. |
| Ответ | Хлор имеет порядковый номер 18 и расположен в третьем периоде Периодической системы Д.И. Менделеева, следовательно, атом этого химического элемента состоит из положительно заряженного ядра, внутри которого находится 17 протонов, а вокруг ядра имеется три оболочки, по которым движутся 17 электронов. |
Электронная формула хлора выглядит следующим образом:
На внешнем энергетическом уровне атома хлора находится семь электронов, все они считаются валентными. Электронно-графическая формула имеет следующий вид:
Электронная формула элемента.
Алгоритм составления электронной формулы элемента:
2. По номеру периода, в котором расположен элемент, определите число энергетических уровней; число электронов на последнем электронном уровне соответствует номеру группы.
3. Уровни разбить на подуровни и орбитали и заполнить их электронами в соответствии с правилами заполнения орбиталей:
1. Составим электронную формулу азота. В периодической таблице азот находится под №7.
Энергетическая диаграмма азота.
2. Составим электронную формулу аргона. В периодической таблице аргон находится под №18.
1s 2 2s 2 2p 6 3s 2 3p 6 .
Энергетическая диаграмма аргона.
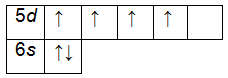
3. Составим электронную формулу хрома. В периодической таблице хром находится под №24.
Энергетическая диаграмма цинка.
4. Составим электронную формулу цинка. В периодической таблице цинк находится под №30.
1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10
Обратим внимание, что часть электронной формулы, а именно 1s 2 2s 2 2p 6 3s 2 3p 6 – это электронная формула аргона.
Электронную формулу цинка можно представить в виде:
Электронное строение атома, электронные формулы атомов и электронно-графические формулы.
Строение атома описывается с помощью схемы электронного строения атома, электронной формулы атома, электронно-графической формулы атома.
Схемы электронного строения атомов показывают распределение электронов по энергетическим уровням.
11Na +ll) ) )
Распределение электронов в атомах по энергетическим подуровням показывают электронные формулы (конфигурации).
11Na ls 2 2s 2 2p 6 3s 1
Например, структура электронной оболочки для атома алюминия будет иметь следующий вид:
| 2s 2 | 2p 6 | 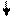 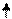 |  _ _ | ||
| 1s 2 | 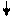  |  | 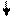 | 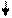  | 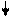  |
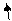  |
По энергетическим соображениям 1s-орбиталь заполняется раньше, чем орбиталь 2s, которая в свою очередь заполняется раньше, чем 2р-орбиталь. Порядок заполнения трех 2р-орбиталей определяется правилом Гунда, согласно которому ни одна из р-орбиталей данной оболочки не может быть занята двумя электронами до тех пор, пока все р-орбитали этой оболочки не будут содержать по одному электрону.
Например, для атома фосфора, электронная формула которого
  | p | |||
 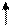 | 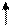   | 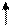  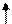 |    | d |
  |
Основное состояние атома фосфора.
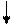  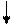 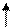 | 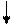  | 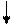  p p | 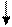 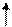 | |
| d | ||||
 |  | 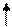 | 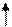 |  |
состояние атома фосфора
| Символ элемента, порядковый номер, название | Схема электронного  строения строения | Электронная формула | Электронно-графическая формула | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Элементы II периода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3Li Литий |  )) 2 1 )) 2 1 | ls 2 2s l |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4Be Берилий |  К L )) 2 2 К L )) 2 2 | ls 2 2s 2 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5B Бор | К L )) 2 3 | 1s 2 2s 2 2p 1 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6C Углерод |  К L )) 2 4 К L )) 2 4 | 1s 2 2s 2 2p2 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7N Азот |  К L К L  )) 2 5 )) 2 5 | 1s 2 2s 2 2p 3 |
Строение элементов II, III и IV периодов
13Аl Алюминий | KLM |  ))) 2 8 3 ))) 2 8 31s 2 2s 2 2p 6 3s 2 3p 1 | |
18 Аr Аргон | |  KLM ))) 2 8 8 KLM ))) 2 8 81s 2 2s 2 2p 6 3s 2 3p 6 | |
Элементы IV периода | 13К Калий | |  KLMN )))) 2 8 8 1 KLMN )))) 2 8 8 11s 2 2s 2 2p 6 3s 2 3p 6 4s 1 | |
20Са Кальций | KLMN | 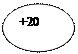 )))) 2 8 8 2 )))) 2 8 8 21s 2 2s 2 2p 6 3s 2 3p 6 4s 2 | |
2lSc Скандий | KLMN | 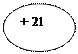 )))) 2 8 9 2 )))) 2 8 9 2ls 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1 или ls 2 2s 2 2p 6 3s 2 3p 6 3d 1 4s 2 | |
24Сr Хром | | 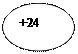 KLMN )))) 2 8 13 1 KLMN )))) 2 8 13 1ls 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 5 | |
|




 KLM ))) 2 8 1
KLM ))) 2 8 1 Цинк
Цинк )))) 2 8 18 3
)))) 2 8 18 3 ls 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 p 1
ls 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 p 1




