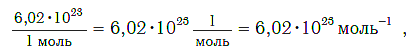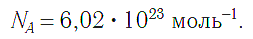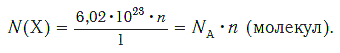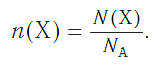Как подсчитать количество атомов в наблюдаемой Вселенной?
В интернете уже не первый год гуляет вопрос о том сколько во Вселенной атомов, и, даже несмотря на возражения снобов, существует ответ! 10^80 — именно столькими по мнению Википедии и остальных интернет-ресурсов атомами заполонена наша Вселенная. Как они пришли к такому ответу?
Вы можете задать свой вопрос мне в телеграме. Мой телеграм-канал об астрофизике и космологии.
Находим примерное количество атомов в наблюдаемой Вселенной
Для грубого подсчета количества атомов прибегнем в ньютоновским законам механики и рассмотрим цепочку того, что из чего во Вселенной состоит. А главное, что нам почти не понадобятся входные данные в виде размеров Вселенной или массы каких-либо тел (за одним исключением). Основное число материи располагается в звездах, таких, например, как наше Солнце.
Рассмотрим систему из планеты (Земля) и звезды (Солнце). Оно описывается законом Всемирного тяготения:
где me — масса Земли и ms — масса Солнца. Так как Земля находится на орбите и обращается вокруг звезды, то она движется с центростремительным ускорением, вычисляемым по формуле:
Вспомним второй закон Ньютона:
где a = ac, соответственно, объединив три вышеописанных уравнения:
Домножив на R 2 обе части, получим:
Зная, что скорость движения по окружности определяется по формуле:
где T — период, получим:
Мы пришли к полезной формуле, благодаря которой можем получить массу Солнца. Зная, что период оборота Земли вокруг Солнца составляет около 1 года (
3,15×10 7 сек), а расстояние от Земли до Солнца
1,5×10 11 м, находим массу Солнца ≈ 1,77×10 30 кг.
Количество атомов в звезде определим как частное массы звезды и массы одного атома водорода, из которого, в основном, и состоят звезды и вся наблюдаемая Вселенная:
Далее определим количество солнцеподобных звезд в галактике тем же путем. Масса галактики будет равна:
3×10 4 световых лет или 2,84×10 20 м и T
2×10 8 лет или 6,3×10 15 сек, соответственно mg
3,41×10 41 кг. Тогда количество звезд в одной галактике типа Млечный Путь равно:
Оценивать количество галактик будем по следующему способу: рассмотрим изображение Hubble Ultra Deep Field, полученное телескопом им. Хаббла в 2012 году. На нем находится около 10 000 галактик. Угловой размер этого кадра составляет 1/60 градуса:
Сколько HUDF сможет поместиться на небесном куполе? Площадь поверхности сферы определяется:
где радиус R можем представить как 1 радиан, равный 57,29 градуса. Тогда площадь поверхности составит 4,13×10 4 квадратных градусов. Подсчитав площадь одного изображения HUDF, равную 1/3600 квадратного градуса, находим количество HUDF на небе:
Если мы умножим полученное количество полей на количество галактик в одном поле, то получим число 14 868 000 000 000 (почти 15 триллионов) — согласно нашим вычислениям это общее количество галактик в наблюдаемой Вселенной.
Складываем!
Мы получили количество галактик, количество звезд в каждой из них и количество атомов в каждой звезде.
Мы ушли недалеко от новостных сайтов и ресурсов с интересными фактами, но зато смогли самостоятельно понять, как кому-то удалось прийти к такому числу. Попутно мы вспомнили законы механики и коснулись законов Кеплера. Ответ на такой, казалось бы, сложный вопрос мы получили простейшими вычислениями. Но неважно, точен ли ответ или нет — для современной науки он бесполезен. Ведь астрономы уже давно не считают звезды =)
Больше информации Вы можете найти в телеграм-канале об астрофизике, космологии и астрофотографии. Пишите мне в личку, наш чат или в блоке комментариев под статьей. Спасибо за внимание.
Как определить количество атомов в молекуле?
Чтобы узнать число атомов в молекуле, достаточно знать молекулярную формулу вещества. После чего мы суммируем число всех атомов в молекуле. Число атомов конкретного химического элемента в веществе мы узнаем по нижнему индексу.
Среди простых веществ, в природе молекулы встречаются не так часто. Среди них: водород H2, азот N2, кислород O2, озон O3, йод I2. За исключением озона все эти молекулы содержат по 2 атома.
Примеры
Определить количество атомов в молекуле воды H2O.
Молекула воды содержит 2 атома водорода и 1 атом кислорода. Значит всего в молекуле содержится 3 атома.
Определить количество атомов в молекуле этана C2H6.
Молекула содержит 2 атома углерода и 6 атомов водорода. Всего в молекуле содержится 2 + 6 = 8 атомов.
Определить количество атомов в молекуле оксида азота (V) N2O5.
Молекула содержит 2 атома азота и 5 атомов кислорода. Всего в молекуле содержится 2 + 5 = 7 атомов.
Определить количество атомов в молекуле пищевой соды NaHCO3.
Молекула содержит 1 атом натрия, 1 атом водорода и 3 атома кислорода. Всего в молекуле содержится 1 + 1 + 3 = 5 атомов.
Определить число атомов в молекуле глюкозы C6H12O6.
Молекула содержит 6 атомов углерода, 12 атомов водорода и 6 атомов кислорода. Всего в молекуле содержится 6 + 12 + 6 = 24 атома.
Определить число атомов в молекуле аспаргина (одна из аминокислот) C4H8O3N2.
Как видим, молекула аспаргина содержит 4 атома углерода, 8 атомов водорода, 3 атома кислорода и 2 атома азота. Всего молекула содержит 4 + 8 + 3 + 2 = 17 атомов.
Как видим, рассчитать общее число атомов в молекуле не такая уж и сложная задача.
Как посчитать кол во атомов
Атомы чрезвычайно малы относительно масштаба человеческой жизни. Ученые используют единицу, называемую моль, для описания большого количества атомов и других мелких вещей. Один моль равен 6,022 х 10 ^ 23 частиц. Это значение называется числом Авогадро. Эти частицы могут быть отдельными атомами, молекулами соединения или любой другой наблюдаемой частицей. Чтобы рассчитать количество атомов в одном граммовом образце любого вещества, вы должны рассчитать число молей этого вещества на основе его молярной массы. Затем вы можете использовать число Авогадро для расчета количества частиц.
Реальное приложение
Реальное применение числа Авоградо относится к культовому примеру исследования плотности того, что весит больше: тонны пера или тонны чего-то очень тяжелого, например, кирпича или металлических гирь. Более легкие перья требуют большего количества, чтобы создать ту же плотность, что и более тяжелые предметы.
Найти атомную массу
Прежде чем определять атомную массу, вам нужно посмотреть элементы в периодической таблице и отметить их атомные массовые числа под химическим символом элемента. Чистые элементы имеют атомную массу, которая также является молярной массой или количеством граммов на моль.
Добавить атомную массу
Разделите число родинок
Разделите один грамм на молярную массу соединения. Это дает количество молей соединения в одном грамме образца. Например, один грамм диоксида кремния, разделенный на 60 грамм на моль, дает около 0,0167 моля диоксида кремния.
Умножьте на число Авогадро
Затем умножьте число родинок на число Авогадро. Эта формула дает количество молекул в одном грамме. Например, 0,0167 моль диоксида кремния, умноженное на 6,022 × 10 23, соответствует примерно 1 × 10 22 молекулам диоксида кремния.
Умножить на номер атома
Наконец, умножьте на количество атомов в одной молекуле. Например, каждая молекула диоксида кремния содержит три атома. Следовательно, в одном грамме диоксида кремния содержится около 3 х 10 ^ 22 атомов.
Мольные доли вещества и количество атомов
Мольная доля химического элемента в веществе помогает узнать, сколько моль содержится в том или ином веществе.
Просьба не путать это с массовой долей химического вещества. Это совершенно разные сущности.
Покажем, как вычисляется мольная доля на примере аммоний азотнокислого.
В одном 1 моль вещества содержится
Соответственно мольные доли равны
В 1 моль любого химического вещества содержится постоянное количество атомов/молекул равное
Количество атомов кислорода
Количество атомов азота
Количество атомов водорода
У некоторых читателей может возникнуть недопонимание, как так в 1 моль вещества находится 2 моль азота + 4 моль водорода+3 моль кислорода.
Да и с количеством атомов, тоже получается путаница.
Объясняем на примере воды.
В одном моль воды находится молекул(!) воды(!). В одной молекуле воды содержится 2 атома водорода и один атом кислорода.Следовательно один моль воды состоит из 2 моль водорода и одного моль кислорода, которые в свою очередь содержат соответственно атомов(!!) водорода и атомов кислорода.
Калькулятор который представлен на сайте, может решать следующие задачи
— Расчет мольных долей химических элементов, входящих в формулу
— Расчет количества каждого из химического элемента
— Число атомов химического элемента в 1 моль заданного вещества
— При вводе массы вещества, расчет количества этого вещества (в моль)
Рассмотрим несколько примеров.
1. Чему равна мольная доля кислорода в нитрат калия?
Пишем формулу. Получаем результат
| Заданная формула | |||||
| Количество вещества в указанной массе | |||||
| Количество атомов в веществе(поэлементно) | ||||
| Заданная формула | ||
| Количество вещества в указанной массе | ||
| Заданная формула |
| Количество вещества в указанной массе |
| Количество вещества в указанной массе |