Аневризма вены Галена
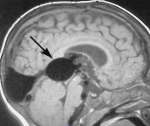
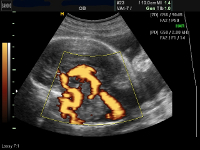
Аневризма вены Галена – это группа аномалий развития большой мозговой вены, образующихся в результате персистенции эмбриональных сосудов с формированием артериовенозного шунтирования. Проявляются сердечной недостаточностью, гидроцефалией, отставанием в физическом и умственном развитии. Характерна неврологическая симптоматика, возможен разрыв аневризмы с внутричерепным кровоизлиянием. Диагностика аневризмы вены Галена проводится во время пренатального УЗИ-скрининга с допплерографией. У новорожденных диагноз подтверждается при помощи КТ, МРТ, ангиографии. Лечение оперативное, осуществляется эмболизация сосудов, питающих вену.
МКБ-10
Общие сведения
Аневризма вены Галена объединяет в себе множество сосудистых аномалий, связанных с нарушением эмбрионального развития большой мозговой вены. Патология встречается крайне редко, частота всех артериовенозных мальформаций головного мозга не превышает 1% среди населения всех возрастов. Патология в два раза чаще встречается у мальчиков. Актуальность проблемы в современной педиатрии связана с высоким уровнем смертности, который лишь незначительно снизился в последние годы (до 50-70%), несмотря на огромный прогресс сосудистой нейрохирургии. Кроме того, из-за редкой встречаемости аневризмы вены Галена большинство специалистов оказываются неподготовленными к подобным случаям. По этой причине все операции проводятся в крупных федеральных центрах.
Причины
Питание тканей головного мозга изначально осуществляется посредством эмбриональных сосудов, стенки которых по своей структуре отличаются от нормальной сосудистой стенки. В течение 4-8 недель внутриутробной жизни эти сосуды заменяются полноценными артериями и венами. Под воздействием различных повреждающих факторов данный процесс нарушается, эмбриональные сосуды персистируют. Таким образом, образование всех артериовенозных мальформаций, в том числе аневризмы вены Галена, происходит в первом триместре беременности. Высокой тропностью к нервной и сосудистой ткани обладают многие бактерии и вирусы. Патологии развития мозговых сосудов также могут сформироваться под влиянием лекарственных препаратов, радиации и других факторов.
Патогенез
Аневризма вены Галена может быть представлена собственно патологическим расширением сосуда, но чаще всего речь идет о наличии множественных артериовенозных шунтов эмбрионального строения. Шунтирование приводит к сбросу артериальной крови и, соответственно, анемизации тканей головного мозга. Кроме того, повышается нагрузка на венозное русло. Как уже было сказано, строение эмбриональных сосудов отличается от обычных. В частности, они не имеют привычного мышечного слоя, именно с этим связан высокий риск разрыва шунтов. Переполненность венозного русла приводит к растяжению, вследствие чего возможно механическое сдавление сильвиева водопровода с формированием гидроцефалии.
Классификация
Артериовенозная мальформация располагается в передней черепной ямке, сверху и сзади от зрительных бугров, в так называемой цистерне вены Галена. Структурно выделяют три типа аневризмы вены Галена.
Симптомы
Патология проявляется с рождения у 50% пациентов. Ведущим симптомом является сердечная недостаточность, развивающаяся в результате высокого венозного возврата крови от головного мозга и, соответственно, возрастающей нагрузки на левые отделы сердца. Поскольку аневризма вены Галена формируется еще внутриутробно, уже к рождению сердечная недостаточность отличается высоким риском декомпенсации. Клинически это выражается в усталости при кормлении, генерализованных отеках, одышке вследствие интерстициального отека легких. В дальнейшем сердечная недостаточность становится одной из причин отставания в физическом развитии.
Гидроцефалия является неблагоприятным прогностическим признаком, поскольку свидетельствует об окклюзии сильвиева водопровода или значительном объеме сброса крови в венозное русло. Голова ребенка увеличена с рождения, на ее поверхности заметны расширенные вены. Может отмечаться рвота, экзофтальм, очаговая неврологическая симптоматика в виде птоза, косоглазия. Повышение внутричерепного давления иногда сопровождается судорогами. В дальнейшем характерно отставание в умственном развитии, связанное также с недостаточным питанием тканей мозга. Реже аневризма вены Галена проявляется симптомами внутричерепного кровоизлияния: потерей сознания, судорогами и т. д.
Диагностика
Первичная диагностика становится возможной при плановом УЗИ-скрининге в III триместре беременности. Аневризма вены Галена визуализируется как анэхогенное образование в центре головы. Для подтверждения используется цветовое допплеровское картирование. Метод отличается высокой степенью достоверности. В отсутствие дородовой диагностики установить наличие сосудистой аномалии после родов бывает проблематично. Во-первых, заболевание встречается крайне редко, поэтому становится для педиатра исключением среди множества других причин сердечной недостаточности и гидроцефалии. Во-вторых, аневризма вены Галена не всегда клинически проявляется с момента рождения.
Компьютерная томография и МРТ также широко используются в диагностических целях. На снимках можно визуализировать патологические клубки эмбриональных сосудов. Для дальнейшего планирования тактики лечения необходимо проведение ангиографии, которая позволяет установить топографические отношения с нормальными сосудами и обнаружить другие возможные сосудистые аномалии. Заподозрить тромбоз можно по результатам ангиографии, поэтому контрастное рентгенологическое исследование сосудов остается основным в диагностике аневризмы вены Галена. Именно данный метод позволяет сосудистым хирургам планировать тактику оперативного вмешательства.
Лечение аневризмы вены Галена
Основным методом терапии в настоящее время остается эндоваскулярная эмболизация сосудов, питающих аневризму. Рекомендованный возраст ребенка для проведения операции – 2-6 месяцев. На этапе предоперационной подготовки используются антикоагулянты для профилактики тромбоза сосудов, а также кардиотоники с целью компенсации сердечной недостаточности. При наличии признаков выраженной гидроцефалии показано наложение шунта для нормализации внутричерепного давления. Обычно проводится вентрикулоперитонеальное шунтирование. Открытые хирургические операции в лечении аневризмы вены Галена практически не применяются.
Прогноз
Прогноз заболевания чаще неблагоприятный. Развитие современных методов нейрохирургии позволило снизить смертность до 50-70%. Тем не менее, выжившие после операции дети отстают в умственном развитии, сохраняется неврологическая симптоматика. Первичная профилактика проводится пренатально. При обнаружении аневризмы вены Галена на УЗИ врачи и родители определяют тактику дальнейшего ведения беременности. Большинство специалистов рекомендуют оперативное родоразрешение путем кесарева сечения с последующей терапией, описанной выше. В настоящее время смертность в таких случаях достигает 80%.
Сосудистые аномалии различной локализации (артериовенозная мальформация, венозная мальформация, лимфатическая мальформация и их комбинации, сосудистые опухоли)
14-16 октября, Алматы, «Атакент»
150 участников из 10 стран. Новинки рынка стоматологии. Цены от производителей
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «25» июня 2020 года
Протокол №101
Артериовенозная мальформация (АВМ) – это нарушение в строении артерии, приводящее к образованию одного или нескольких прямых соединений между артериями и венами. Обычно артерии доставляют насыщенную кислородом кровь к органам и тканям. При аномальном скоплении артерий на одном участке туда поступает слишком много крови, что создает условия для артеризаций одноименных вен и перегрузке правых отделов сердца.
Венозная и Лимфатическая мальформации (ВМ/ЛМ) – это врожденный порок развития, характеризирующийся наличием патологических венозных/лимфатических коммуникаций с прогрессирующим застоем венозной крови/лимфы в полостях.
Младенческая гемангиома (инфантильная гемангиома) – это доброкачественная сосудистая опухоль, наиболее часто встречающаяся у детей первого года жизни, развивающаяся из эндотелиальной ткани в первые месяцы жизни и способная к спонтанной инволюции в течении последующих лет.
Название протокола: СОСУДИСТЫЕ АНОМАЛИИ РАЗЛИЧНОЙ ЛОКАЛИЗАЦИИ (артериовенозная мальформация, венозная мальформаци, лимфатическая мальформация и их комбинации, сосудистые опухоли)
Код(ы) МКБ-10:
| МКБ-10 | |
| Q27.3 | Периферический артериовенозный порок развития |
| Q27.8 | Другие уточненные врожденные аномалии системы периферических сосудов |
| Q87.2 | Синдромы врожденных аномалий, вовлекающих преимущественно конечности (синдром Клиппеля-Треноне) |
| D18.0 | Гемангиома любой локализации |
| D18.1 | Лимфангиома любой локализации |
Дата разработки протокола/пересмотра протокола: 2019 год.
Сокращения, используемые в протоколе:
АВМ – артерио-венозная мальформация
АВС – артерио-венозный свищ
ВМ – венозная мальформация
ЛМ – лимфатическая мальформация
ИГ – инфантильная гемангиома
КАД – капиллярная ангиодисплазия (мальформация), «винные пятна»
АЧТВ – активированное частичное тромбопластиновое время
КТ – компьютерная томография
КТА – компьютерно-томографическая ангиография
МНО – международное нормализованное отношение
МРА – магнитно-резонансная ангиография
МРТ – магнитно-резонансная томография
МСКТА – мультиспиральная компьютерно-томографическая ангиография
ОАМ – общий анализ мочи
ПВ – протромбиновое время
ПТИ – протромбиновый индекс
УД – уровень доказательности
УЗДГ – ультразвуковая допплерография
УЗИ – ультразвуковое исследование
Пользователи протокола: ангиохирургии, кардиологи, педиатры, врачи общей практики, дерматологи.
Категория пациентов: дети.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или Высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Лечение неразорвавшихся аневризм головного мозга
14-16 октября, Алматы, «Атакент»
150 участников из 10 стран. Новинки рынка стоматологии. Цены от производителей
Общая информация
Краткое описание
Ассоциация нейрохирургов России
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ЛЕЧЕНИЮ НЕРАЗОРВАВШИХСЯ АНЕВРИЗМ ГОЛОВНОГО МОЗГА (Москва, 2015)
Клинические рекомендации утверждены на Пленуме Правления Ассоциации нейрохирургов России 14.10.2015 г. Красноярск
Введение
В последние годы число обращений пациентов с неразорвавшимися аневризмами (НА) в нейрохирургические учреждения неуклонно возрастает. Опубликованные в зарубежной литературе серии по анализу этой патологии содержат до нескольких сотен, а кооперативные исследования – до нескольких тысяч больных.
Учитывая, что неразорвавшиеся аневризмы потенциально могут стать источником внутричерепного кровоизлияния, возникла необходимость определения тактики ведения и лечения этих больных. Единой точки зрения по этому вопросу не существует, хотя в последние годы рекомендации различных клиник все более совпадают по различным позициям и становятся более конкретными. Основной проблемой при выявлении неразорвавшейся аневризмы является оценка вероятного риска ее разрыва. Несмотря на опубликованные незначительные показатели первичных кровоизлияний из ранее неразорвавшихся аневризм [28, 75, 90], существуют группы больных с высоким риском разрыва аневризм. К таким факторам риска относят как морфологические особенности выявленной аневризмы (несколько куполов, неровность тела аневризмы, соотношение размера аневризмы к диаметру несущего сосуда, расположение, большой и гигантский размеры, увеличение размеров аневризмы с течением времени и т.д.), так и семейный анамнез кровоизлияния из аневризмы, наличие ряда вредных привычек, таких как курение, присутствие сопутствующих заболеваний (артериальная гипертензия). Существенное увеличение пациентов с диагностированными неразорвавшимися аневризмами в РФ и накопление значительного опыта хирургического лечения этой патологии явилось обоснованием для создания российского рекомендательного протокола по ведению и лечению больных с НА.
Этиология и патогенез
В настоящее время этиология и патогенез НА рассматриваются в рамках этиологии и патогенеза аневризм в целом. Факторы, лежащие в основе заболевания, принято делить на немодифицируемые и модифицируемые. К первым относят: генетические факторы [12, 26, 100]; ряд наследственных заболеваний [4, 9, 13, 19, 21, 84, 85, 99, 106, 120]; возраст и пол [6, 30, 31, 35, 40, 41, 62, 66, 71, 97, 103, 114, 115]. Во вторую группу входят: артериальная гипертония, курение, алкоголь, лекарства и вещества с симптомиметическим действием, пероральные контрацептивы [31, 32, 36, 45, 52, 53, 114]. Доказательность степени влияния этих факторов на формирование аневризм, в том числе, неразорвавшихся, различна.
Эпидемиология
Факторы и группы риска
Группы повышенного риска выявления НА
Пол и возраст
Частота выявления НА увеличивается с возрастом, достигая максимума в возрастной группе от 50 до 60 лет. Чаще аневризмы выявляются у женщин, в независимости от возрастной категории [6, 30, 31, 35, 40, 41, 62, 66, 71, 97, 103, 114, 115].
Сопутствующие заболевания
Пациенты с перечисленными ниже заболеваниями входят в группу повышенного риска обнаружения неразорвавшихся аневризм [4, 9, 13, 19, 21, 84, 85, 99, 106, 120]:
— аутосомно-доминантный поликистоз почек (частота обнаружения аневризм в 3-14 раз выше по сравнению с основной популяцией)
— синдром Элерса-Данло IV типа
— синдром Марфана
— коарктация аорты
— двустворчатый аортальный клапан
— эластическая псевдоксантома
— наследственная геморрагическая телеангиэктазия
— нейрофиброматоз 1 типа
— недостаточность α1-антитрипсина
— фиброзномышечная дисплазия
— феохромацитома
— сидром Кляйнфельтера
— туберозный склероз
— Синдром Нунан (наследственное сочетание стеноза клапанов лёгочной артерии, гипертелоризма, оттопыренных ушных раковин и др. нарушений)
— недостаточность α-глюкозидазы
— первичная карликовость с микроцефалией и остеодисплазией
— внутричерепные артериовенозные мальформации
«Семейные аневризмы»
По данным различных исследований [9, 55, 56, 76-78, 83, 86, 94] частота встречаемости «семейных аневризм» составляет от 7 до 20% в зависимости от различных методов оценки семейного анамнеза и анализа полученных данных. Чаще выявляют неразорвавшиеся аневризмы среди родственников первого поколения пациента с разрывом аневризмы – около 4% [74, 94], с некоторой большей встречаемостью среди сибсов пациента, чем среди его детей.
К факторам, повышающим вероятность обнаружения аневризмы среди родственников больного, перенесшего САК, относят следующие: старший возраст, женский пол, курение, наличие в анамнезе гипертонической болезни, гиперхолестеринемия, семейный анамнез поликистозной болезни почек, семейный анамнез наличия САК или аневризмы у 2 и более родственников [74]. Частота выявления неразорвавшихся аневризм у родственников первой степени родства при наличии в анамнезе аневризм и/или САК у 2 и более членов их семей составляет от 8,7% [76] до 19,1% (старше 30 лет, наличие таких отягощающих факторов, как курение и гипертоническая болезнь) [9].
Риск разрыва аневризмы
Таблица 1. Риск разрыва НА в зависимости от ее размера и локализации (по данным ISUIA [114]).
| Пятилетний кумулятивный риск разрыва в соответствии с размером и расположением аневризмы | |||||
| 7-12 мм | 13-24 мм | 25 мм | |||
| Группа 1 | Группа 2 | ||||
| Кавернозный отдел ВСА (n=210) | 0 | 0 | 0 | 3.0% | 6.4% |
| ПСА и ПМА/СМА/ВСА | |||||
(n=1037)
средняя мозговая артерия, ВСА – внутренняя сонная артерия, ВББ – вертебробазилярный бассейн, ЗМА – задняя мозговая артерия, ЗСА – задняя соединительная артерия
Группа 1 – пациентов без САК
Группа 2 – пациенты с САК в анамнезе при разрыве другой аневризмы
Предрасполагающие факторы риска разрыва аневризмы
Рост аневризмы
К факторам, ответственным за рост аневризм с течением времени, относят повышенное АД, гемодинамический стресс в зависимости от формы аневризмы и ее расположения, изначальный размер аневризмы, воспаление в стенке аневризмы, женский пол, курение, молодой возраст, избыточное употребление алкоголя. Отмечается повышенный риск роста аневризм у пациентов с наличием инсульта или транзиторной ишемической атакой в анамнезе, и при выявлении множественных аневризм [39, 58, 89].
Проспективное исследование, проведенное в США и включавшее пациентов с аневризмами диаметром менее 7 мм и без наличия САК в анамнезе (всего 319 аневризм) не зафиксировало ни одного разрыва аневризмы за период наблюдения в течение 2,4 лет. Однако за период наблюдения был отмечен рост аневризмы как минимум на 0,75 мм у 5,4% пациентов в течение года [10].
Отмечено, что ежегодный риск разрыва «растущей» аневризмы может превышать данный показатель у аневризмы без роста в 12 раз [58, 71, 104].
Морфологические параметры и локализация
Наибольшая частота кровоизлияний характерна для аневризм в вертебробазилярном бассейне, в области ПСА и перикаллезной артерии [111,121]. Аневризмы в области СМА менее подвержены риску разрыва.
Больший риск разрыва аневризмы отмечают при выявлении следующих морфологических параметров: больший размер, неправильная форма и/или наличие дивертикулов, узкая шейка аневризмы, соотношение максимального размера аневризмы к диаметру несущей артерии более 2,05, соотношение высоты аневризмы к диаметру шейки более 1,6 [47, 80, 111, 121].
Другие факторы
Факторами риска разрыва НА являются молодой возраст, курение, артериальная гипертензия, женский пол, наличие в анамнезе САК из другой аневризмы, семейный анамнез САК [10, 61].
Клиническая картина
Cимптомы, течение
НА наиболее часто определяются в ходе обследования больных после кровоизлияния из другой аневризмы, а также при наличии у больного неврологической симптоматики или возникновения внезапной головной боли или изменения ее характера. В исследовании ISUIA неразорвавшаяся аневризма была выявлена у пациентов в ходе обследования по поводу кровоизлияния из другой аневризмы (30.4%), головной боли (23.7%), ТИА или ОНМК по ишемическому типу (10.5% и 10.6% соответственно), поражения черепных нервов (8.0%), судорожных припадков (2.9%), появления симптомов объемного образования головного мозга (2.7%), субдуральной или внутримозговой гематомы (1.2%), опухоли головного мозга (0.8%), демиелинизирующих заболеваний головного мозга (0.4%) и неопределенных “приступов” (7.1%) [114].
Характер проявления НА влияет на естественное течение заболевания и на выбор тактики лечения. Отмечено, что среди неразорвавшихся симптомных аневризм риск кровоизлияния в 4 раза выше по сравнению с асимптомными, случайно выявленными, аневризмами [111].
Диагностика
Диагностика
Возможности методов нейровизуализации аневризм резко расширились в последнее десятилетие, включая применение дигитальной субтракционной ангиографии в 2D и 3D режимах, МР-ангиографии и КТ-ангиографии.
После выявления неразорвавшейся аневризмы необходимо оценить ее анатомические особенности (и, что возможно будет доступно в широкой практике в будущем, гемодинамические параметры) как при первичном исследовании, так и при обследовании в динамике для определения дальнейшей тактики лечения [22, 63, 122].
Методы обследования
Компьютерная томография в ангиографическом режиме (КТ-ангиография)
Чувствительность, специфичность и точность КТ-ангиографии в диагностике аневризм составляет 96.3%, 100% и 94.6% соответственно. При милиарных аневризмах размером менее 3 мм эти показатели составляют 81.8%, 100% и 93.3% соответственно [108].
При проведенном в 2003 мета-анализе 21 исследования, включавших 1251 пациентов, выявлено, что чувствительность и специфичность КТ-ангиографии составляет 93.3% и 87.8% соответственно в сравнении с цифровой церебральной ангиографией [14]. Выполнение КТ-ангиографии позволяет оценить наличие кальцификатов в стенке аневризмы и тромбов в ее полости [70]. Однако 3D-реконструкция может не совсем точно отражать истинную анатомию и размеры шейки/купола/несущего сосуда, особенно при аневризмах малых размеров (менее 5 мм) [29].
Дигитальная субтракционная ангиография (ДСА)
ДСА остается «золотым стандартом» в диагностике аневризм, особенно с введением в рутинную практику 3D-ротационной ангиографии, для выявления аневризм менее 3 мм и сосудов малого диаметра (в том числе, перфорирующих артерий) [20, 29, 46, 60, 91, 95, 101, 102, 116]. ДСА не может быть использована как скриннинговое исследование в связи с необходимостью госпитализации пациентов и наличием вероятных осложнений при проведении манипуляции, таких как аллергическая реакция на контраст, ОНМК по ишемическому типу, разрыв аневризмы, повреждение артерии, гематома в области пункции артерии и другие [34, 82]. Количество осложнения при проведении ДСА, включая постоянный неврологический дефицит у пациентов с аневризмами, САК и АВМ, не превышает 0.07% [17].
Проведение ДСА нецелесообразно [рекомендация] у пациентов с аутосомно-доминатным поликистозом почек, почечной недостаточностью, синдромом Элерса-Данло.
Анализ изображений [рекомендации]
При выявлении аневризмы, независимо от того, какой метод использовался, необходимо определить ряд параметров для уточнения тактики лечения и проведения динамического наблюдения. Необходимо оценить размеры шейки аневризмы, соотношение диаметра купола к диаметру шейки, угол расположения аневризмы относительно несущего сосуда (для латеральных аневризм), соотношение максимального размера купола к диаметру несущего сосуда, размеры аневризмы в 3 плоскостях [63].
Скриннинг
Определенные группы в популяции, имеющие повышенный риск обнаружения аневризм головного мозга, подлежат проведению скрининга. Пациент перед проведением обследования должен быть информирован о возможных последствиях как проведения самого исследования, так и различных видов лечения или консервативного лечения, включая такие психологические факторы, как стресс и тревогу, если аневризма будет обнаружена. Учитывая данные эпидемиологических исследований, можно рекомендовать проводить неинвазивные методы скрининга каждому человеку в общей популяции после 30 лет в независимости от наличия или отсутствия факторов риска обнаружения аневризмы. Если при первом обследовании данных за аневризму не обнаружено, повторное обследование можно рекомендовать по достижении 50 лет.
Лечение
Хирургическое лечение пациентов с неразорвавшимися аневризмами
Отбор пациентов с неразорвавшимися аневризмами на операцию [рекомендации]
Проведение операции по поводу НА сосудов головного мозга показано при наличии одного и/или нескольких следующих факторов риска разрыва аневризмы:
• размер аневризмы 7 и более мм
• несферическая форма и наличие дивертикулов
• латеральное расположение аневризмы
• коэффициент соотношения высоты купола аневризмы к диаметру шейки аневризмы более 1,6
• коэффициент соотношения максимального размера аневризмы к диаметру несущего сосуда более 2,05
• угол отклонения латеральной аневризмы от несущей артерии более 1120
• рост размера аневризмы на 0,75 мм и более в течение 6 месяцев
• появление новых клинических проявлений (симптомы поражения черепных нервов, появление и/или изменение характера головных болей, ишемические нарушения в бассейне несущей аневризму артерии)
• незамкнутость артериального круга большого мозга
• «перианевризматическое» окружение – контакт аневризмы с ТМО, костями черепа, черепными нервами, артериями и венами
• множественные аневризмы
• наличие в анамнезе кровоизлияния из другой аневризмы
• курение
• артериальная гипертензия
При выявлении у больного НА размерами 3 мм и менее хирургическое лечение не показано, больному необходимо проведение динамического наблюдения с повторными обследованиями через 6, 12 месяцев и затем каждые 2 года [стандарт]. Подобному же наблюдению подлежат пациенты, отказавшиеся от хирургического лечения [стандарт].
При выявлении аневризм размерами от 3 до 7 мм необходимо измерение морфологических параметров аневризмы, вопрос о проведении хирургического лечения принимается индивидуально с учетом факторов риска (возраст, пол, наличие в анамнезе курения, гипертонической болезни, наличие «семейного» анамнеза, наличие генетических заболеваний) [рекомендации].
Больной с НА должен быть информирован о характере болезни, возможных вариантах течения, возможных осложнениях хирургического вмешательства [стандарт].
Обследование в нейрохирургическом стационаре [рекомендации]
После поступления больного в специализированный нейрохирургический стационар, помимо общих клинических исследований, необходимо провести:
— подробный неврологический осмотр;
— КТ-АГ или МР-АГ головного мозга при поступлении в том случае, если: с момента предыдущего исследования прошло более 6 месяцев; отмечено изменение в неврологическом статусе больного за время с момента выявления аневризмы до госпитализации; качество ранее выполненных КТ и/или МРТ низкое.
— проведение ДСА (в 2D и 3D режимах) показано пациентам со «сложными» аневризмами для оценки их морфологических особенностей и выбором тактики хирургического лечения; также больным с аневризмами размерами менее 7 мм для оценки их морфологических параметров и уточнения рисков разрыва.
Хирургические вмешательства у пациентов с неразорвавшимися церебральными аневризмами [рекомендации]
1) Микрохирургическое лечение:
— пациенты в возрасте до 60 лет
— аневризмы доступной локализации
— аневризмы большого и гигантского размера, оказывающие объемное воздействие на окружающие структуры
— частично тромбированные аневризмы
— при необходимости выполнения комбинированных (микрохирургическое выключение аневризмы из кровотока и реваскуляризирующие вмешательства) операций.
2) Эндоваскулярное лечение:
— пациенты в возрасте старше 60 лет
— локализация аневризм в вертебробазилярном бассейне, в области кавернозного отдела или офтальмического сегмента ВСА
— наличие декомпенсированных соматических заболеваний
Интраоперационный контроль эффективности прямого хирургического вмешательства [рекомендации]
Для подтверждения радикальности клипирования аневризмы и состоятельности кровотока по несущей артерии и функционально значимым ветвям выполняют следующее:
— пункция аневризмы и/или вскрытие просвета аневризмы
— визуальная оценка области клипирования (через микроскоп и/или эндоскоп)
— контактная интраоперационной допплерографии/флуометрия
— интраоперационная ангиография с использованием индоцианина зеленого
Оценка результатов операции и исходов лечения больных, динамическое наблюдение за пациентами после выключения аневризмы из кровотока
Окончательную оценку исходов проводят в сроки не ранее 6 месяцев после операции. Более раннюю оценку (при выписке больного) выполняют как промежуточный этап. Оценку исходов лечения проводят по шкале исходов Глазго.
Пациентам с оперированными церебральными аневризмами, вне зависимости от типа хирургического вмешательства, необходимо проведение контрольных обследований для исключения повторного заполнения аневризмы, оценки остаточной заполняющейся части аневризмы, а также для выявления аневризм de novo [63] [стандарт].
Для проведения динамического наблюдения за пациентами после операции возможно выполнение МР-ангиографии, КТ-ангиографии или ДСА.
Несмотря на то, что применение МР-ангиографии и КТ-ангиографии ограничивается наличием возможных артефактов от металлических имплантов, таких как клипсы, стенты и спирали, эти методы остаются достаточно эффективными для послеоперационного контроля [1, 2, 48, 88, 92]. Напряженность поля при выполнении контрольной МР-ангиографии должна быть 1,5 Тесла [опция].
Применение КТ-ангиографии для динамического наблюдения может быть ограничено в связи с нежелательностью рентгеновского облучения у ряда пациентов [70, 79, 98, 107].
Использование ДСА в качестве контрольного обследования у пациентов с оперированными аневризмами ограничено в связи с инвазивностью обследования и наличием радиационной нагрузки [24, 76].
После проведенного хирургического лечения контрольную ДСА в ранние сроки (до 2 недель после операции) выполняют в том случае, если аневризма не была полностью выключена, при сомнении хирурга в радикальности проведенной операции, или при подозрении на миграцию наложенного клипса. Повторное исследование после микрохирургической операции необходимо провести в течение 6-12 месяцев после вмешательства [рекомендация].
После выполнения эндоваскулярного вмешательства необходимо выполнение контрольного обследования (ДСА) в период от 6 до 12 месяцев после операции [1, 2, 3, 48, 72, 87, 92] [рекомендации]. Время последующих контрольных обследований зависит от характера окклюзии аневризмы при вмешательстве и первом контрольном обследовании, а также от состояния пациента. При наличии резидуальной аневризмы после эмболизации или стентирования обязательно проведение обследований в отдаленном периоде, так как возможны кровоизлияния и рост остаточной части аневризмы. Показано проведение серии контрольных обследований при аневризмах с широкой шейкой, больших и гигантских аневризмах, так как у них имеется высокий риск повторного заполнения [10, 93].
Всем пациентам, входящим в популяционные группы риска по формированию аневризм, независимо от вида оперативного вмешательства, после завершения периода наблюдения можно рекомендовать выполнение неинвазивных методов обследования (МР- или КТ-ангиографии) 1 раз в 5 лет для исключения формирования аневризм de novo [рекомендация].
Динамическое наблюдение за пациентами с неразорвавшимися церебральными аневризмами, не получавшими хирургического лечения [рекомендации]
Пациентам с неразорвавшимися аневризмами сосудов головного мозга, которые не получали хирургического лечения, необходимо проведение нейровизуализационного обследования в динамике для исключения роста аневризмы, изменения ее формы и появление других факторов риска ее разрыва [4, 11, 24, 25, 37, 42, 59, 64].
1) При отсутствии противопоказаний основной методикой для проведения динамического наблюдения является TOF MRA (времяпролётная магнитно-резонансная ангиография), а также у пациентов с почечной недостаточностью и тем, у кого имеет значение доза полученного рентгеновского облучения.
2) КТ-ангиография головного мозга является методом выбора у пациентов с противопоказаниями к проведению МРТ или при наличии аневризм, которые не могут быть правильно оценены с помощью МРТ (милиарные аневризмы менее 3 мм, «сложные» аневризмы).
3) Первое динамическое обследование после выявления неразорвавшейся аневризмы необходимо проводить в период от 6 до 12 месяцев [8, 33, 56, 112, 113]. Затем рекомендуется проводить обследование 1 раз в год или каждые 2 года при отсутствии признаков роста аневризмы и/или изменения ее других морфологических параметров (формы, расположение относительно несущего сосуда и т.д.) [113].
Госпитализация
Больного с неразорвавшейся аневризмой сосудов головного мозга, при наличии показаний к хирургическому лечению, необходимо госпитализировать в плановом порядке в стационары, где имеются:
— нейрохирургическое отделение;
— специалисты, владеющие опытом прямых микрохирургических операций по поводу церебральных аневризм;
— специалисты, владеющие опытом эндоваскулярного выключения аневризм;
— отделение лучевой диагностики, оснащенное аппаратурой для проведения КТ или МРТ, спиральной КТ-ангиографии, МР-ангиографии, ангиографическая операционная для проведения ДСА и выполнения эндовазальных операций;
— операционная, оснащенная оборудованием для микрохирургии церебральных аневризм (операционный микроскоп, микрохирургический инструментарий, съемные и постоянные немагнитные клипсы);
— отделение нейрореанимации.
Информация
Источники и литература
Информация
| Крылов Владимир Викторович | академик РАН, профессор, доктор медицинских наук, заведующий научным отделением неотложной нейрохирургии НИИ скорой помощи им. Н.В. Склифосовского, заведующий кафедрой нейрохирургии и нейрореанимации Московского государственного медико-стоматологического университета им. А.И. Евдокимова, главный внештатный специалист нейрохирург Министерства Здравоохранения Российской Федерации |
| Элиава Шалва Шалвович | Доктор медицинских наук, профессор, заведующий отделением сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Яковлев Сергей Борисович | Доктор медицинских наук, заведующий отделением эндоваскулярной нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Хейреддин Али Садек | Доктор медицинских наук, врач отделения сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Белоусова Ольга Бенуановна | Доктор медицинских наук, ведущий научный сотрудник отделения сосудистой нейрохирургии НИИ НХ им. акад. Н.Н. Бурденко |
| Полунина Наталья Алексеевна | Кандидат медицинских наук, научный сотрудник отделения неотложной нейрохирургии НИИ СП им. Н.В. Склифосовского |
Определение понятий
Стандарт
Общепринятые принципы диагностики и лечения, которые могут рассматриваться в качестве обязательной лечебной тактики (эффективность подтверждена несколькими рандомизированными исследованиями, мета-анализами или когортными клиническими исследованиями).
Рекомендация
Лечебные и диагностические мероприятия, рекомендованные к использованию большинством экспертов по данным вопросам. Могут рассматриваться как варианты выбора лечения в конкретных клинических ситуациях (эффективность подтверждена отдельными рандомизированными исследованиями или когортными клиническими исследованиями).
Опция
Лечебные и диагностические мероприятия, которые могут быть полезны (эффективность подтверждена мнением отдельных экспертов, в отдельных клинических случаях).
Не рекомендуется
Лечебные и диагностические мероприятия, не имеющие положительного эффекта или могущие принести вред (любой уровень подтверждения).